Clear Sky Science · tr
Dokuya özgü Drosophila metabolizmasının modellenmesi, yüksek şekerli diyetin kasta reaksiyon ve yol seviyelerinde neden olduğu metabolik düzensizliği tanımlıyor
Bu meyve sineği çalışması insan sağlığı için neden önemli
Beslenmemizdeki fazla şeker, vücudun yakıt yönetme kapasitesini zorlayabilir ve zaman içinde tip 2 diyabete katkıda bulunabilir. Bu çalışma, farklı dokuların metabolizmayı nasıl yönettiğini ve yüksek şekerli bir diyetin kas fonksiyonunu nasıl bozduğunu dikkat çekici ayrıntıda ortaya koymak için meyve sineklerini kullanıyor. Sinekler metabolik genler ve organ sistemleri bakımından insanlarla çok sayıda ortak noktaya sahip olduğu için, bu bulgular uzun süreli şeker aşırı yüklenmesi altında kendi kaslarımızda nelerin yanlış gidebileceğini anlamamıza yardımcı oluyor.
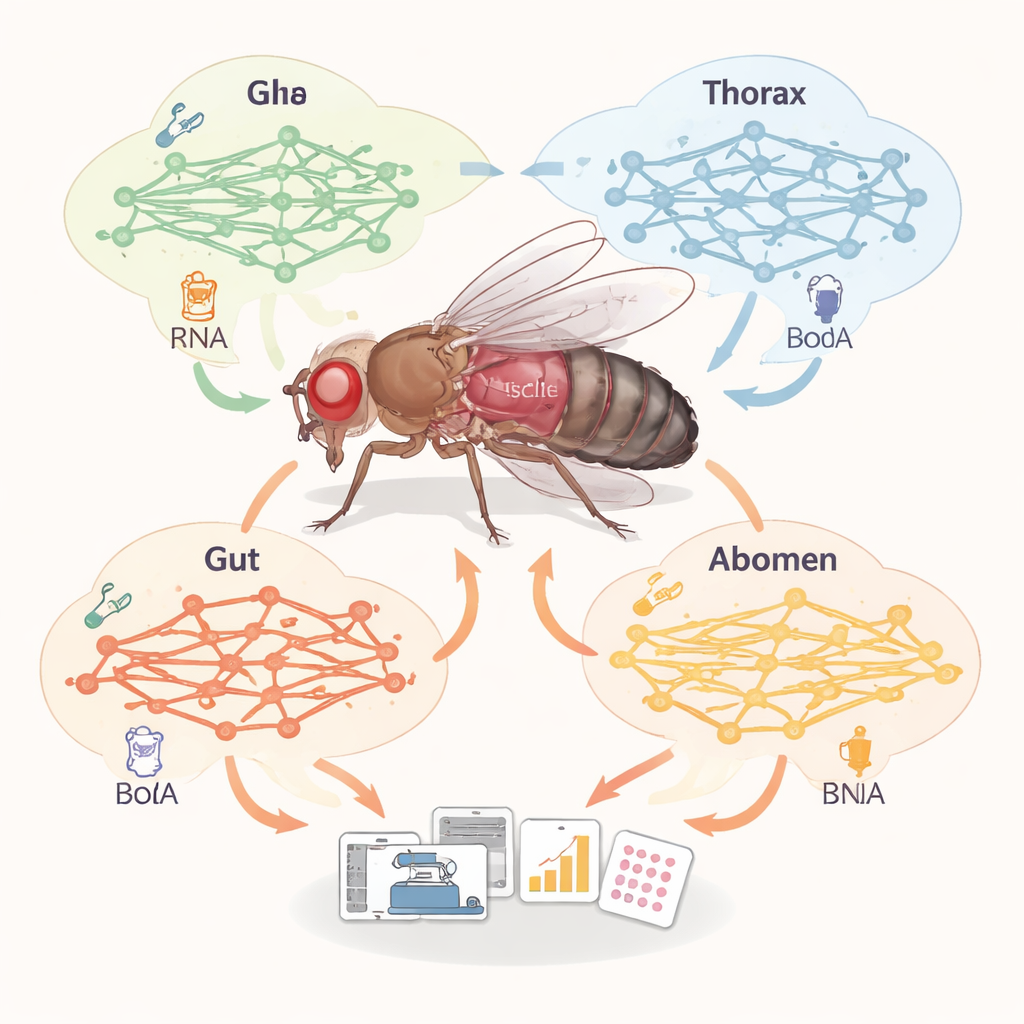
Doku dokuya metabolizmayı haritalama
Vücudumuz, meyve sineklerinde olduğu gibi, çok farklı metabolik rollere sahip dokulardan oluşur: kas yakıtı yakar, yağ depolar, bağırsak yiyeceği işler vb. Araştırmacılar, her enzimi doğrudan ölçmek yerine, 32 ayrı sinek dokusu için geniş ölçekli “metabolizma haritaları” — genom ölçekli metabolik modeller — oluşturdular. Mevcut, kürate edilmiş bir reaksiyon ağı ile her dokuda hangi metabolik genlerin aktif olduğunu gösteren tek hücre gen ifadesi verilerini birleştirdiler. Bu, her dokuya özgü ağda kaç reaksiyon, metabolit ve genin aktif olduğunu karşılaştırmalarına ve kas, yağ dokusu, bağırsak ve çeşitli sinir hücresi tiplerinde hangi yolların öne çıktığını görmelerine olanak sağladı.
Farklı organların farklı yakıt görevleri
Karşılaştırma, dokular arasında belirgin metabolik “kişilikler” ortaya koydu. İnsan yağ ve karaciğerine karşılık gelen yağ dokusu (fat body) ve oenositler en zengin reaksiyon setine sahipti; özellikle yağların beta-oksidasyon yoluyla yakılmasını sağlayan reaksiyonlar. Kas ise en geniş ağa sahip olmamakla birlikte, hücre içine ve dışına madde taşıyan reaksiyonların en yüksek oranına sahipti; bu da kasın vücudun geri kalanıyla yakıt ve yapı taşlarını değiştirmek için önemli bir merkez olduğunu düşündürüyor. Bilim insanları ayrıca öngörülen yolların farklı beden bölgelerinde ölçülen gerçek metabolit desenleriyle uyumlu olup olmadığını da kontrol ettiler. Hedefe yönelik metabolomik kullanarak sinek başları, toraksları, bağırsakları ve karın bölgelerinden yüzlerce küçük molekülü analiz ettiler ve veride zenginleşen yolların modellerin öngördükleriyle örtüşüp örtüşmediğini sorguladılar. Kas ve yağ dokusunda eşleşme güçlüydü; bu da dokuya özgü modellerin, yalnızca gen ifadesinden daha iyi gerçek biyolojiyi yakaladığını gösterdi.
Yüksek şekerli diyetin kas yakıt akışına etkisi
Doğrulanmış bir kas modeliyle ekip, sineklerin uzun süreli yüksek şekerli diyetle beslendiğinde — tip 2 diyabetin iyi kurulmuş bir modeli — neler olduğunu simüle etti. Modeli diyabetik kastaki bilinen özelliklerle, örneğin azalmış glukoz alımı ve mitokondrideki merkezi enerji döngüsündeki yavaşlamış aktivite gibi kısıtlayarak çalıştırdılar. Hesaplamalı “akış” analizleri — reaksiyonların ne kadar hızlı çalışabileceğinin hesapları — elektron taşıyan ve enerji üretimi için temel olan redoks çifti NAD/NADH’ye bağımlı reaksiyonlarda geniş çaplı azalmalar gösterdi. Özellikle merkezi şeker yakma yolu olan glikolizdeki reaksiyonlar, GAPDH enziminin katalizlediği adımlar da dahil olmak üzere yavaşladı. Model ayrıca kasın genel NADH üretme kapasitesinde yaklaşık dörtte birlik bir düşüş öngördü; bu da redoks dengesinin etkilendiğine işaret ediyor. Sinek torasik kasındaki doğrudan ölçümler, yüksek şekerli diyette NAD ile NADH oranının gerçekten düştüğünü doğruladı.
İzotoplu şekeri ve oksitlenmiş proteinleri izlemek
Bu öngörülen darboğazların yaşayan hayvanlarda gerçekten meydana gelip gelmediğini görmek için araştırmacılar, sinekleri tamamen etiketli karbon-13 glukoz içeren yüksek şekerli bir diyetle beslediler ve etiketli karbonun nereye gittiğini takip ettiler. GAPDH’nin yukarısındaki erken glikoliz ara ürünlerinin biriktiğini, buna karşın aşağıdaki ürünlerin ve etiketli paylarının düştüğünü buldular; bu, bu adımda ve sonrasında gerçek bir yavaşlamaya işaret ediyor. Benzer şekilde, glukoz karbonunun merkezi enerji döngüsüne katkıları azaldı. Aynı zamanda redoks proteomik — proteinlerdeki belirli amino asitlerdeki oksidatif değişiklikleri tespit eden bir yöntem — birçok glikolitik enzimin, GAPDH dahil, artan oksidasyonunu gösterdi. Glikoliz genelinde, daha fazla oksidatif modifikasyon taşıyan enzimlerin, genellikle protein düzeyleri büyük ölçüde değişmemesine rağmen, öngörülen akışlarda daha büyük düşüşler gösterme eğiliminde olması dikkat çekiciydi. Bu, enzim bolluğunun azalmasından ziyade oksidatif stresten kaynaklanan kimyasal hasarın kaslarda şeker işlemeyi bozmanın önemli bir sürücüsü olduğunu düşündürür.
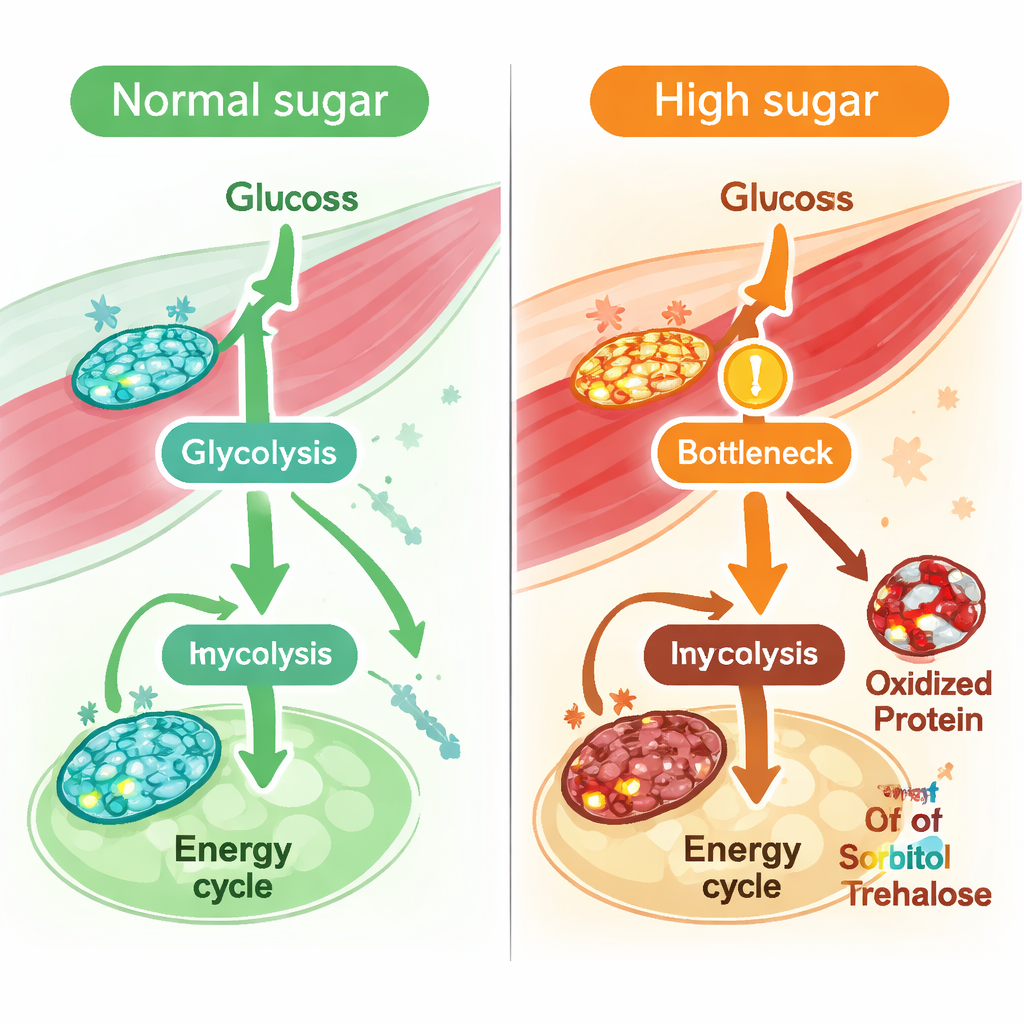
Fruktoz ve sukroz işlenmesinde gizli sorunlar
Tek tek reaksiyonların ötesine bakarak ekip, hangi yolların yüksek şekerle en çok bozulduğunu görmek için akışları tüm yollar bazında ortaladı. Glikoliz, enerji döngüsü ve oksidatif fosforilasyon hepsi azalmalar gösterdi, ancak en güçlü öngörülen düşüşlerden biri fruktoz metabolizmasındaydı. Kasın metabolit profillemesi bu fikri destekledi: sorbitol ve trehaloz/sukroz seviyeleri arttı ve trehalozu glukoza dönüştüren anahtar enzim Trehalaz hem azalmış öngörülen aktivite hem de hassas bir metiyonin kalıntısında artmış oksidasyon gösterdi. Birlikte ele alındığında, bu bulgular kronik şeker aşırı yüklenmesi altında kasın diyetsel şekerleri — özellikle fruktoz benzeri ve sukroz kaynaklı yakıtları — işlemesinde daha geniş bir bozulmaya işaret ediyor.
Bu, diyabeti anlamak için ne anlama geliyor
Düz ifadeyle, bu çalışma çok fazla şekerin sadece kan dolaşımını aşırı yüklemediğini; aynı zamanda kas hücrelerinin yakıt yollarını ve yakma biçimlerini sessice yeniden şekillendirdiğini gösteriyor. Meyve sineği için ayrıntılı, dokuya özgü metabolik haritalar oluşturup bunları metabolomik, izotop izleme ve redoks proteomikle çapraz kontrol ederek araştırmacılar, yüksek şekerin redoks stresini artırdığını, GAPDH gibi ana glikolitik enzimleri oksitlediğini, şeker parçalanmasını yavaşlattığını ve fruktoz ile ilişkili yolları bozduğunu ortaya koyuyor. Oldukça elverişli bir model organizmada elde edilen bu içgörüler, insan kasında tip 2 diyabeti önlemek veya tedavi etmek için hangi reaksiyonların ve yolların korunması veya onarılmasının önemli olabileceğini belirlemeye yönelik güçlü bir çerçeve sunuyor.
Atıf: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Anahtar kelimeler: Drosophila metabolizması, dokuya özgü metabolik modeller, yüksek şekerli diyet, kas glikolizi, redoks düzenlemesi