Clear Sky Science · tr
Tmem110, TRPML1 konformasyonunu düzenleyerek endolizosomal homeostazı korur ve mitokondriyal DNA sızıntısını ile patolojik kendi‑DNA işlenmesini önler
Yaralanma sonrası dökülen DNA neden önemli
Ağır bir travma, örneğin kafa üzerine alınan büyük bir darbe yaşadığımızda, hasar sadece yaralanma bölgesiyle sınırlı kalmaz. Birçok hasta daha sonra akciğerlerin, karaciğerin, böbreklerin ve diğer organların işlevinin bozulduğu tehlikeli bir tüm‑vücut reaksiyon geliştirir. Bu çalışma, hücre içindeki küçük yapılardan — lizozomlar, mitokondriler ve bağışıklık sensörleri — birbirleriyle nasıl konuştuğunu, artıkların sessizce temizlenip temizlenmeyeceğine ya da kendi kendine yönelen bağışıklık saldırısına dönüşüp dönüşmeyeceğine nasıl karar verildiğini ortaya koyuyor. Bu gizli temizleme sistemini anlamak, travma sonrası organ yetmezliğini önlemenin ve otoimmün ile enflamatuar hastalıkları tedavi etmenin yeni yollarını açabilir.
Kafa yaralanmasından tüm vücut krizine
Travmatik beyin yaralanması (TBY), çok organ disfonksiyonu sendromu (MODS) olarak adlandırılan güçlü bir iltihap fırtınasını tetikleyebilir, ancak beyneki hasarın uzak organlara nasıl yayıldığı belirsizdi. Yazarlar, kanda ve dokularda devriye gezen ve profesyonel çöp toplayıcılar gibi çalışan monositler ve makrofajlara odaklanıyor. TBY sonrası hücreler kontrolsüz şekilde ölür ve kendi DNA’larını taşıyan küçük enerji fabrikaları olan bütün mitokondrileri dolaşıma salar. Bu mitokondriyal DNA (mtDNA) bağışıklık sistemi için bakteriyel DNA gibi görünür ve hızla temizlenmezse güçlü antiviral tarzı savunmaları açabilir. Normalde hücreler bu sürüklenen mitokondrileri lizozom adı verilen asidik bölmelere alır; burada enzimler DNA’yı hücre sıvısına sızmadan önce sindirir. 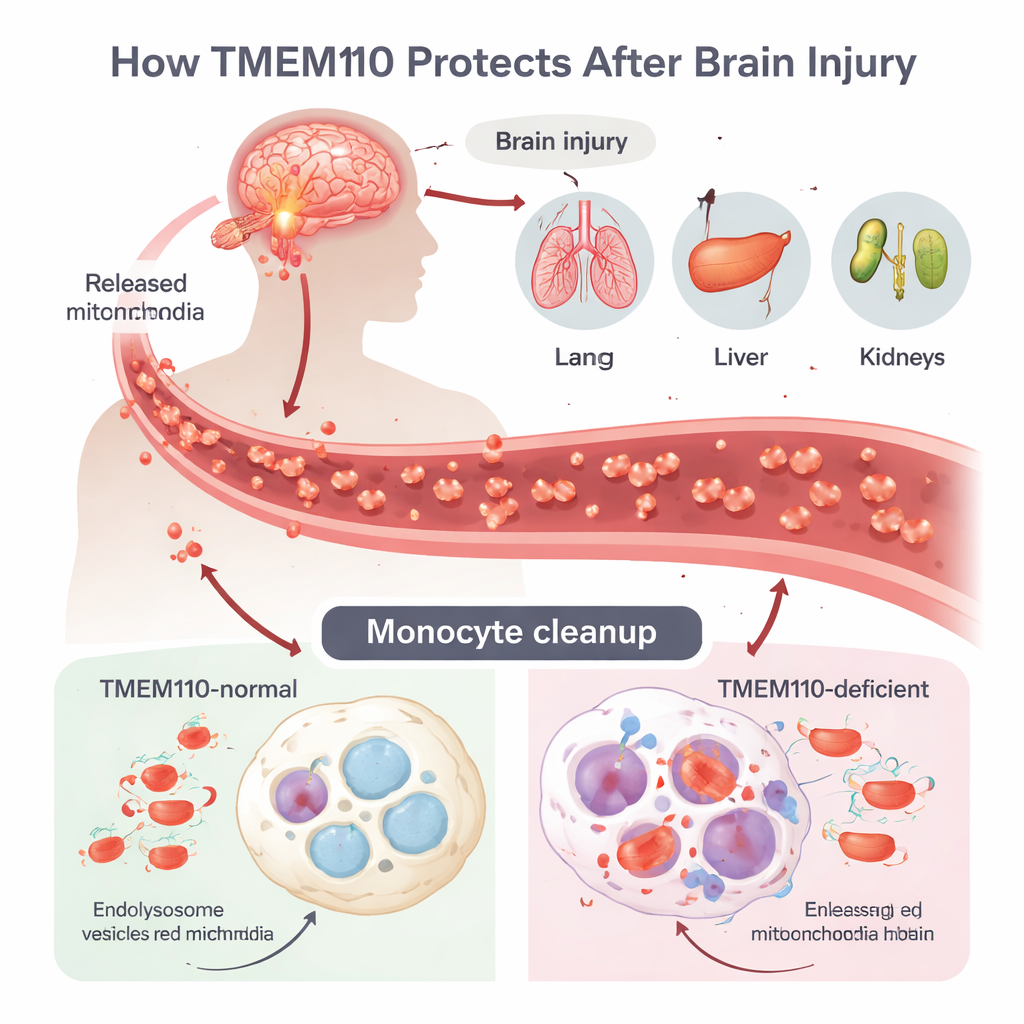
Lizozomları kararlı tutan bir kapı bekçisi protein
Ekip, bu süreçte endoplazmik retikulum zarını (büyük bir hücre içi zar ağı) geçen bir protein olan TMEM110’u kritik bir kapı bekçisi olarak tanımladı. Sadece monositler ve makrofajlarda TMEM110 eksik olan genetik olarak değiştirilmiş fareler kullanarak kontrollü bir beyin yaralanması modeli oluşturdular. Normal farelerle karşılaştırıldığında, TMEM110 eksik hayvanlarda kanda ve beyin‑omurilik sıvısında çok daha yüksek düzeyde tip I interferon—güçlü antiviral sinyal molekülleri—görüldü. Akciğerleri, karaciğerleri, böbrekleri ve lenf düğümleri daha ciddi hasar gösterdi ve TBY sonrası uzun dönem sağkalım belirgin şekilde daha kötüydü. Araştırmacılar tip I interferon reseptörünü engellediklerinde veya mutant kemik iliğini normal hücrelerle değiştirdiklerinde organ hasarı ve ölüm oranları düştü; bu da periferik monositlerden aşırı interferon sinyalinin bu bağlamda MODS’un önemli bir sürücüsü olduğunu gösteriyor.
Hatalı iyon yönetiminin DNA’nın kaçmasına izin vermesi
Bu bağışıklık hücrelerinin içine giren araştırmacılar, TMEM110 eksik lizozomların kimyasal olarak dengesiz olduğunu buldular: daha az asidikti ve kalsiyumla aşırı yüklüydü. Bu koşullar altında lizozomlarda normalde DNA’yı parçalayan DNase II enzimi aktivitesini yitirdi, lizozomal membranlar kırılganlaştı ve mtDNA çevreleyen sitozole sızdı. Etiketlenmiş verici mitokondrileri yutan insan monositleriyle yapılan laboratuvar deneyleri, TMEM110 olmadan daha fazla mtDNA’nın hücre sıvısına sızdığını ve interferon‑ile uyarılmış genlerin patlamasını tetiklediğini doğruladı. Çalışma, TMEM110’un lizozomal iyon kanalı TRPML1’i kontrol ederek işlediğini gösteriyor. TMEM110 bulunduğunda TRPML1 ile fiziksel temas kurar ve onu lizozom yüzeyinde küçük kalsiyum salım sıcak noktaları oluşturan “açık” bir konformasyona kaydırır. Bu kontrollü kalsiyum akımları doğru asiditeyi korumaya, membran onarımını desteklemeye ve mtDNA’yı içeride tutup parçalanmış halde kalmasını sağlamaya yardımcı olur. 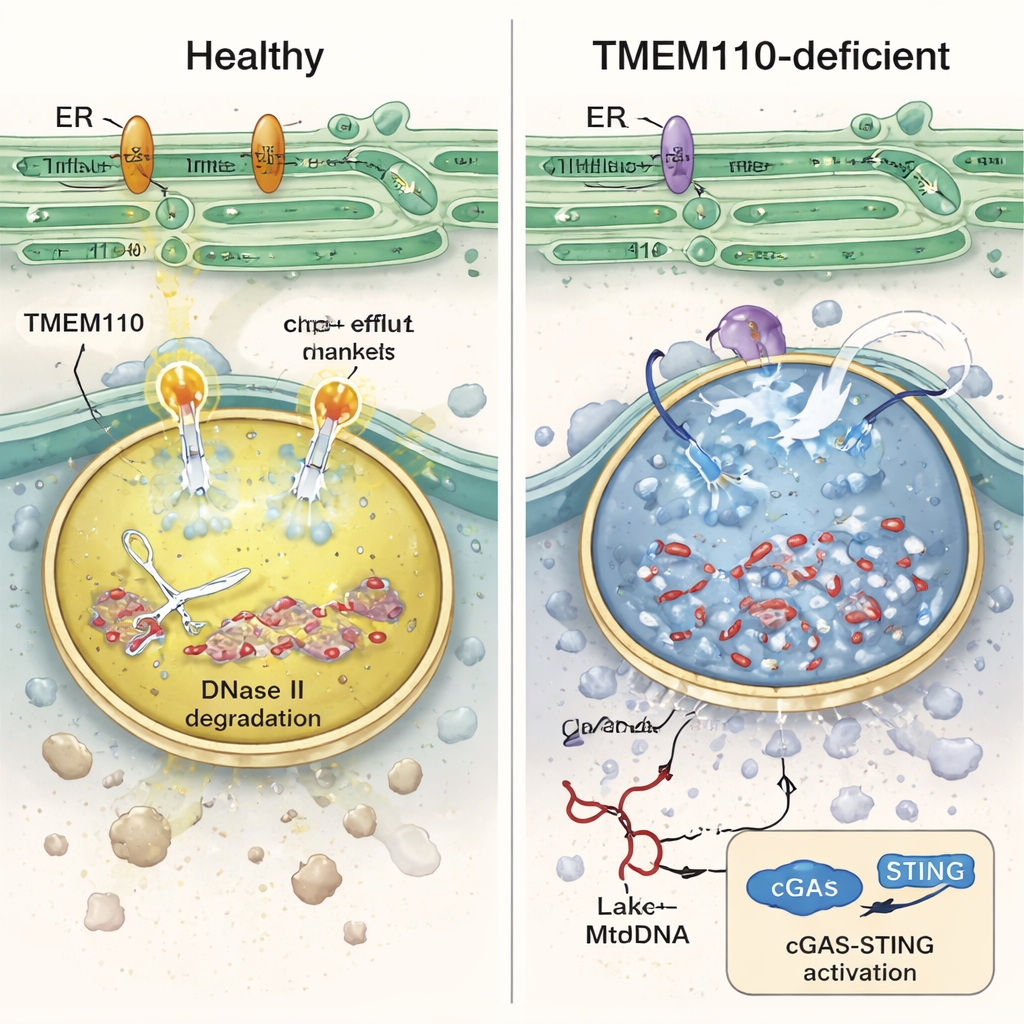
Hücresel DNA alarm sistemiyle geri besleme döngüsü
MtDNA sitozole sızdığında, hücrenin yabancı DNA için ana alarm sistemi olan cGAS–STING yolu tarafından tanınır. İlginç şekilde TMEM110 dinlenme halinde de STING’e bağlanır ve gereksiz alarmı önlemek için onu endoplazmik retikulumda tutulmuş halde bırakır. Sitoplazmik DNA biriktiğinde, STING aktive olur ve TMEM110 üzerindeki tutuşunu gevşetir. Bu da TMEM110’un TRPML1 ile etkileşen farklı bir bölgesini açığa çıkarır ve lizozomal kalsiyum çıkışını artırarak bir geri besleme döngüsü oluşturur: kendi DNA’sının algılanması, DNA temizliğini artıran bir mekanizmayı etkinleştirir. İnsan otoinflamatuvar sendromlarında bulunan hastalık ilişkili STING mutasyonları bu el değiştirmeyi bozarak TMEM110’u inhibe edilmiş bir durumda sıkışmış hale getirir ve kronik interferon aktivasyonuna katkıda bulunur. Böyle bir STING mutasyonu taşıyan farelerde TBY daha kötü organ hasarı ve daha yüksek mortaliteye yol açtı, ancak lizozomlara hedeflenen küçük bir TMEM110 fragmanının mRNA‑lipid nanopartikül terapisi ile verilmesi mtDNA kontrolünü kısmen geri getirip sağkalımı iyileştirdi.
Hastalarla elde edilen ipuçları ve yeni tedavilere yollar
Daha sonra yazarlar, travma ilişkili beyin yaralanması ve MODS olan 143 kişilik klinik bir kohorta yöneldiler. Yaralanma sonrası erken dönemde monositlerinde daha yüksek TMEM110 düzeyine sahip olan hastalar organ fonksiyonunu geri kazanma ve hayatta kalma şansına daha çok sahipti. Daha düşük TMEM110’e sahip olanlarda daha fazla dolaşımdaki mtDNA ve hücresizleşmiş mitokondri, daha güçlü interferon yanıtları, daha yüksek organ yetmezliği skorları ve DNA ile nükleer proteinlere karşı antikorlar da dahil olmak üzere daha geniş otoantikor profilleri görüldü. Bu desenler farelerdeki bulgularla yakından örtüşerek TMEM110 kaynaklı lizozomal stabilite ve mtDNA bertarafının insan hastalığında paylaşılan bir mekanizma olduğu fikrini destekliyor.
Ağır travma geçiren hastalar için bunun anlamı
Günlük ifadeyle, bu çalışma büyük bir yaralanma sonrası bağışıklık sistemimizin hassas bir seçimle karşı karşıya olduğunu gösteriyor: ölen hücrelerden yayılan öz‑DNA selini sessizce sindirmek mi, yoksa onu viral bir istila olarak yorumlayıp kendi organlarımıza zarar verebilecek tam ölçekli bir saldırı mı başlatmak mı. TMEM110, bir lizozomal iyon kanalını ayarlayarak ve DNA sensörü STING ile koordinasyon sağlayarak hücrelerin daha güvenli yolu seçmesine yardımcı olur. Bu sistem başarısız olduğunda—TMEM110 eksikse, STING mutasyona uğramışsa veya lizozomlar aşırı yüklenmişse—mtDNA kaçar, alarm sürekli çalar ve çoklu organ hasarı ortaya çıkar. TMEM110–TRPML1–STING eksenini hedeflemek, örneğin lizozom yönelimli mRNA terapileri ile, ağır travma sonrası organ yetmezliğini ve otoimmün benzeri komplikasyonları önlemenin veya tedavi etmenin yeni bir yolunu sunabilir.
Atıf: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Anahtar kelimeler: travmatik beyin yaralanması, mitokondriyal DNA, lizozomlar, tip I interferon, cGAS‑STING yolu