Clear Sky Science · tr
İnsan COP1-DET1 ubiquitin ligaz kompleksinin kriyo-EM yapısı
Hücreler Hangi Proteinleri Yok Edeceklerine Nasıl Karar Verir
Her hücre içinde, binlerce proteinin doğru zamanda sürekli olarak inşa edilmesi, yeniden düzenlenmesi veya yok edilmesi gerekir. Bu makale, kanser ve gelişimle bağlantılı güçlü gen düzenleyicilerini ne zaman ortadan kaldıracağına karar veren hücrenin temel “kalite kontrol” makinelerinden birine, moleküler bir öğütücüye odaklanıyor. Yazarlar üç boyutlu yapısını yakın-atomik ayrıntıda ortaya koyarak, bu makinenin etkin olmayan, üst üste yığılmış bir durum ile alt tabakayı işleyen, aktif bir form arasında nasıl geçiş yapabildiğini gösteriyor—bu içgörü sonunda onu açıp kapatacak ilaçların tasarlanmasına yardımcı olabilir.
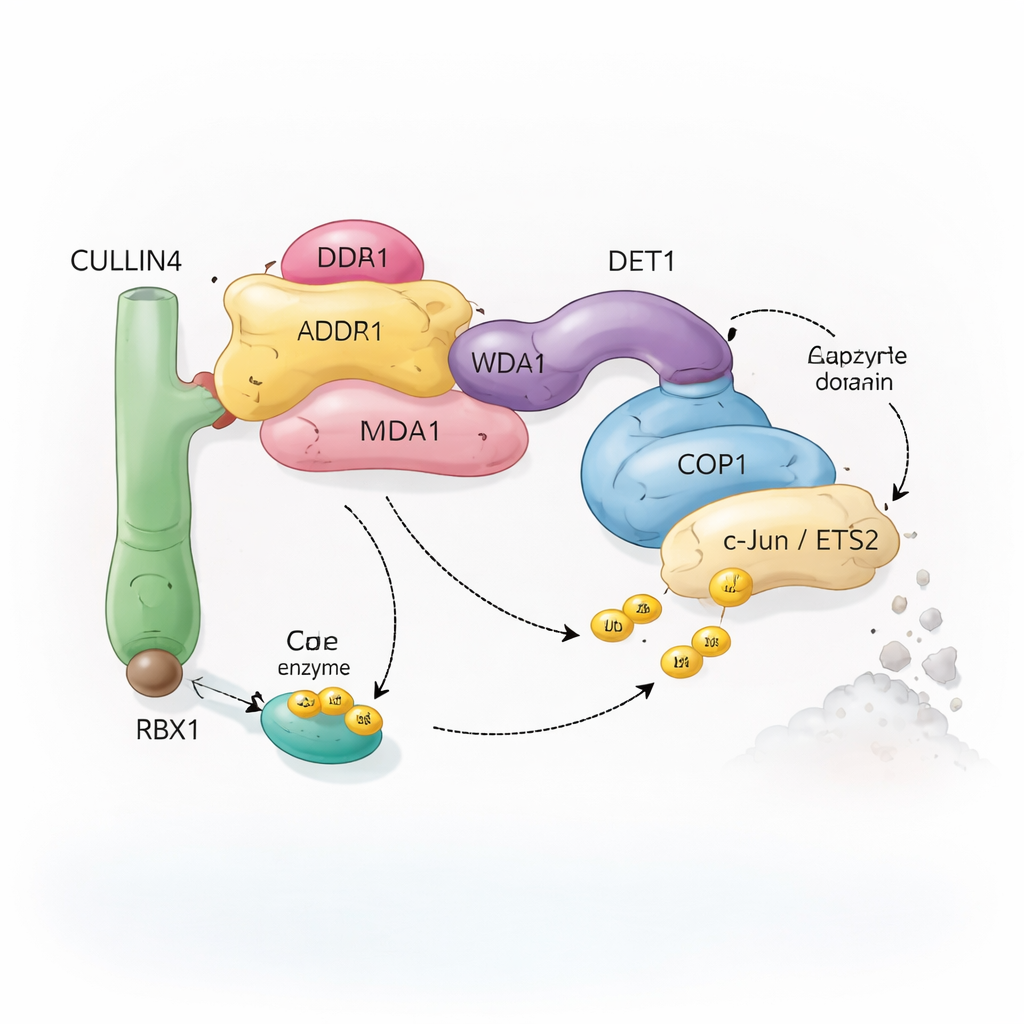
Çok Parçalı Moleküler Bir Geri Dönüşüm Ekibi
Hücreler, proteinleri geri dönüşüme işaretlemek için ubiquitinasyon adı verilen bir sisteme güvenir. Küçük ubiquitin molekülleri, bir proteine değiştirilip değiştirilmemesi, yeniden yerleştirilmesi veya yok edilmesi gerektiğini söyleyen çıkarılabilir bayraklar gibi davranır. Ubiquitin ligaz adı verilen özel enzim kompleksleri bu bayrakları seçilmiş hedeflere ekler. Burada incelenen kompleksin odağı, bitkilerden insanlara kadar bulunan ve önemli transkripsiyon faktörlerini—hangi genlerin açılıp kapatılacağını kontrol eden proteinleri—etiketlemeye yardımcı olan COP1 proteinidir. COP1 tek başına çalışmaz: CULLIN4 adlı bir iskelesel proteinin etrafında inşa edilen daha büyük bir düzenek içine takılabilir ve DDB1, DDA1 ve DET1 adlı birkaç adaptörü içerir. Birlikte, bu bileşenler c‑Jun ve ETS2 gibi, çoğu hücre büyümesi ve kanserle ilgili olan belirli transkripsiyon faktörlerini tanıyan esnek bir “geri dönüşüm ekibi” oluşturur.
Kompleksi 3B'de Yakalamak
Bu ekibin nasıl çalıştığını anlamak için araştırmacılar tek parçacık kriyo-elektron mikroskopisini kullandılar; bu teknik, şokla dondurulmuş proteinleri görüntüler ve yüksek çözünürlükte şekillerini yeniden yapılandırır. İnsan COP1–DET1 sistemini kültür hücrelerinde yeniden oluşturdular, kompleksleri saflaştırdılar ve birkaç farklı yapısal durumu görselleştirdiler. Önce merkezi bir merkez görevi gören DDB1–DDA1–DET1 modülünün yapısını çözdüler. DET1 katı bir disk yerine olağandışı, kısmen esnek bir şekil alıyor ve ortaklara tutunabilen dışa doğru çıkıntılı bir “pençe” barındırıyor. Ardından COP1 ve E2 olarak bilinen yardımcı enzim sınıfını ekleyerek, tüm parçaların nasıl bir araya geldiğini gösteren daha büyük düzenekleri yakaladılar; bu düzenekler hem sıkı yığılmış paketleri hem de daha açık dimetik (iki‑COP1) düzenlemeleri ortaya koydu.
İnaktif Bir Yığın ve Aktif Bir Dimer
En çarpıcı bulgulardan biri, kompleksin tekrarlayan katmanlarından oluşan yığınlı, filament benzeri bir yapıdır. Her katmanda, sekiz COP1 molekülü burgu‑kılıf segmentleri aracılığıyla iç içe geçerek elmas şeklinde bir halka oluşturur. Substrat tanıma bölgeleri olan WD40 domenleri hepsi tek bir yöne bakar ve komşu katmanlar tarafından kısmen örtülür. Bu sıkı paketlenme, hedef proteinlerin erişiminin sınırlı olduğu “kapalı” yani devre dışı bir durumu temsil ediyor olabilir. Buna karşılık, ekip COP1 substratları (c‑Jun veya ETS2 gibi) ile birlikte eş‑ekspres etmiş kompleksleri incelediğinde farklı, dimerik bir form gördü: iki COP1 molekülü yan yana dizilmiş, WD40 domenleri dışa bakıyor ve birçok transkripsiyon faktöründe bulunan kısa “VP” motiflerini bağlanmaya hazır durumda. Biyokimyasal testler yalnızca bu dimerik durumun c‑Jun üzerinde uzun ubiquitin zincirleri inşa etmeyi etkin şekilde desteklediğini doğruladı.
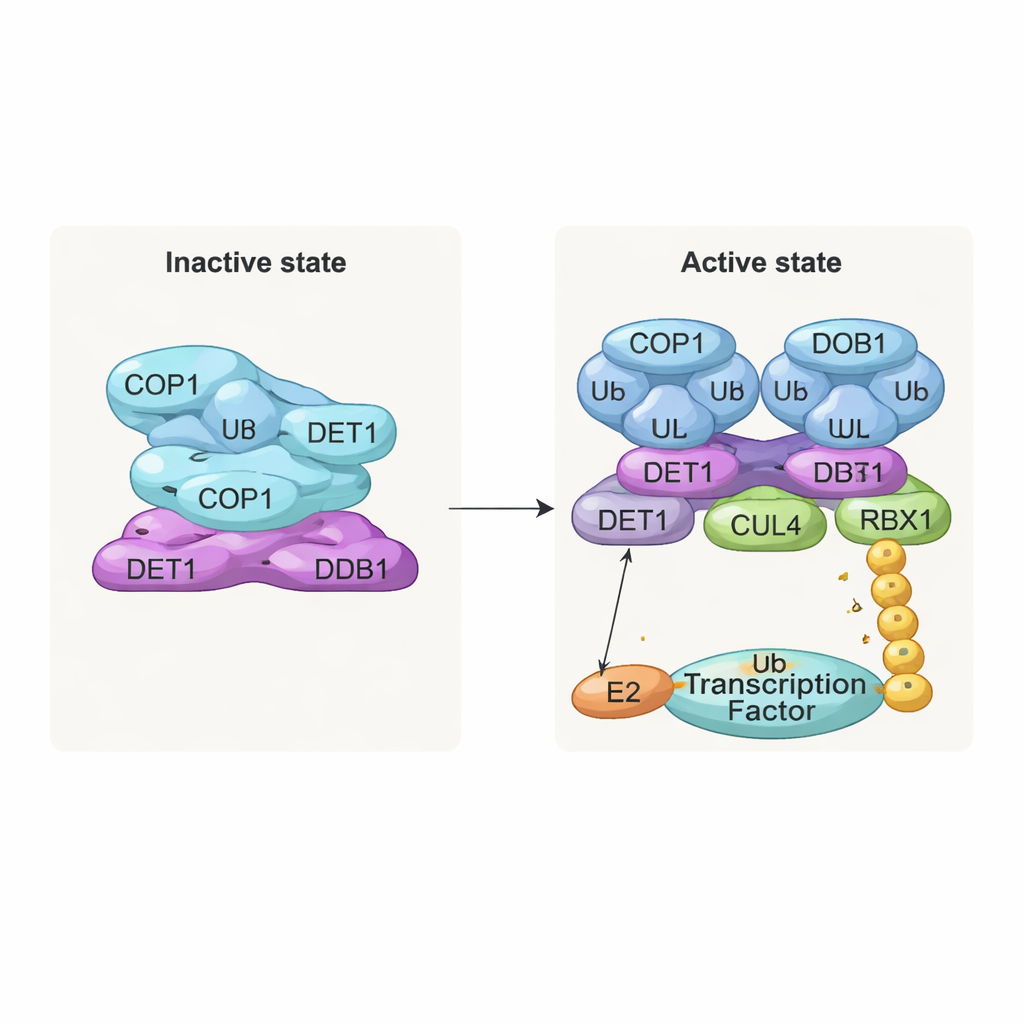
DET1: Esnek Bir Köprü ve Trafik Yöneticisi
DET1, makinenin tüm parçalarını birleştiren ana düzenleyici olarak ortaya çıkıyor. N‑terminal bölgesi DDB1’in içine yuvalanarak kompleksi CULLIN4 iskelesine sabitlerken, pençe bölgesi Ube2e adlı E2 enzim ailesini sarıyor. Ayrıntılı mutasyonel deneyler, E2’leri doğrudan kavrayanın COP1 değil DET1 olduğunu gösteriyor; DET1 onları COP1’in katalitik RING bölgesine yakın konumlandırıyor. Bu düzende Ube2e, substrata ilk ubiquitin etiketlerini yerleştirmeye yardımcı oluyor gibi görünüyor. İkinci bir E2 enzimi olan Ube2d3 ise bu etiketleri tam yıkımı işaretleyen daha uzun zincirlere uzatmak üzere CULLIN4–RBX1 kolu aracılığıyla işe çağrılıyor. Başka bir deyişle, DET1 bir E2’yi COP1’e sunan esnek bir köprü görevi görürken, daha büyük iskelesel yapı işi bitirmek için ikinci bir E2 getiriyor.
Sağlık ve Hastalık Açısından Neden Önemli
Bu yapısal durumları ve aktivitelerini haritalayarak çalışma, aynı protein setinin nasıl boşta, üst üste yığılmış bir form ile transkripsiyon faktörlerini hedef alan aktif bir dimer arasında geçiş yapabileceğini açıklıyor. Bu anahtar bir geçiş özellikle hücre bölünmesini tetikleyen ve yanlış düzenlendiğinde kansere sıkı sıkıya bağlı olan c‑Jun gibi faktörler için önemlidir. COP1 ve DET1’in nasıl işbirliği yaptığını—DET1’in pençesinin belirli E2 enzimlerini nasıl seçtiğini, COP1’in WD40 yüzeyinin VP içeren substratları nasıl tanıdığını ve aktif dimerin nasıl oluştuğunu—anlamak gelecekteki çalışmalar için bir kılavuz sunuyor. Uzun vadede, inaktif yığını stabilize eden veya aktif dimeri tercih eden ilaçlar, protein yıkımının bozulduğu kanser ve diğer hastalıklarda gen kontrol yollarını ayarlamak için yeni yollar sağlayabilir.
Atıf: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Anahtar kelimeler: ubiquitin ligaz, COP1, protein yıkımı, kriyo-EM yapısı, c-Jun