Clear Sky Science · tr
Fsr paylaşımlı algısının kaybı, enterokokal infektif endokarditte biyofilm oluşumunu artırır ve sonuçları kötüleştirir
Kalp kapaklarındaki sessiz sabotajcılar
İnfektif endokardit, kalp kapaklarının yaşamı tehdit eden bir enfeksiyonudur ve dünya çapında giderek daha yaygın hale gelmektedir. Bu çalışma, başlıca suçlulardan biri olan bağırsak bakterisi Enterococcus faecalis’e odaklanıyor ve bazı enfeksiyonların neden özellikle zor tedavi edildiğini sorguluyor. Araştırmacılar, bu bakterilerin birbirleriyle nasıl iletişim kurup kalp kapaklarında koruyucu biyofilm inşa ettiklerini çözdükçe, bazı suşların neden daha şiddetli hastalığa neden olduğunu ve antibiyotiklere nasıl direnç gösterdiklerini ve Fsr adındaki bir bakteriyel iletişim sisteminin beklenmedik biçimde bir hızlandırıcı değil, hasarı sınırlayan bir fren olduğunu ortaya koyuyor.
Bakteriler kalpte nasıl kale kurar?
Kalp kapakları normalde vücutta en hızlı kan akımlarına maruz kalan yapılardandır, ancak kapak yüzeyi zarar görürse plateletler ve pıhtılaşma proteinleri küçük bir pıhtı veya vegetasyon oluşturabilir. Bu pıhtı, kanda dolaşan bakteriler için bir iniş yeri haline gelir. Bir kez tutunduklarında bakteriler çoğalır ve kendilerini bağışıklık hücreleri ve ilaçlardan koruyan yapışkan, yapılandırılmış bir topluluk olan bir biyofilm içine örerler. Ekip, laboratuvarda kan akışını taklit etmek için mikroakışkan cihazlar ve canlı hayvanlarda endokarditi yeniden oluşturmak için bir sıçan modeli kullandı; bu sayede E. faecalis’in enfeksiyonun birkaç dağılmış hücreden kalın, olgun biyofilm hâline ilerlerken nasıl uyum sağladığını izleyebildiler. 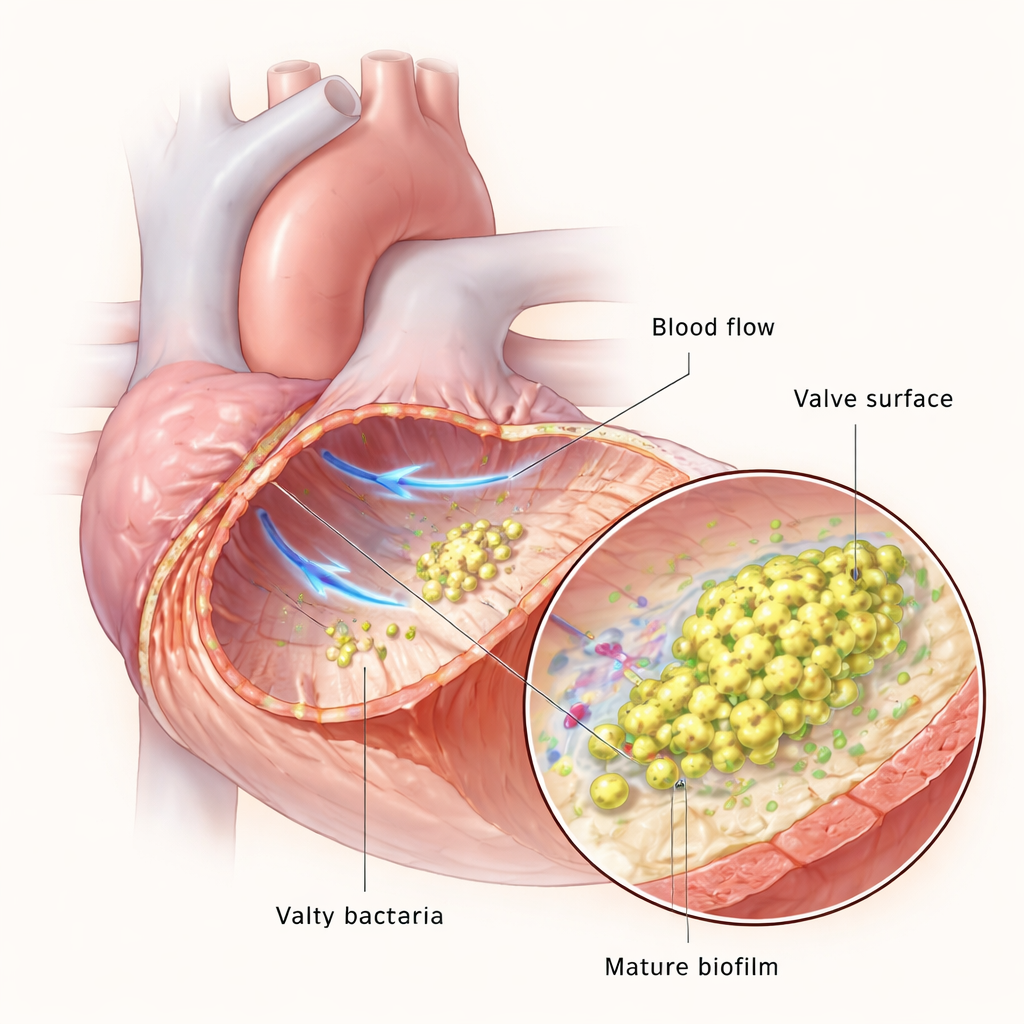
Hızlı kan akışı bakteriyel “sohbeti” kapattığında
Bakteriler sıklıkla davranışlarını, yeterli sayıda hücre biriktiğinde genleri açıp kapatan kimyasal bir “oylama” sistemi olan quorum sensing ile koordine eder. Fsr, E. faecalis’in kullandığı quorum sensing sistemidir. İlginç biçimde araştırmacılar, güçlü ve hareketli sıvının Fsr’nin aktive olması için gerekli sinyal moleküllerini gerçekte yıkayıp uzaklaştırdığını buldular. Erken enfeksiyon döneminde, bakteriler vegetasyonun açık yüzeyine tutunmuş ve kan akışının tam gücünü hissediyorken Fsr büyük ölçüde sessiz kalıyor. Ancak daha sonra mikrokoloniler büyüyüp vegetasyonun daha derinlerine gömüldükçe—akımdan korunmuş olarak—Fsr etkinleşiyor. Bu, gerçek kalpte quorum sensing’in sadece bakteri sayısına değil, aynı zamanda onların üç boyutlu yapı içindeki konumlarına bağlı olduğunu gösteriyor.
Fsr kapandığında biyofilmler kontrolsüz büyüyor
Fsr’nin enfeksiyon için gerçekte ne yaptığını sınamak üzere ekip, normal bakteriler ile tüm Fsr sisteminden yoksun mutantları karşılaştırdı. Erken dönemde her iki tür de kapakları eşit ölçüde kolonize etti. Ancak üç gün sonunda, Fsr-eksik suşlarla enfekte hayvanlarda daha büyük vegetasyonlar ve içlerine çok daha fazla bakterinin paketlendiği görüldü. Ayrıntılı görüntüleme, bu suşların biyofilmlerinin pıhtının yüzeyini daha fazla örttüğünü ve mikrokolonilerinin daha büyük olduğunu gösterdi. Fsr kaybı ayrıca biyofilmi şekillendirmeye ve aşırı büyümeyi sınırlamaya yardımcı olan iki ana salgılanan enzim olan GelE ve SprE’yi devre dışı bıraktı. Sadece bu enzimlerden yoksun mutantlarla enfekte hayvanlar da daha hacimli biyofilmler geliştirdi, ancak Fsr-null suşlarda görülen kadar aşırı değildi; bu da başka Fsr kontrollü faktörlerin de rol oynadığını düşündürüyor. 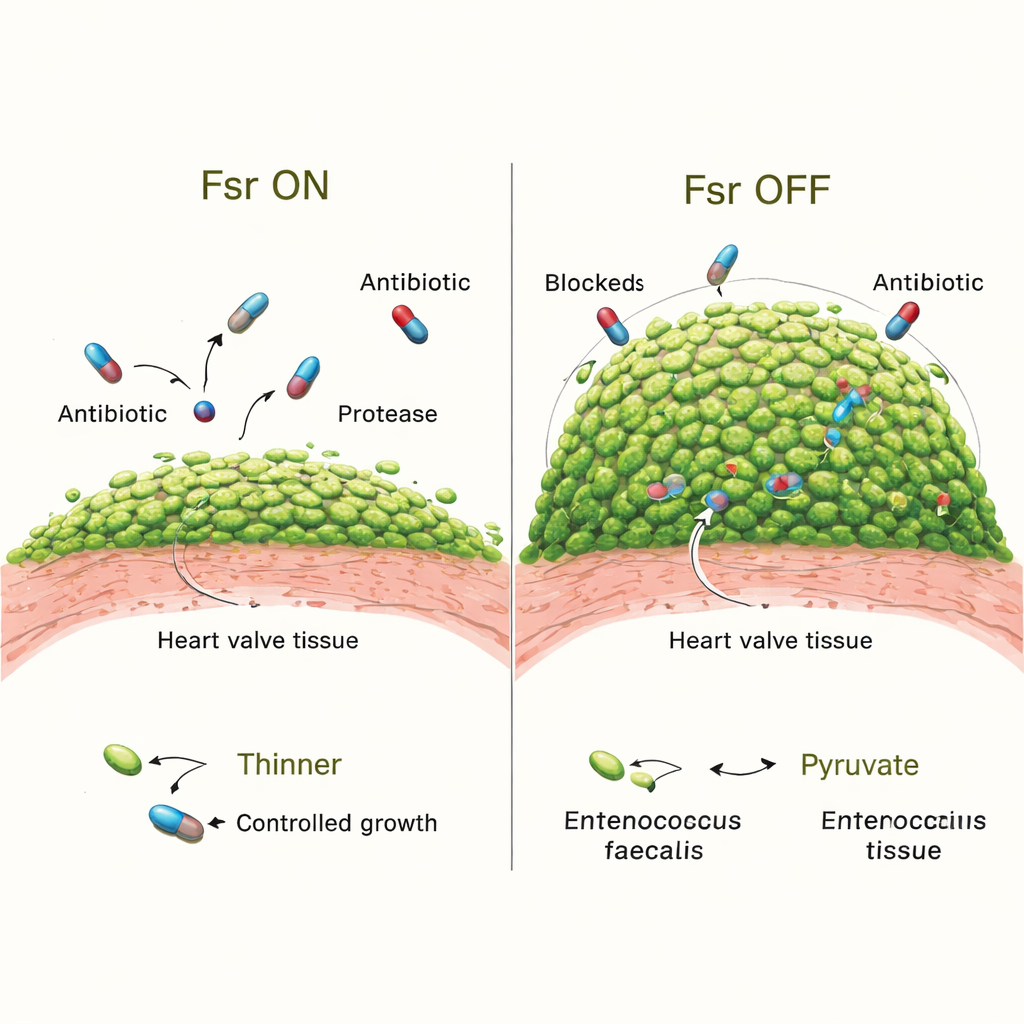
Metabolik yeniden yönlenme ve antibiyotiklere daha sıkı tutunma
Enfekte kapaklardaki bakterilerin gen ifadesi profillemesi, Fsr’nin yalnızca birkaç enzimi kontrol etmekten öte işler yaptığını ortaya koydu. Fsr olmadığında yüzlerce genin aktivitesi değişti; özellikle şeker alımı ve enerji üretimiyle ilgili genlerde belirgin değişimler vardı. lrgA ve lrgB adlı gen çifti öne çıktı: Fsr-eksik bakterilerde şiddetle açılmışlardı ve hücrelerin kanda bulunan enerji açısından zengin küçük bir molekül olan pirüvattan daha iyi yararlanmalarını sağladılar. Araştırmacılar lrgAB’yi Fsr ile birlikte sildiklerinde, aşırı biyofilm büyümesi ortadan kalktı; bu, bu metabolik yolun aşırı büyümeyi destekleyen kilit bir rol oynadığını gösteriyor. Önemli olarak, Fsr-eksik biyofilmler tedaviye de daha dirençliydi. Gentamisin verilen sıçanlarda normal bakteriyle olan enfeksiyonlar küçüldü ve hastalık şiddetinin bir göstergesi olan platelet sayıları düzeldi. Buna karşın Fsr-eksik enfeksiyonlar neredeyse yanıt vermedi, oysa standart laboratuvar testlerinde bakteriler daha fazla ilaç dirençli değildi.
İnsanlara özgü bir iltihaplanma bükümü
Çalışma ayrıca bu bakterilerin insanlarda iltihabı nasıl kışkırtabileceğine dair potansiyel bir yol ortaya koydu. GelE enzimi, bağışıklık sinyali IL-1β’nin insan öncülünü aktif biçime keserek iltihaplanmayı tetikleyebiliyor. İlginçtir, GelE sıçan IL-1β’sini farklı biçimde kesiyor; onu aktive etmek yerine parçalıyordu ve sıçan ve fare proteinlerinde insanlardaki kesin “aktifleştirici” kesim noktası eksikti. Bu tür türlere özgü etki, insanda GelE’nin biyofilmin kenarında iltihabı odaklamaya yardımcı olabileceğini ve endokardit sırasında doku hasarını kötüleştirebileceğini düşündürüyor.
Laboratuvardan klinige: Fsr kaybı hastalar için neden önemli?
Bu deneysel bulguların gerçek hayatta da önem taşıyıp taşımadığını görmek için araştırmacılar İsviçre ve Amerika Birleşik Devletleri’ndeki 81 infektif endokardit hastasından izole edilmiş E. faecalis suşlarını analiz ettiler. Suşların neredeyse yarısı doğal olarak Fsr sisteminden yoksundu. Bu Fsr-negatif suşlarla enfekte hastalarda kanlarında bakteri saptanmaya devam etme süresi daha uzundu—daha fazla gün bakteriyemi vardı—ve yoğun bakım, uzun hastane yatışları, büyük kalp prosedürleri veya ölüm gibi yüksek şiddetli bir kategoriye girme olasılıkları daha yüksekti. Diğer virülans genleri bu deseni açıklayamıyordu; bu da daha agresif hastalığın ana belirteci olarak doğrudan Fsr kaybına işaret ediyor.
Gelecekteki tedaviler için neden önemli?
Bir araya gelen bu bulgular, bakteriyel iletişimin bloke edilmesinin her zaman enfeksiyonları zayıflatacağına dair basit fikri çürütüyor. E. faecalis endokarditinde Fsr sistemi aslında biyofilm genişlemesini sınırlıyor ve bakterileri antibiyotiklere karşı daha savunmasız kılıyor. Fsr eksik olduğunda bakteriler daha yoğun biyofilmler oluşturuyor, kan besinlerinden daha verimli biçimde yararlanıyor ve ısrarcı, uzamış enfeksiyonları körüklüyor. Hastalar açısından bu, Fsr’den yoksun suşların daha zor tedavi edilen hastalığı öngörebileceği ve quorum sensing’i körü körüne kapatan terapilerin bu bağlamda ters etki yapabileceği anlamına geliyor. Bunun yerine pirüvat kullanımına benzer metabolik yolları hedeflemek veya prognostik belirteçler olarak Fsr ve GelE durumunu izlemek, bu tehlikeli kalp enfeksiyonlarını yönetmek için daha iyi yollar sunabilir.
Atıf: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Anahtar kelimeler: infektif endokardit, bakteriyel biyofilmler, quorum sensing, Enterococcus faecalis, antibiyotik toleransı