Clear Sky Science · tr
Yapılandırılmış VPg saRNA, kap-bağımsız, düşük immünojenik ve terapötik proteinlerin hassas kodlanmasını canlıda sağlar
RNA İlaçları için Kuralları Yeniden Yazmak
Mesajcı RNA (mRNA) tabanlı aşılar COVID-19 ile mücadelede dönüm noktası oldu, ancak benzer molekülleri kronik hastalıklarda eksik proteinleri yerine koymak veya tamamlamak için kullanmak çok daha zordur. Vücut yabancı RNA’yı hızla yok etme ve güçlü bağışıklık tepkileri başlatma eğilimindedir ve mevcut birçok kendi kendini çoğaltan RNA tasarımı kendini kopyalarken hatalar yapar. Bu çalışma, insan norovirüsünden alınan parçalarla inşa edilmiş yeni bir kendi kendini çoğaltan RNA türünü tanımlar; bu yapı uzun ömürlü, daha az iltihaplandırıcı ve alışılmadık şekilde hassas olacak şekilde tasarlanmıştır; bu da daha kesin ve dayanıklı RNA ilaçlarının önünü açar.
Daha Akıllı Bir Kendi Kendini Kopyalayan RNA
Geleneksel mRNA ilaçları bir proteinin tek bir “tarifini” taşır ve hücre tarafından bir kez okunup sonra yıkılır. Kendi kendini çoğaltan RNA (saRNA), hücre içinde RNA’nın kendi kendine kopyalanmasını sağlayan ek viral makinelere sahiptir; bu, küçük bir dozdan büyük miktarda üretimi mümkün kılar. En çok çalışılan saRNA sistemleri alfavirüslerden gelir; fakat bunlar hantal, güçlü antiviral savunmaları tetikleyen ve dizilerini nispeten düşük doğrulukla kopyalayan sistemlerdir. Yazarlar bunun yerine sık görülen mide gribi etkeni insan norovirüsüne yöneldiler. Norovirüsün kompakt bir genetik bölümünü izole edip terapötik genleri taşıyacak şekilde yeniden inşa ettiler. Temelinde, RNA’nın ön ucuna kimyasal olarak bağlanmış küçük bir viral protein olan VPg bulunur. VPg, insan mRNA’larında bulunan tipik “kap” yapısının yerini alır ve RNA’nın hücrenin farklı bir çeviri faktörleri seti tarafından çevrilmesine olanak tanır; bu faktörler belirli stres sinyallerine karşı daha az duyarlıdır. 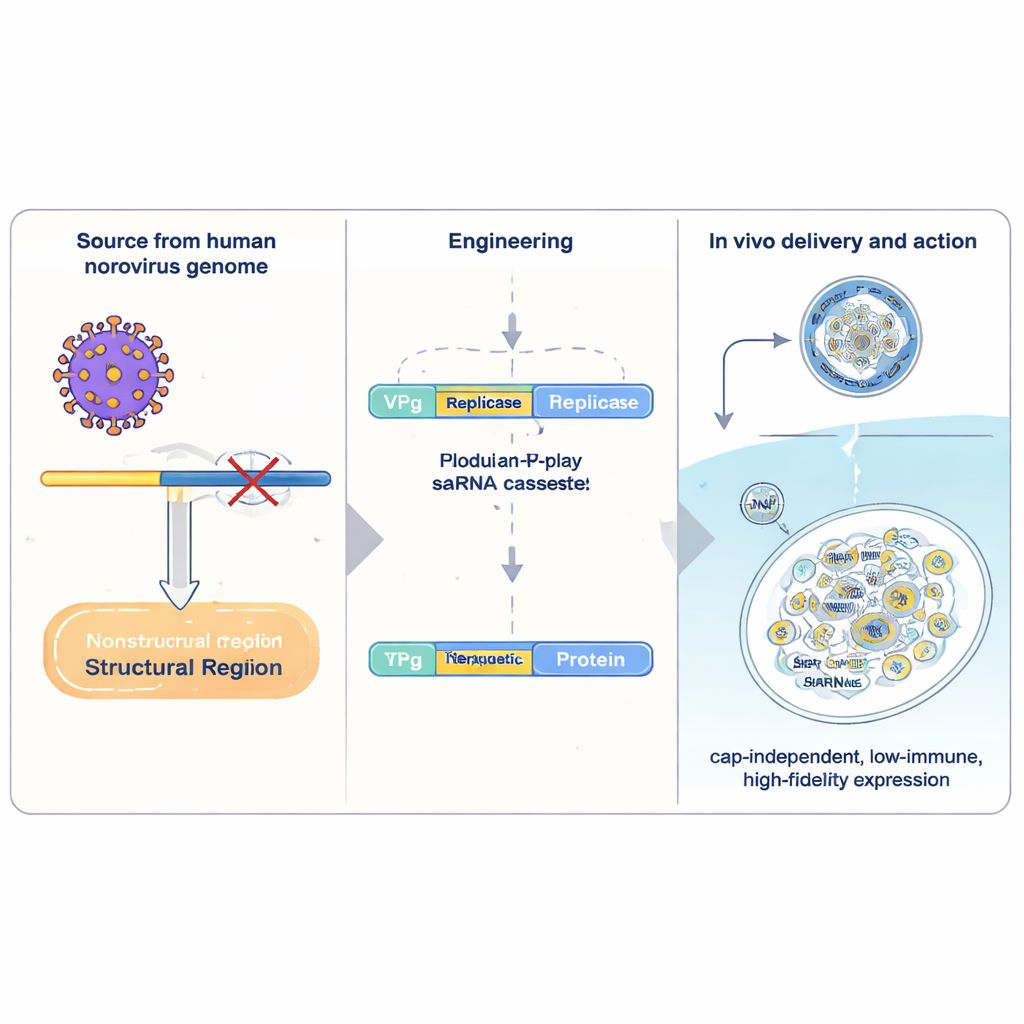
İmmüniteyi Kışkırtmadan Yüksek Doğruluk
Protein terapilerinde doğruluk önemlidir: küçük kopyalama hataları bile bir ilacın davranışını değiştirebilir veya toksik yan ürünler oluşturabilir. Ekip, norovirüs VPg’si virüsün RNA kopyalama enzimi (polimeraz) ile bağlandığında hatalı yapı taşlarının eklenme hızını yavaşlattığını ve böylece hata oranını keskin şekilde azalttığını gösterdi. VPg’de polimerazın ana kontrol bölgesiyle temas eden belirli amino asitleri tanımladılar ve bu arayüz bozulduğunda kopyalamanın daha az doğru hale geldiğini kanıtladılar. Aynı zamanda klasik saRNA tasarımları, antiviral savunmaları etkinleştiren ve protein üretimini kapatan çift sarmaklı RNA’dan (dsRNA) büyük miktarlar oluşturur. Yazarlar, polimerazı belirli bir VPg-bağlı başlangıç formunu tercih edecek şekilde yeniden tasarlayarak ve yalnızca terapötik zincirin verimli şekilde üretilmesini sağlayacak şekilde genomu yeniden düzenleyerek çift sarmaklı RNA oluşumunu büyük ölçüde azalttılar. Ayrıca VPg’nin doğru yere bağlanmasını sağlayacak şekilde RNA’nın bir kuyruk bölgesini ayarlayarak kısa, istem dışı parçacıkların ortaya çıkıp dolaşıya karışabilecek peptidler üretmesini engellediler.
Geleneksel mRNA’nın Başarısız Olduğu Yerlerde Etkili
Yeni VPg tabanlı saRNA, sıradan kaplı mRNA’nın zorlandığı zorlu hastalık ortamlarında test edildi. Kas ve yağ dokularının eridiği bir tükenme sendromu olan kanser ilişkili kakeksiada, standart mRNA kapını tanıyan ana çeviri faktörleri kapatılır; bu durum kap-bağımlı mRNA’ları verimsiz hale getirir. VPg alternatif bir çeviri giriş noktası kullandığı için pankreas kanseri fare modelinde iştah ve metabolizma hormonu ghrelin üretimini sürdürdü. Aylık düşük doz enjeksiyonlar kas ve yağın korunmasına, yiyecek alımının ve metabolizmanın iyileşmesine yardımcı oldu ve belirgin toksisite veya kronik bağışıklık aktivasyonu işaretleri olmadan yaşam süresini ölçülü şekilde uzattı.
Hassas Kanser Saldırısı ve Daha Sakin Otoimmünite
Yüksek doğruluklu kopyalamanın gerçekten önemli olup olmadığını test etmek için araştırmacılar VPg vektörünü, kanser hücresi mitokondrisinde delikler açmak ve tümöre özgü bağışıklık yanıtlarını uyarmak üzere tasarlanmış karmaşık bir onkolitik yapı olan GSDMDENG ile yüklediler. Aynı yapı geleneksel bir alfavirüs saRNA’sına konulduğunda, tekrar eden kopyalama döngülerinde mutasyonlar birikti ve seçici kanser hücresi öldürme ile bağışıklık harekete geçirme fonksiyonlarını zayıflattı. Buna karşılık VPg sistemi amaçlanan diziyi korudu, güçlü tümör hücresi öldürmesi üretti ve pankreas kanseri fare modellerinde tümörleri yavaşlatan veya engelleyen kalıcı T hücre yanıtları tetikledi. Son olarak, VPg saRNA’sini farklı bir zorlukta kullandılar: kemik iliği naklinden sonra bağışıklık hücrelerinin akciğerleri hedef aldığı kronik graft-versus-host hastalığında, aktifleşmiş protein C’yi kodlayan bir VPg saRNA zararlı antikor oluşumunu azalttı, akciğer skarlaşmasını engelledi ve farelerde solunumu iyileştirdi; karşılaştırılabilir bir alfavirüs-temelli yapı ise daha güçlü doğuştan bağışıklık tepkisi provake etti ve sonuçları kötüleştirdi.
Gelecek RNA İlaçları İçin Neden Önemli
Genel olarak bu çalışma, üç arzu edilen özelliği birleştiren kompakt, “tak-çalıştır” bir RNA platformunu özetliyor: kendini doğru şekilde kopyalar, bağışıklık alarmlarını en aza indirecek şekilde tasarlanmıştır ve standart mRNA çevirisini sınırlayan bazı darboğazları aşar. Terapötik gen, sabit bir norovirüs tabanlı iskelete basitçe yerleştirilebildiği için hormonlardan pıhtılaşma düzenleyicilerine ve onkolitik ajanlara kadar birçok farklı protein aynı şasi üzerinde test edilebilir. İnsan kullanımına gelmeden önce yapılması gereken çok iş olsa da, bu VPg saRNA yaklaşımı, düşük dozlu, daha uzun etkili ve sıradan mRNA mesajlarının güvenilir okunamadığı hastalıklı dokularda bile çalışacak şekilde tasarlanmış protein infüzyonlarına daha çok benzeyen RNA ilaçlarına giden bir yol olduğunu öne sürüyor. 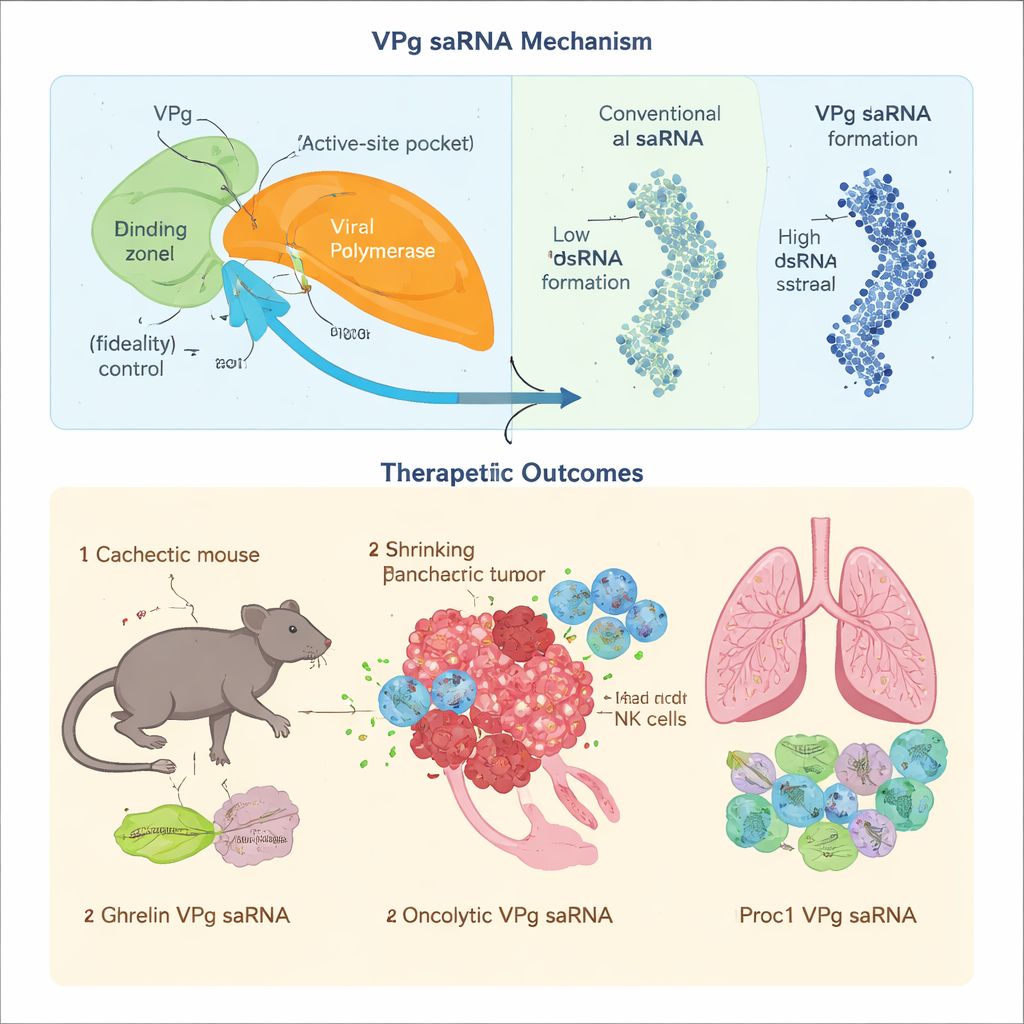
Atıf: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Anahtar kelimeler: kendi kendini çoğaltan RNA, mRNA terapötikleri, norovirüs VPg, kanser kakeksisi, graft-versus-host hastalığı