Clear Sky Science · tr
Düşük karmaşıklıklı tekrarların RNA–RNA etkileşimlerindeki rolü ve dörtlü tahmini için derin öğrenme çerçevesi
Hücre Davranışını Şekillendiren Yapışkan RNA Dizileri
Her hücrenin içinde RNA molekülleri sürekli birbirleriyle çarpışır, genlerin hangilerinin aktif olduğu, proteinlerin nasıl üretildiği ve hücrelerin nasıl geliştiği üzerinde etkili olan geçici ortaklıklar kurarlar. Bu çalışma, birçok RNA–RNA karşılaşmasının rastgele olmadığını gösteriyor: kısa, basit ve yoğun tekrar içeren diziler moleküler cırt cırt gibi iş görerek yönlendiriyor. Araştırmacılar ayrıca böyle RNA çiftlerinin nerede oluşacağını tespit edebilen bir yapay zeka aracı geliştirdiler; bu da sağlıklı ve hastalıklı durumlarda hücre işleyişini keşfetmek için yeni yollar açıyor.
Güçlü Etkilere Sahip Basit Tekrarlar
RNA genellikle DNA’dan proteinlere genetik bilgi taşıyan bir haberci olarak tanımlanır, ancak aynı zamanda bir iskelet, düzenleyici ve rehber görevi de görür. Bu işlevlerin çoğu iki RNA ipliğinin birbirine bağlanmasına dayanır. İnsan ve fare hücrelerinde yapılan birkaç büyük deneysel çalışmanın verilerini birleştirerek, yazarlar gerçek eşleşmelerin gerçekleştiği RNA bölgelerinin düşük karmaşıklıklı tekrarlarla güçlü şekilde zenginleştiğini gösteriyorlar. Bunlar, G ve C bazlarının ardışık tekrarları gibi kısa motiflerden oluşan tekrar edilen diziler. Genomik “çöp” değil, tersine bir RNA’nın birçok başkasıyla bağlanabileceği başlıca bağlanma noktalarıdır ve transkriptom genelinde yoğun etkileşim merkezleri oluştururlar. 
Gelişim ve Düzenleme İçin RNA Merkezleri
Ekip, bu tekrar zengini temas bölgelerine hangi genlerin sahip olduğunu incelediğinde çarpıcı bir desen ortaya çıktı: birçoğu transkripsiyon faktörleri gibi gelişimi ve hücre kimliğini kontrol eden proteinleri kodluyordu. Aktif olarak farklılaşmayan kanser hücre hatlarında bile, gelişim programlarıyla ilişkilendirilen RNA’lar tekrar-temelli temaslarda yoğun olarak yer alıyordu. Yazarlar ayrıca protein kodlamayan ancak sıklıkla düzenleyici olan uzun kodlamayan RNA’lara (lncRNA) da odaklandı. Örneğin, lncRNA TINCR’in hedefleri ile motor nöron oluşumu için önemli başka bir lncRNA olan Lhx1os’un hedefleri, tamamlayıcı tekrarların fazlalığını gösteriyordu. Bu durumlarda, lncRNA üzerindeki basit tekrarlar, partner RNA’larda tamamlayıcı tekrarlarla eşleşerek anahtar gelişim genlerinin seviyelerini veya çevirisini ayarlamaya yardımcı olabilecek stabil eşleşmeler sağlar.
Proteinler ve Düzenleyici Enzimlerin Katkısı
Bu tekrar kaynaklı RNA temasları nadiren tek başına işler. Yazarlar etkileşim verilerine protein bağlanma haritalarını örtüştürdüklerinde, tekrar taşıyan temas bölgelerinin birçoğunun çeviri kontrolü, RNA bozunumu ve P-cisimcikleri ile stres granülleri gibi sitoplazmik granüllerin oluşumunda rol alan RNA-bağlayıcı proteinler tarafından da tanındığını buldular. Özellikle STAU1 adlı bir protein, RNA hedeflerinin yok edilmesini tetikleyebildiğinden, düşük karmaşıklıklı tekrarlar aracılığıyla oluşan dörtlülere sıkça bağlanıyordu. STAU1 bastırıldığında, özellikle tekrar taşıyanlar olmak üzere bu dörtlülere dahil RNA’ların düzeylerinde artış görüldü; bu da tekrar aracılı RNA eşleşmesinin transkriptleri kontrollü degradasyon için işaretleyebileceğini düşündürüyor. Aynı tekrar zengin bölgeler ayrıca ADAR1 gibi RNA düzenleme enzimlerini de çekiyor; bu enzimler çift iplikli RNA içindeki belirli bazları kimyasal olarak değiştirir ve düşük karmaşıklıklı tekrarların düzenleme noktalarını konumlandırmaya yardımcı olabileceğini ima ediyor.
Bir Sinir Ağını RNA Temaslarını Okumaya Öğretmek
Standart bilgisayar programları RNA–RNA bağlanmasını çoğunlukla termodinamik kararlılık temelinde tahmin etmeye çalışır—bir dörtlünün oluşması ya da kırılmasının ne kadar enerji gerektireceği. Faydalı olmasına rağmen, bu modeller hücrelerde gözlemlenen gerçek etkileşimleri, özellikle uzun RNA’lar arasındaki etkileşimleri sıklıkla kaçırır. Basit enerji kurallarının ötesine geçmek için yazarlar, RNA dizilerinden öğrenilen kalıpları kodlayan sayısal gömme (embedding) yöntemlerini kullanan “dil modeli” tarzı gömmelere dayanan RIME adında bir derin öğrenme modeli eğittiler. RIME’ye RNA segment çiftleri gösterildi ve bunların etkileşip etkileşmeyeceğini sınıflandırmayı öğrendi; pozitif örnekler olarak psoralen tabanlı çaprazlama deneylerinden elde edilmiş çok sayıda gerçek eşleşme, negatifler olarak ise dikkatle oluşturulmuş etkileşmeyen çiftler kullanıldı. 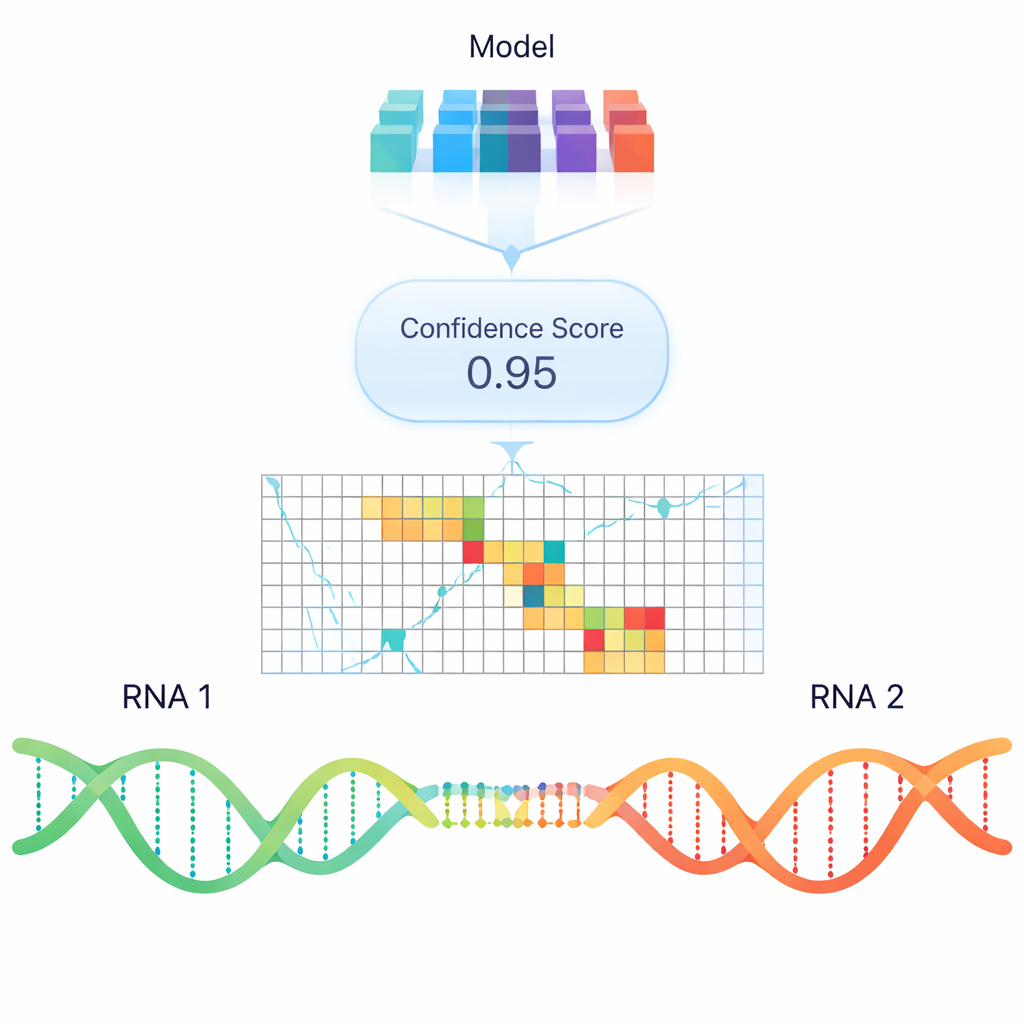
Daha Akıllı Tahminler ve Yeni Biyolojik İpuçları
RIME, önde gelen termodinamik tabanlı araçlar ve başka bir sinir ağı yöntemiyle kıyaslandığında, özellikle yüksek güvenilirlikli deneysel etkileşimler için gerçek RNA–RNA temaslarını sahte eşleşmelerden ayırt etmede tutarlı olarak daha iyi performans gösteriyor. İki RNA’nın eşleşip eşleşmeyeceğini tahmin etmesinin ötesinde, genellikle ilgili bölgeleri de vurguluyor ve doğal olarak düşük karmaşıklıklı tekrarların güçlü bir temas belirleyicisi olduğunu öğreniyor. Dikkate değer biçimde, farklı RNA’lar arasındaki etkileşimler üzerinde eğitilmiş olan aynı model, tek bir RNA molekülü içindeki içsel baz eşleşmelerini tahmin etmede de iyi sonuç veriyor; bu, yapısal deneylerle ve klasik katlanma algoritmalarıyla uyumlu. TINCR, NORAD ve SMaRT gibi kodlamayan düzenleyiciler için RIME bilinen işlevsel etkileşim bölgelerini yeniden keşfediyor ve ek aday bölgeler öneriyor.
Neden Önemli
Halk için temel mesaj şu: Bir zamanlar işe yaramaz gürültü olarak gözardı edilebilen kısa, tekrarlı RNA dizileri hücrenin RNA bağlantı şemasında merkezi bağlantı noktaları olarak işlev görüyor. RNA’ları bir araya getiriyor, düzenleyici proteinleri ve düzenleme enzimlerini davet ediyor ve hücrelerin gelişimini ve strese yanıtını kontrol eden yollar tarafından yoğun biçimde kullanılıyorlar. Yeni RIME modeli, araştırmacılara bu RNA–RNA ortaklıklarını taramak için güçlü bir araç sunuyor; özellikle tekrar genişlemeleriyle ilişkili nörolojik ve diğer hastalıklarda yanlış gidebilecek etkileşimleri bulma açısından. Özetle, basit RNA tekrarlarının nasıl birbirine yapıştığını anlamak ve tahmin etmek, gen düzenlemesinin gizli katmanlarını ortaya çıkarabilir.
Atıf: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Anahtar kelimeler: RNA–RNA etkileşimleri, düşük karmaşıklıklı tekrarlar, uzun kodlamayan RNA, derin öğrenme, gen düzenlemesi