Clear Sky Science · tr
Transkriptom imzası yönlendirmeli ara alveoler epitel hücrelerinin tükenmesi farelerde pulmoner fibrozisi hafifletir
Neden yara izi oluşmuş akciğerler önemli?
Pulmoner fibroz, ince hava keseciklerinin zamanla sert yara dokusuna dönüşerek her nefesi zorlaştırdığı ciddi bir akciğer hastalığıdır. Hekimler bu skarlaşmanın normal onarım süreçleri yolundan çıktığında başladığını biliyor, ancak hangi özel hücrelerin suçlu olduğu ve sağlıklı akciğer dokusuna zarar vermeden bunların nasıl ortadan kaldırılacağı belirsizdi. Bu çalışma akciğer hücrelerinin içindeki moleküler mesajları “okumanın”, zararlı geçişsel hücreleri tanımlamanın ve farelerde skarlaşmayı azaltmak için bunları seçici olarak elimine etmenin yeni bir yolunu araştırıyor.
Hatalı onarımın gerçekleştiği an yakalanan hücreler
Akciğer hasarından sonra, surfaktan üreten özel tip II hücreler normalde çoğalır ve ardından hava keseciklerini kaplayan ve oksijenin kana geçmesini sağlayan ince tip I hücrelere olgunlaşır. Fibrozda, bu hücrelerin birçoğu yolculuğu tamamlamak yerine ara, yani geçişsel bir durumda takılır. Önceki tek hücre RNA dizileme çalışmaları bu ara hücreleri farelerde ve insanlarda bulmuştu, ancak bunların sadece pasif gözlemciler mi yoksa hastalığın ana sürücüleri mi olduğu net değildi. Yazarlar, farelerde Krt8+ alveoler farklılaşma ara formları olarak adlandırılan geçişsel bir hücre tipine ve yaralaşmış akciğerlerde yüksek sayıda görülen insan muadilleri olan anormal bazaloid hücrelere odaklandı.
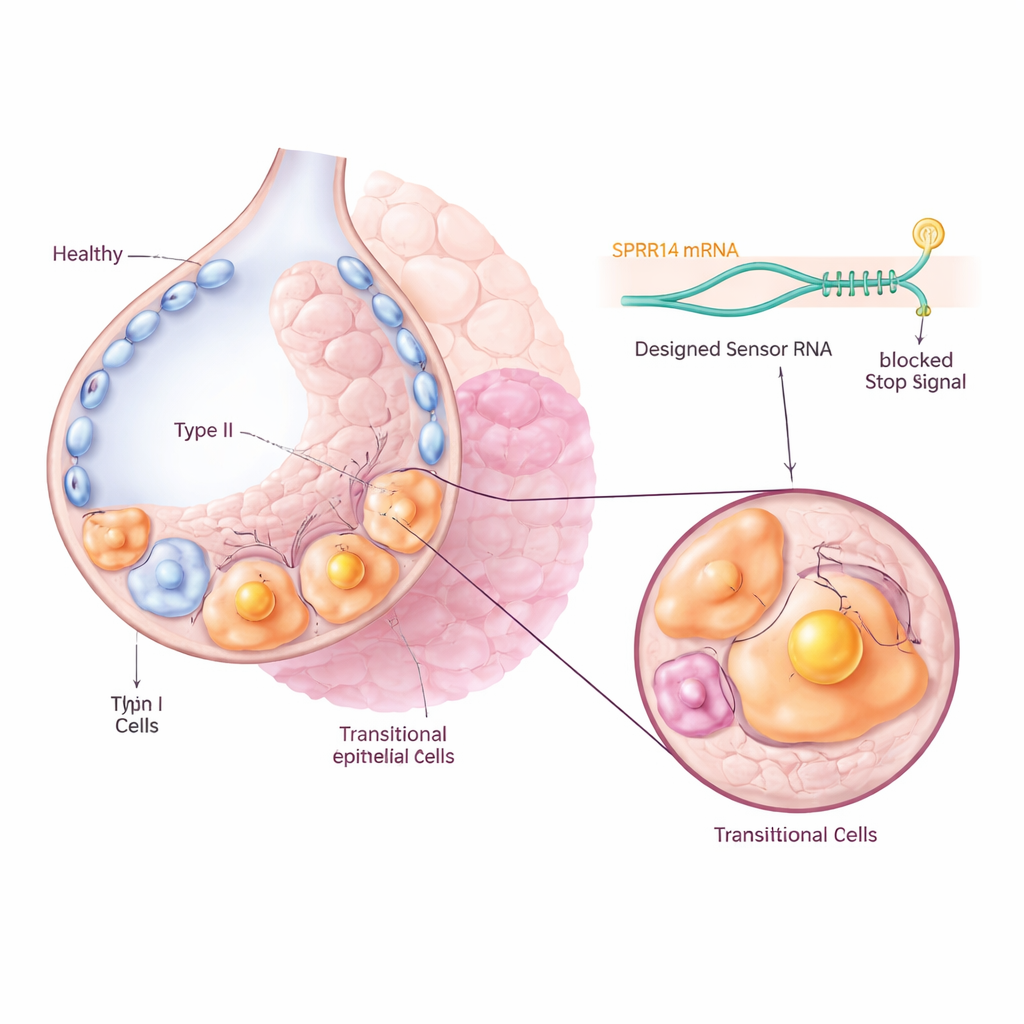
Eşsiz bir moleküler isim etiketi bulmak
Sorunlu hücreleri sağlıklı komşularına dokunmadan hedeflemek için ekip önce büyük gen ifade veri kümelerinde geçişsel popülasyonda güçlü ve özgün olarak açık olan bir belirteç aradı. SPRR1A adlı bir molekülü öne çıkan bir “isim etiketi” olarak tanımladılar: fibrotik fare akciğerlerindeki Krt8+ ara hücrelerde ve idiyopatik pulmoner fibrozlu hastalardan alınan KRT5-/KRT17+ anormal bazaloid hücrelerde yüksek düzeyde zenginleşmiş, ancak normal akciğer hücrelerinde büyük ölçüde yoktu. Fare ve insan akciğer dokusunun mikroskopik görüntülenmesi, SPRR1A'nın esas olarak hasarlı, yeniden modellenmiş bölgelerde ortaya çıktığını ve sağlıklı hava keseciklerinde bulunmadığını doğruladı; bu da onun suçlu hücreleri tanımlamak için hassas bir tutamaç olabileceğini gösterdi.
Hücreleri bir RNA sensörüyle programlamak
Araştırmacılar daha sonra hücre içi moleküler bir sensör gibi davranan yakın zamanda geliştirilmiş CellREADR adlı teknolojiyi kullandılar. SPRR1A RNA'sıyla eşleşebilen kısa RNA dizileri tasarladılar. Sensör SPRR1A'yı algıladığında, ekli bir “efektör” proteinin — bir floresan işaretçi veya hücreyi bir ilaca duyarlı kılan bir reseptör gibi — üretilmesini tetikliyor. Farelerde bu sensör–efektör yapıları virüsler aracılığıyla akciğer hücrelerine verildi. Sadece aktif olarak SPRR1A üreten hücreler floresan sinyali açtı ve ekip geçişsel hücreleri fibrotik akciğerlerden doğrudan izleyip izole edebildi. Tek hücre dizilemesi, etiketlenen hücrelerin bilinen geçişsel gen imzasıyla yakından eşleştiğini göstererek RNA sensörünün hedef popülasyona doğru şekilde yöneldiğini doğruladı.
Zararlı ara formları kapatmak
Daha sonra efektör zararsız bir floresan proteinden difteri toksin reseptörüne dönüştürüldü, böylece SPRR1A-pozitif hücreler difteri toksini verilerek seçici olarak öldürülebiliyordu. Kimyasal akciğer hasarından sonra geçişsel hücrelerin en yüksek bolluğuna denk gelecek şekilde tedavi zamanlandırıldığında, yazarlar bu popülasyonun yaklaşık üçte birini ortadan kaldırabildi. Bu hedefe yönelik tükenme çarpıcı şekilde daha az akciğer skarlaşması ile sonuçlandı: kollajen birikimi azaldı, fibrotik protein düzeyleri düştü ve hava keseciği yapıları daha normal göründü. Ayrıntılı analizler, çoğu SPRR1A-pozitif hücrenin stresli, yaşlanma benzeri bir durumun işaretlerini taşıdığını, küçük bir alt kümenin ise yüksek proliferasyon kapasitesine sahip olduğunu gösterdi; bu da bu ara hücrelerin hem dokuyu düzgün onaramadığı hem de fibrotik süreci sürdüğüne işaret ediyor.
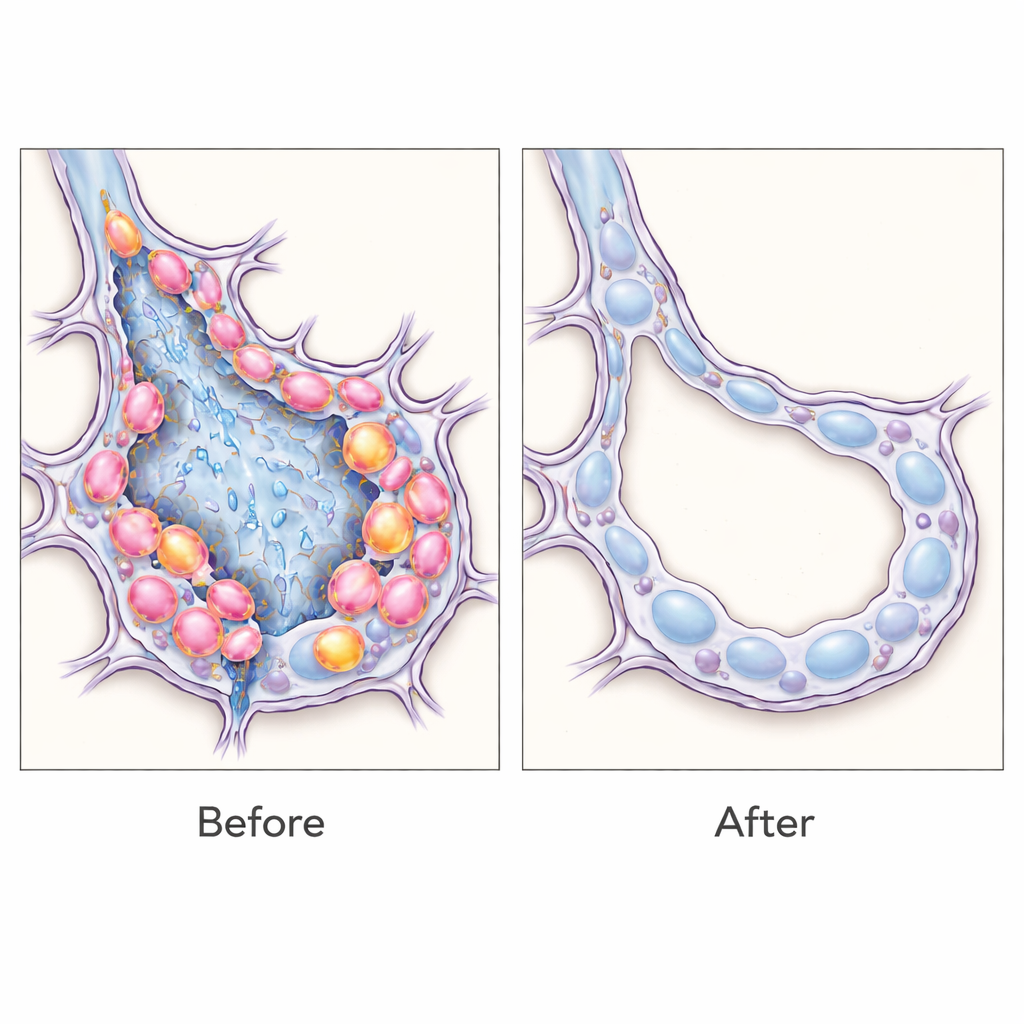
Gelecek tedaviler için bunun anlamı
Bu bulgular, geçişsel epitel hücrelerinin sadece belirteçler olmadığını, pulmoner fibrozun aktif sürücüleri olduklarını ve bunları seçici olarak ortadan kaldırmanın farelerde daha sağlıklı akciğer mimarisine doğru dengeyi kaydırabileceğini savunuyor. Daha geniş anlamda, çalışma esnek bir stratejiyi gösteriyor: hücreye özgü RNA imzalarını “okuyarak”, araştırmacılar canlı dokuda dar tanımlı hücre popülasyonlarını etiketleyebilir, inceleyebilir ve hatta her seferinde özel hayvan hattı oluşturmaya ihtiyaç duymadan ortadan kaldırabilir. Bu RNA algılayıcı araçların insanlar için güvenli bir şekilde uyarlanmasından önce yapılması gereken çok iş olsa da, bu yaklaşım kronik akciğer skarlaşmasında iyileşmeyi rayından çıkaran tam olarak hangi hücre tiplerinin hedefleneceğine yönelik kesin tedavilere giden bir yol açıyor ve potansiyel olarak diğer fibrotik hastalıklar için de uygulanabilir.
Atıf: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Anahtar kelimeler: pulmoner fibroz, alveoler epitel hücreleri, tek hücre RNA dizilemesi, RNA algılama teknolojisi, hücresel senesans