Clear Sky Science · tr
Merkezi amigdala tek-nükleus atlası, insan alkol kullanım bozukluğunda kromatin ve gen transkripsiyon dinamiklerini ortaya koyuyor
Bu araştırma gündelik yaşam için neden önemli
Alkol kullanım bozukluğu (AKB) milyonlarca insanı ve onların ailelerini etkiliyor, ancak uzun süreli ağır içmenin insan beyninde tek tek hücre düzeyinde ne yaptığı hakkında hâlâ şaşırtıcı derecede az şey biliyoruz. Bu çalışma, korku, stres ve motivasyonun bir merkezi olan küçük ama kritik bir bölge — merkezi amigdala — üzerinde yakın plan yaparak alkolün beyin hücrelerini ve onların genetik kontrol sistemlerini nasıl yeniden şekillendirdiğini haritalıyor. Önde gelen "tek hücre" dizileme yöntemlerini bağımlılık riskine ilişkin genetik çalışmalarla eşleştirerek, yazarlar neden bazı insanların AKB’ye daha savunmasız olduğunu ve alkolün beyinde nasıl kalıcı moleküler izler bıraktığını açıklamaya başlıyorlar.
Çok küçük bir beyin merkezine yakından bakmak
Merkezi amigdala, beynin duygu ve stres ağında önemli bir çıkış istasyonu olup anksiyete azalması, isteksizlik ve zorlayıcı alkol kullanım ile güçlü şekilde ilişkilidir. Bu çalışmada araştırmacılar, otopsi sonrası merkezi amigdalanın yaklaşık 175.000 bireysel hücre çekirdeğini 50 kişiden — 22’si alkol kullanım bozukluğu öyküsüne sahip ve 28’i AKB olmayan — analiz ettiler. Aynı hücrede hem gen aktivitesini (RNA) hem de kromatin erişilebilirliğini (DNA’nın ne kadar "açık" veya "kapalı" olduğu) okuyan bir teknoloji kullanarak bu bölgedeki tüm ana beyin hücre tiplerinin ayrıntılı bir atlasını oluşturdular; buna çeşitli nöron türleri ve astrositler ile mikroglia gibi destek hücreleri de dahil. İnhibitör nöronların — beyin aktivitesini azaltan veya şekillendiren hücreler — merkezi amigdala içinde özellikle bol olduğu ve AKB’li kişilerde belirgin şekilde etkilendiği görüldü. 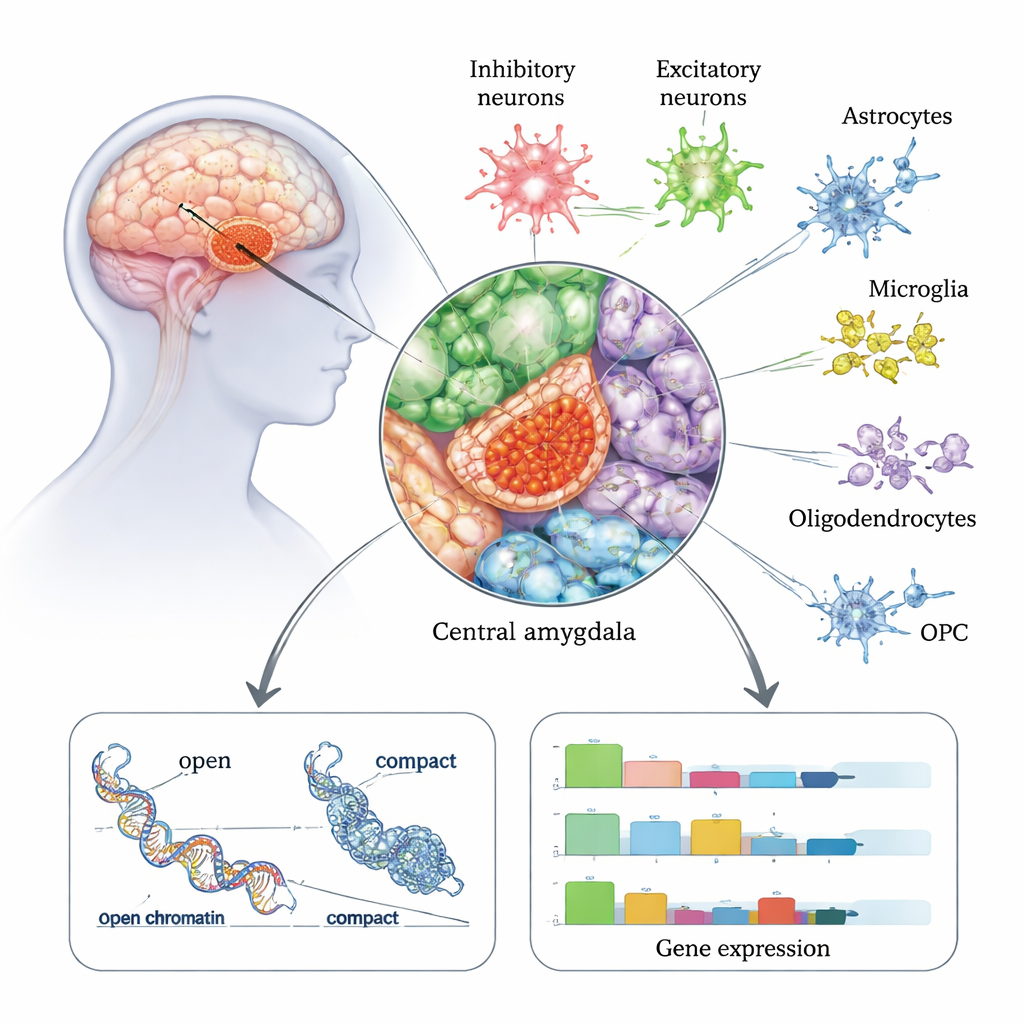
Alkol kullanım bozukluğunda hangi hücreler ve genler değişiyor?
Araştırma ekibi, AKB’li ve AKB’siz kişilerde gen aktivitesini hücre tipine göre sistematik olarak karşılaştırdı. Spesifik hücre popülasyonlarında aktivitesi değişen 1.800’den fazla gen keşfettiler; en büyük değişimler inhibitör nöronlarda, ardından eksitatör nöronlar ve astrositlerde görüldü. Proenkefalin (PENK) peptidini işaretleyen bir inhibitör nöron alt tipi özellikle güçlü değişimler gösterdi. Etkilenen genlerin birçoğu beyin hücreleri arasındaki iletişimde, özellikle eksitatör sinyal glutamat ile inhibitör sinyal GABA arasındaki dengede rol oynuyordu. Örneğin GABA reseptörünün önemli bir alt birimini oluşturmaya yardımcı olan GABRA2 bazı inhibitör nöronlarda artmışken, bir glutamat reseptörü olan GRM8 ve sinapslar için önemli bir hücre-adezyon molekülü olan NCAM1 nöron alt tipleri arasında zıt yönlerde değişti. Bu desenler, merkezi amigdalada uyarılma ve baskılanmanın ince ayarının AKB’de bozulduğunu gösteriyor.
Beynin kontrol anahtarları: kromatin ve düzenleyici elemanlar
Genler tek başına hareket etmez; anahtarlar ve dimmerler gibi işlev gören DNA kesimleri tarafından kontrol edilirler. Kromatini — DNA’nın nasıl paketlendiğini — inceleyerek araştırmacılar yarım milyondan fazla aday düzenleyici eleman tespit etti ve bunları hücre tipine özgü biçimde yakınlardaki genlere bağladılar. Bu elemanların neredeyse yarısı tek bir hücre tipine özgüydü, bu da farklı beyin hücrelerinin ne kadar uzmanlaştığını vurguluyor. AKB’de değişen birçok düzenleyici eleman, CALN1 gibi kalsiyum işlenmesi ve glutamat sinyaliyle ilişkili genlere bağlıydı; CALN1 nöronlarda güçlü şekilde aktif olan bir kalsiyum bağlayıcı gendir. İnhibitör nöronlarda CALN1 hem artmış ifade hem de yoğun düzenleyici döngü kümeleri gösterdi; bu, alkol maruziyetinin bu geni kontrol eden yerel DNA mimarisini yeniden şekillendirdiğini ima ediyor. 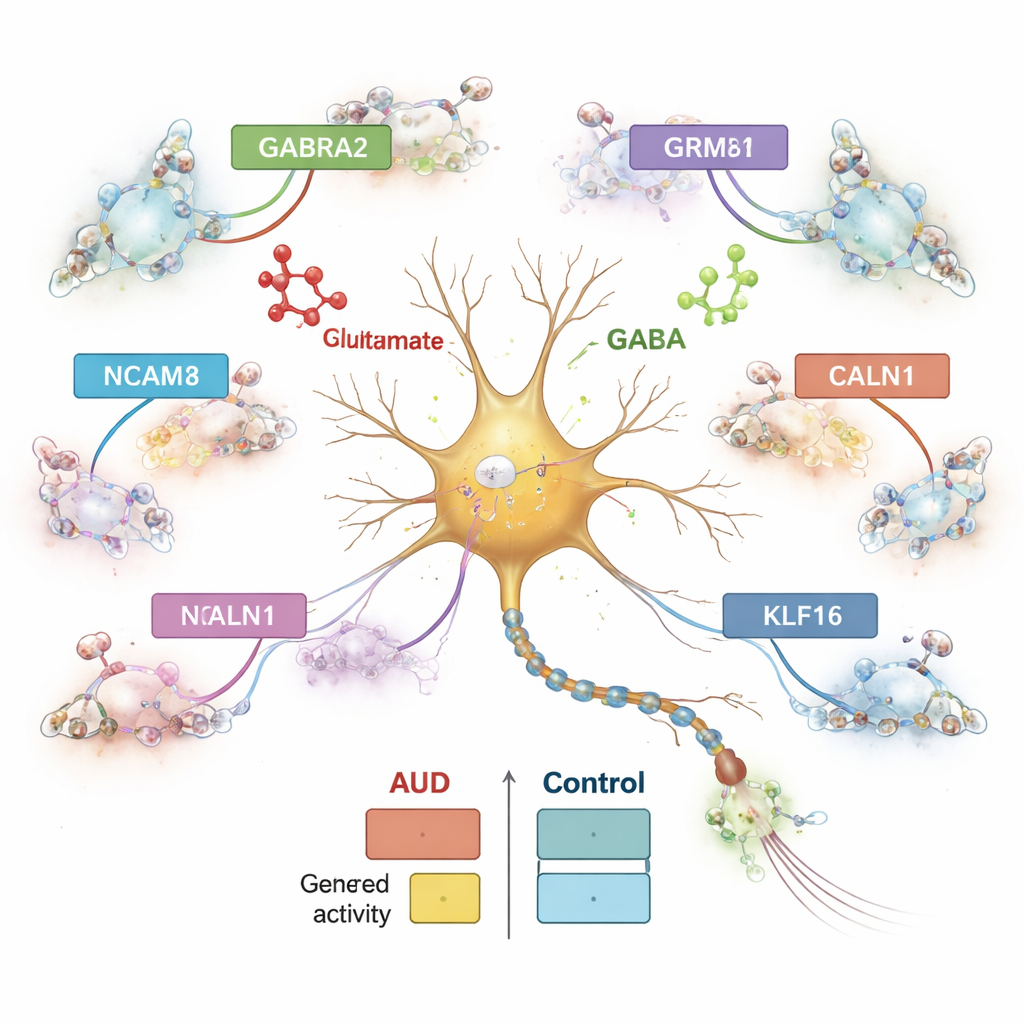
Risk genlerinden gerçek beyin değişikliklerine
Genetik çalışmalar, alkol sorunları geliştirme riskini artıran birçok DNA varyantı tanımladı, ancak bunların beyinde nerede ve nasıl etki ettiği belirsizdi. Tek hücre haritalarını geniş ölçekli genom çapı ilişki çalışmalarının (GWAS) sonuçlarıyla örtüştürerek yazarlar, risk genlerinin merkezi amigdala nöronlarında — özellikle inhibitör nöronlarda — orantısız şekilde aktif ve düzensiz olduğunu buldular. Belirli hücre tiplerinde açık olan düzenleyici elemanların içinde yer alan 200’den fazla olası nedensel risk varyantını saptadılar. Bazıları CACNA1C ve DRD2 gibi daha önce bağımlılıkla ilişkilendirilmiş genlerin içinde veya yakınındaydı; bu genler nöronal uyarılabilirlik ve dopamin sinyallemesini kontrol etmeye yardımcı olur. Diğerleri SEMA6D ve NF1 gibi yeni adaylar olarak ortaya çıktı. Ekip ayrıca Kruppel-benzeri faktörler ailesinden (özellikle KLF16) transkripsiyon faktörlerini tanımladı; bunlar kalsiyum ve glutamatla ilişkili genlerde geniş çaplı değişiklikleri koordine ediyor gibi görünüyor ve bu düzenleyici ağın parçalarını akut alkol maruziyeti olan bir fare modelinde doğruladılar.
AKB’yi anlamak ve tedavi etmek için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma alkol kullanım bozukluğunun sadece yaygın bir beyin sorunu olmadığını, aynı zamanda kritik bir duygusal merkez içinde belirli hücre tiplerine ve moleküler yolaklara odaklanmış, yüksek derecede organize olmuş bir bozulma olduğunu gösteriyor. Merkezi amigdalanın inhibitör nöronları ile astrositler ve diğer destek hücreleri, özellikle glutamat, GABA ve kalsiyum sinyallerini yöneten sistemlerde gen aktivitesi ve bu genleri kontrol eden DNA anahtarlarında eşgüdümlü değişiklikler gösteriyor. Bu hücresel değişiklikleri genetik risk varyantlarıyla ilişkilendirerek çalışma, kalıtsal hassasiyeti beyindeki somut moleküler olaylara bağlayan bir yol haritası sunuyor. Zamanla, bu tür hücreye özgü haritalar uyarılma ve baskılama dengesini geri kazandırmaya yönelik, bütünüyle beyne geniş etki yapan yaklaşımlar yerine daha hassas tedavilerin geliştirilmesine rehberlik edebilir.
Atıf: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Anahtar kelimeler: alkol kullanım bozukluğu, merkezi amigdala, tek hücre genomikleri, inhibitör nöronlar, gen düzenlemesi