Clear Sky Science · tr
TDP-43/RNA kompleks oluşumundan yapı ve hücresel yaklaşımla hastalıkla ilişkili TDP-43 agregasyonuna
Bu beyin proteini neden önemli
Amiyotrofik lateral skleroz (ALS) ve frontotemporal demans gibi nörodejeneratif hastalıklarda genellikle sinir hücreleri içinde yanlış katlanmış protein kümeleri görülür. En sık suçlulardan biri, normalde RNA’yı—genlerimizin çalışan kopyasını—işleyen TDP-43 adlı proteindir. Bu çalışma kritik bir soruyu ele alıyor: TDP-43 sağlıklı hücrelerde ne yapar ve yararlı bir RNA yardımcısını toksik, agregat oluşturan bir proteine dönüştüren ne olur?
TDP-43 sağlıklı sinir hücrelerinde nasıl çalışır
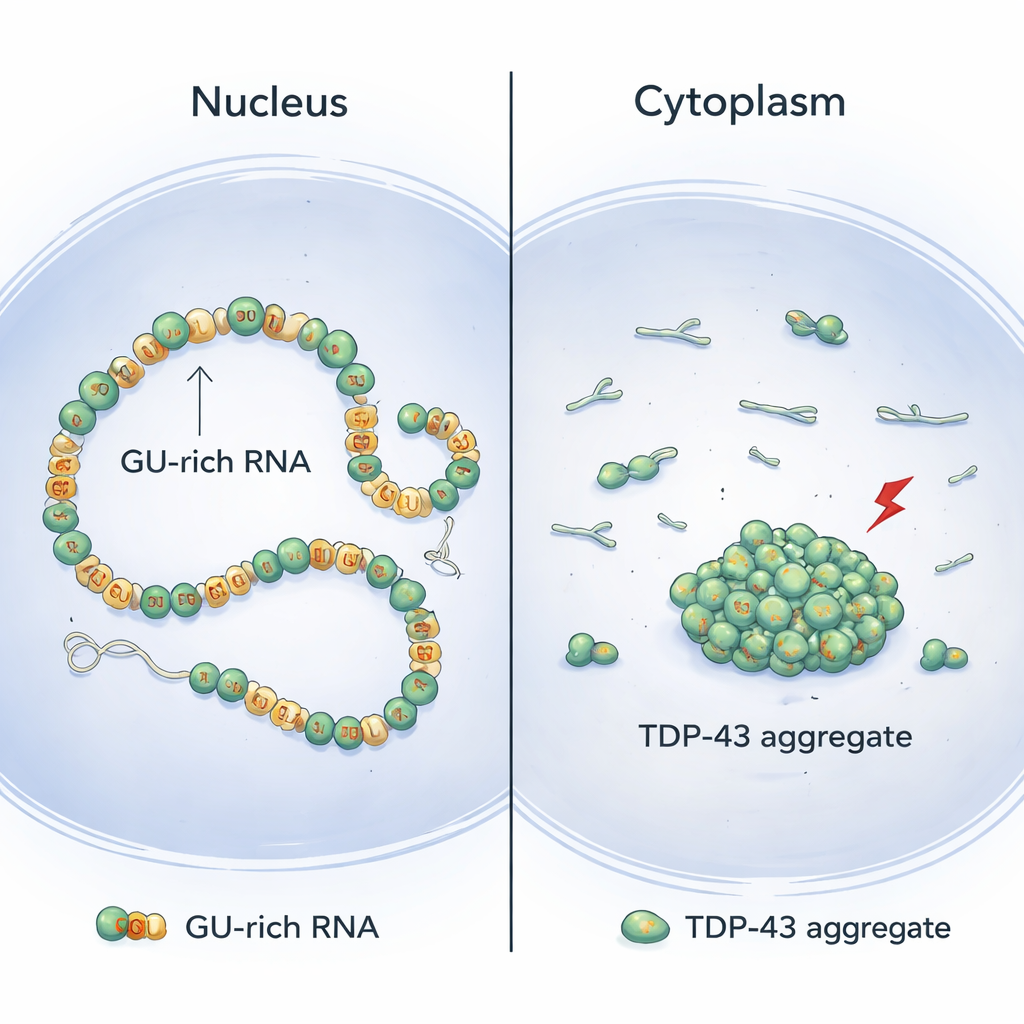
TDP-43 genellikle hücre çekirdeğinde bulunur ve tekrarlayan “GU” yapı taşları bakımından zengin uzun RNA dizilerine bağlanır. Yapısal biyoloji ve hücre deneylerini birleştiren çalışma, TDP-43 moleküllerinin bu GU-zengin bölgeler boyunca işbirlikçi şekilde sıralandığını, RNA üzerinde düzgün, sürekli zincirler oluşturduğunu gösteriyor. Bu düzen içinde proteinin ön ucu—N-terminal bölgesi—komşu moleküller arasında fiziksel olarak ayrılmış kalır. Sonuç olarak, bu N-terminal segmentler aynı RNA’nın uzak GU-zengin bölümlerine uzanıp onları birbirine bağlayacak şekilde kullanılabilir durumda olur; uzun intronları (gen içindeki kodlamayan bölgeler) topolojik olarak hafifçe döndürüp sıkıştırır, ancak kümeleşmeye yol açmaz.
Proteinin içinde yerleşik bir çekişme
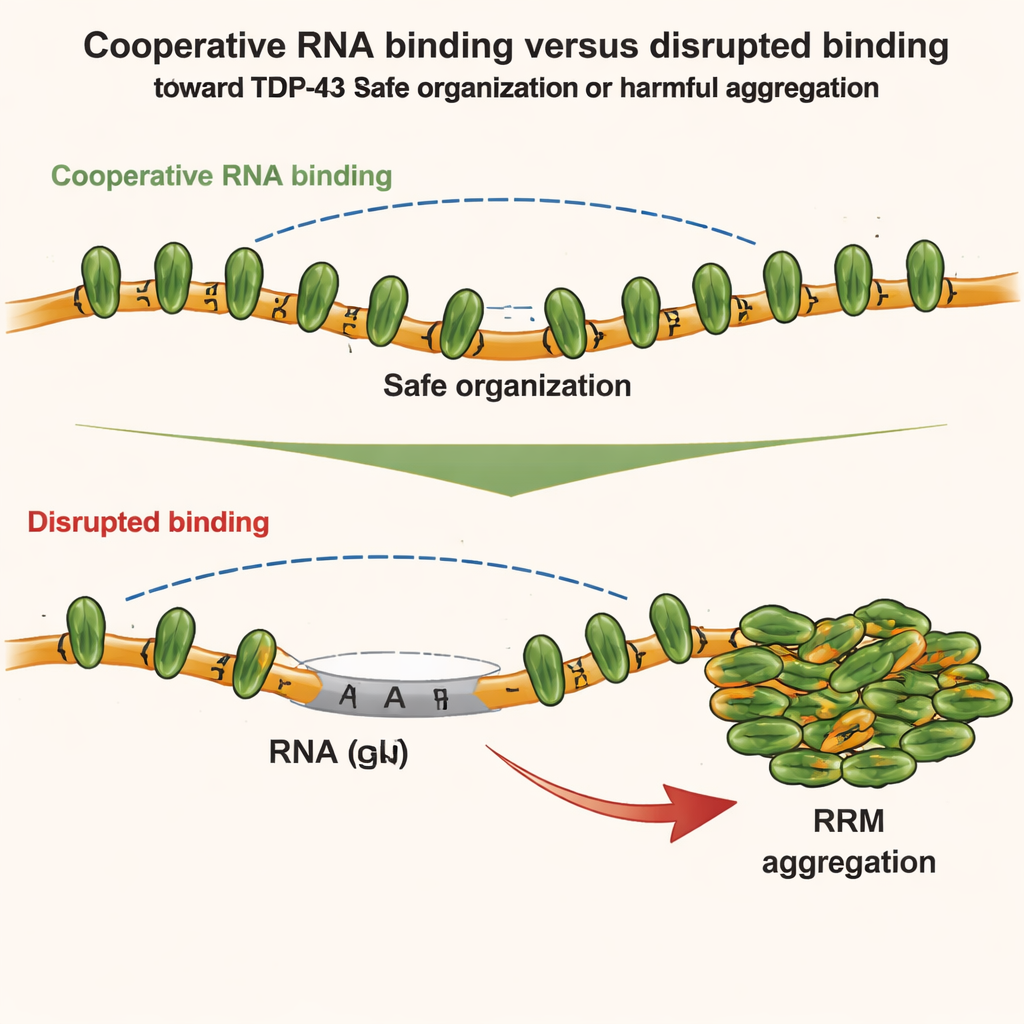
Grup daha sonra TDP-43’ün farklı parçalarının nasıl yarıştığını veya işbirliği yaptığını inceledi. Odaklandıkları iki bölge vardı: birbirine yapışabilen N-terminal domain ve GU-zengin RNA boyunca işbirlikçi bağlanmayı yönlendiren merkezi RNA-bağlayıcı modüller. NMR spektroskopisi, kalorimetri ve küçük açılı X-ışını saçılması gibi hassas tekniklerle, TDP-43 RNA’ya işbirlikçi bağlandığında zincirin geometrisinin aslında bitişik moleküller arasındaki doğrudan N-terminal–N-terminal temaslarını zayıflattığını buldular. Başka bir deyişle, güçlü işbirlikçi RNA bağlanması yerel N-terminal etkileşimlerini kontrol altında tutar. Ancak bu işbirliği bozulduğunda—örneğin RNA’ya GU olmayan diziler eklendiğinde veya TDP-43 mutasyona uğradığında—komşu proteinlerin N-terminal bölgeleri birbirine yaklaşır ve şimdi birbirlerine tutunabilir hale gelir.
Yararlı sıkıştırmadan zararlı kümelenmeye
Bu yapısal bulgular canlı hücrelerde test edildi. Yazarlar farklı TDP-43 mutantlarının yapay RNA-zengin bölmeler içinde nasıl karıştığını veya ayrıştığını izlemek için tasarlanmış hücre sistemleri kullandılar. Hem işbirlikçi RNA bağlanmasının hem de N-terminal etkileşimlerin TDP-43’ü daha yüksek mertebeden yapılara organize etmeye yardımcı olduğunu, ancak farklı yollarla yaptıklarını buldular. İşbirlikçi bağlanma proteinleri GU-zengin RNA boyunca sıraya dizerken, N-terminal temasları uzak kümeleri birbirine bağlar. Ancak hafif oksidatif stres altında tablo değişir. Bir kimyasal stresör (arsenik) merkezi RNA-bağlayıcı motiflerde spesifik kimyasal değişiklikler—asetilasyon—yaparak bunların birbirine yapışmaya yatkın olmasına neden olur. Eğer RNA’ya işbirlikçi bağlanma sağlam kalırsa TDP-43 büyük ölçüde çözünebilir kalır. İşbirliği zayıflarsa, bitişik TDP-43 molekülleri arasındaki N-terminal bağlantılar asetilasyonlu çekirdekleri bir araya getiren bir iskelet gibi davranır ve geri döndürülemez agregasyonu teşvik eder.
TDP-43’ün sitoplazmada neden daha çok kümelendiği
Bu çalışmadan ortaya çıkan model, neden TDP-43 agregatlarının hastalıklı nöronlarda sıklıkla çekirdek yerine sitoplazmada bulunduğunu açıklamaya yardımcı oluyor. Çekirdekte uzun intronlar ve çok sayıda GU tekrarı yaygındır; bu, sürekli, işbirlikçi bağlanmayı teşvik eder, komşular arasındaki riskli N-terminal temaslarını düşük tutar ve bunun yerine güvenli uzun menzilli döngülemeye izin verir. Buna karşılık sitoplazmada olgun RNA’larda çok daha az GU-zengin dizi vardır. Bu durum TDP-43 bağlanmasını yamalı ve daha az işbirlikçi hale getirir; komşu N-terminal domainlerin etkileşme olasılığını artırır ve stres kaynaklı kimyasal değişiklikler ortaya çıktığında agregasyon için zemin hazırlar. Bu görüşü destekleyici olarak, çekirdeğe yapay olarak ekstra GU-zengin intron sağlanması stres altında TDP-43 agregasyonunu azalttı.
Gelecekteki tedaviler için ne anlama geliyor
Basitçe söylemek gerekirse, çalışma TDP-43’ü yararlı RNA organizasyonu ile zararlı kümelenme arasında dengede duran bir protein olarak resmediyor ve GU-zengin RNA’ya işbirlikçi bağlanma bunu bir güvenlik mekanizması olarak işlevlendiriyor. Bu güvenlik ağı çöktüğünde—RNA dizilerinin değişmesi, protein mutasyonları veya hücresel stres nedeniyle—normalde uzun RNA segmentlerini sıkıştıran aynı bölgeler toksik agregatların oluşumunu tetikleyebilir. Uzman olmayanlar için çıkarılacak başlıca sonuç, TDP-43 ile RNA arasındaki doğru türde etkileşimlerin korunmasının ALS ve ilgili beyin hastalıklarında görülen protein kümelenmesini önlemek veya yavaşlatmak için ümit verici bir strateji olabileceğidir.
Atıf: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Anahtar kelimeler: TDP-43 agregasyonu, RNA-bağlayıcı proteinler, ALS, protein–RNA etkileşimleri, nörodejenerasyon