Clear Sky Science · tr
DOT1L aktivitesi transkripsiyon uzama hızını sınırlar ve AID tarafından yaratılan mutagenezi kolaylaştırmak için RNAPII duraklamasını destekler
Bağışıklık hücrelerimiz riskli DNA değişikliklerini nasıl ince ayarlar
Bağışıklık sistemimiz, zaman zaman kansere zemin hazırlayabilen riskli bir strateji olarak, güçlü antikorlar oluşturmak için kendi DNA’sını bilerek değiştirir. Bu çalışma, nerede ve ne kadar verimli biçimde bu amaçlı mutasyonların oluştuğunu kontrol eden şeyi soruyor — basit görünen ama büyük sonuçları olan bir soru. Cevap, B hücrelerinde gen okuma hızını ayarlayan ve böylece mutasyon makinesini doğru noktalara yönlendirmeye yardımcı olan DOT1L adlı bir proteinin etrafında toplanıyor.
Antikorları keskinleştirmek için mutasyonu açmak
B hücreleri bir enfeksiyonla karşılaştığında, antikorlarını iki yolla geliştirir: bağlanma bölgesinde küçük değişiklikler yaparak mikroba daha sıkı bağlanmayı iyileştirir ve antikorun kuyruk kısmını değiştirerek bağışıklık yanıtının şeklini değiştirir. Her iki yükseltme de, aktif olarak okunan genlerde DNA’yı kesen ve değiştiren AID adlı bir enzimle başlar. AID iyi bir bağışıklık için kritik olsa da, başka genleri de hedefleyebilir ve kanser oluşturan tehlikeli kırılmalara yol açabilir. Önceki çalışmalar, AID’in yoğun okunan ve süper-aktif düzenleyicilerle kontrol edilen genleri tercih ettiğini göstermişti, ancak bu, neden yalnızca belirli bir alt kümenin gerçekten savunmasız olduğunu tam olarak açıklamıyordu.
AID’e duyarlı genleri işaretleyen bir kromatin belirteci
Yazarlar, çekirdekte AID’e yakın duran proteinlere odaklandılar. İnsan hücrelerinde bir yakınlık-etiketleme tekniği kullanarak, AID’in DOT1L yakınında kümelendiğini buldular; DOT1L DNA’nın etrafına sarılı histon proteinlerinin belirli bir noktasını süsleyen bir enzimdir. Bu süsleme, histon H3’ün K79 pozisyonunda kimyasal bir işaret olup aktif genlerde yaygındır. Fare B hücrelerinde, AID’in sıkça mutasyon yaptığı genler — antikor genleri ve kanserle ilişkili hedef dışı genler dahil — özellikle yüksek düzeyde bu DOT1L kaynaklı işaretleri taşıyordu. Araştırmacılar DOT1L’i B hücre hatlarında devre dışı bıraktıklarında veya bir ilaçla aktivitesini engellediklerinde, antikor “sınıf değiştirmesi” azaldı; AID kaynaklı DNA kırılmaları ve antikor genleri ile büyüme geni cMyc arasındaki kanser eğilimli füzyonlar da azaldı. Önemli olarak, DOT1L’in sadece varlığı değil katalitik fonksiyonu gerekliydi: histon işaretini koyamayan mutant sürümler normal antikor sınıf değiştirmeyi geri getiremedi.
AID’e zaman tanımak için gen okuyucuyu yavaşlatmak
İlk bakışta bu kafa karıştırıcıdır çünkü DOT1L aktif genlerle ilişkilendirilir, ancak onu ortadan kaldırmak genleri basitçe kapatmadı. Yeni sentezlenen RNA’nın anlık görüntüsünü alan bir yöntem kullanarak, ekibin DOT1L eksik B hücrelerinin aslında birçok DOT1L-işaretli gende daha fazla yeni transkript ürettiğini keşfettiler — buna karşılık bu genlerin üzerinde ana gen-okuma enzimi olan RNA polimeraz II’nin biraz daha az bulunmasına rağmen. Bu yeni sentezlenen RNA ölçümü ile polimeraz yerleşim haritalarını birleştirerek, normal koşullar altında DOT1L’in histon işaretlerinin nazikçe hız kesici görevi gördüğü çıkarımına vardılar. Bu işaretler, polimerazın gen boyunca ilerlerken hızını yavaşlatır ve DOT1L-işaretli genlerin başlangıç yakınlarında ve gen gövdeleri içinde kısa duraklamaları uzatır. DOT1L olmadığında, polimeraz daha hızlı ilerler ve duraklamalar daha kısa sürer. Oysa AID’in DNA’ya bağlanabilmesi için polimerazın kaldığı ve DNA’nın kısa süreliğine açığa çıktığı pencerelere ihtiyacı vardır; bu hızlanma paradoksal olarak AID’in tutunma ve görevini yapma yeteneğini azaltır; tüm transkripsiyon artmasına rağmen AID etkinliği düşer.
Gen etkinliğini mutasyon riskinden ayırmak
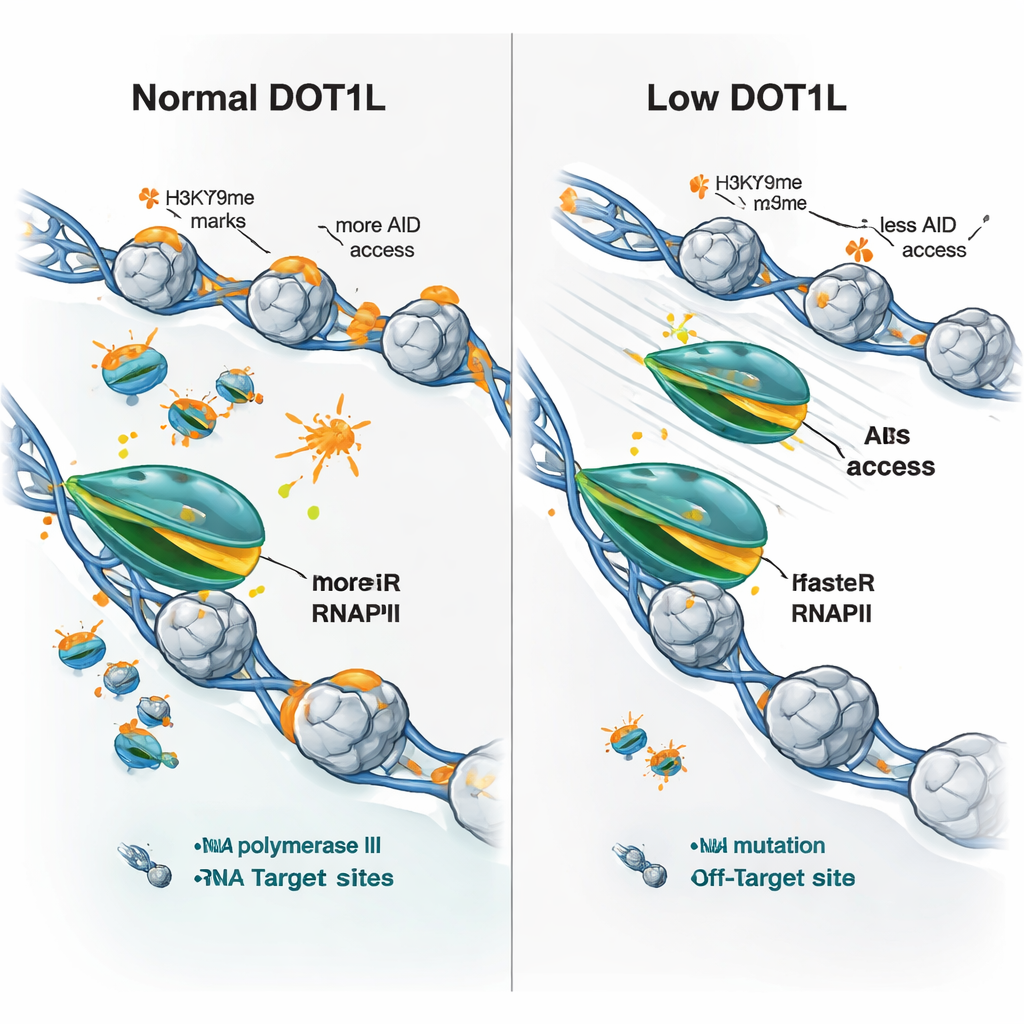
Araştırmacılar daha sonra bu hız değişikliklerinin DOT1L kaybında görülen karışık gen ifade desenlerini açıklayıp açıklamayacağını sordular — bazı genler artarken bazıları azalıyor. DOT1L-işaretli hemen hemen tüm genlerin yokluk hücrelerinde ortak bir özelliği olduğunu buldular: RNA polimeraz II tarafından daha hızlı uzama. Ancak sonuç başlangıç durumuna bağlıydı. Yavaş, zayıf ifade edilen genler, polimeraz hızlandığında genellikle daha fazla RNA üretme eğilimindeyken; zaten aktif, uzun ve hızlı polimerazlara sahip genler bazen daha az üretim gösteriyordu; muhtemelen çok hızlı geçiş verimli işleme veya tamamlanmayı bozuyor. Kritik olarak, hem antikor genlerinde hem de klasik AID hedef-dışı genlerde DOT1L kaybı polimeraz hareketini hızlandırdı, polimerazın “takılma” izlerini azalttı ve genler kapatılmamış olsa bile AID yerleşimini belirgin biçimde düşürdü.
Bu durum bağışıklık ve kanser açısından neden önemli
Bir araya getirildiğinde, bu çalışma DOT1L’i B hücrelerinde genleri okuyan makinelere ilişkin ince bir trafik kontrolörü olarak gösteriyor. DOT1L belirli histon işaretleri koyarak RNA polimeraz II’yi hafifçe yavaşlatır ve duraklamalarını uzatır; böylece AID’in antikor genleriyle verimli şekilde etkileşime girebileceği — ve ne yazık ki sınırlı sayıda diğer hassas gene de — uygun bir transkripsiyonel ortam oluşturur. DOT1L eksik veya inhibitörle engellendiğinde, polimeraz hızla geçer ve AID’in eylem şansları azalır; bu durum antikor çeşitlendirmesini köreltirken aynı zamanda bazı zararlı yeniden düzenlenmelerin riskini düşürür. Bu mekanistik içgörü, DOT1L kaybının hem gen ekspresyonunu artırıp azaltabilmesini açıklar ve transkripsiyon hızının ince kontrolünü bağışıklık sistemimizin kendi DNA’sını nereye ve ne zaman yeniden yazmaya cesaret ettiğine doğrudan bağlar.
Atıf: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Anahtar kelimeler: antikor çeşitlendirmesi, AID enzimi, DOT1L, gen transkripsiyonu, B hücreleri