Clear Sky Science · tr
Dimerik insan arginin vazopressin reseptörü 1A’nın antagonizmasının moleküler temeli
Hormonal bir beyin reseptörü neden önemli
Vazopressin ve oksitosin gibi hormonlar en çok su dengesi, kan basıncı, doğum ve bağlanma davranışlarını kontrol etmeleriyle bilinir. Ancak reseptörlerinin atomik düzeyde nasıl çalıştığı büyük ölçüde gizli kaldı. Bu makale, sosyal davranış, stres ve bazı beyin bozukluklarıyla bağlantılı olan insan vazopressin V1a reseptörünün ayrıntılı 3B yapılarını ortaya koyuyor. Onun formunu ve ilaçların nasıl engellediğini anlamak, otizm, travma sonrası stres bozukluğu ve Huntington hastalığı gibi durumlar için daha iyi tedaviler tasarlamaya yardımcı olabilir.
Kalp, böbrek ve beyin sinyallerini şekillendiren bir çift reseptör
V1a reseptörü vücuttaki birçok hücrenin yüzeyinde bulunur; özellikle kan damarlarında, böbreklerde ve belirli beyin bölgelerinde yoğundur. Vazopressin hormonu ona bağlandığında, reseptör kan basıncı, sıvı dengesi ve sosyal etkileşim, duygu ve stres için beyin devrelerini kontrol eden iç sinyal yollarını açar. Genetik ve klinik çalışmalar, anormal V1a sinyalizasyonunu otizm spektrum bozukluğu, PTSD ve Huntington hastalığı ile ilişkilendirmiş ve bu reseptörü cazip bir ilaç hedefi haline getirmiştir. Birkaç V1a engelleyici ilaç (antagonist) hâlihazırda kullanımda veya klinik denemelerde, ancak şimdiye dek insan V1a reseptörü yüksek çözünürlükte görülmemişti; bu da onun nasıl bir araya geldiği ve bu ilaçların tam olarak nasıl kapattığı konusunda büyük sorular bırakıyordu. 
Reseptörün birden çok ilaçla bağlı durumunu yakalamak
Araştırmacılar, proteinleri ani olarak dondurup elektron ışınıyla görüntüleyen kriyo-elektron mikroskobu (kriyо-EM) tekniğini kullanarak insan V1a reseptörünü görselleştirdiler. Proteini stabilize etmek için ilaç bağlama yeteneğini koruyan hafifçe değiştirilmiş bir form tasarladılar ve görüntülemeye yardımcı olması için küçük bir antikor fragmenti (nanobody) ile eşleştirdiler. Reseptörün kendi hâlini ve üç tıbben önemli antagonistle bağlı yapılarını çözdüler: erken doğumu engellemek için kullanılan bir peptid ilaç olan atosiban ve otizm veya Huntington hastalığı olan kişilerde test edilmiş beyne nüfuz edebilen iki küçük molekül, balovaptan ve SRX246. Tüm yapılar neredeyse atomik çözünürlüğe ulaştı ve reseptörün yedi membran geçişli heliksinin, esnek döngülerinin ve bağlı ilaçların konumlarını ortaya koydu.
Çift olarak çalışmayı tercih eden bir reseptör
Önceki benzer reseptörlerin yalnız birim olarak görüldüğü durumların aksine, V1a dört kriyo-EM yapısının tamamında bir çift — dimer — olarak göründü. İki reseptör membranda yan yana yatıyor ve başlıca helikslerden biri aracılığıyla sıkı temaslar kuruyor; bu temaslar hem polar hem de yağlı (hidrofobik) etkileşimlerle güçleniyor. Bu çiftleşmenin canlı hücrelerde de olup olmadığını test etmek için ekip V1a’yı parlak bir floresan proteine bağladı ve tek molekül fotoblekleme yöntemi kullandı: hücre yüzeyindeki bir nokta iki reseptör kopyası içeriyorsa, ışığı iki adımda kaybolurdu. Gözlemlenen noktaların yaklaşık dörtte üçü tam olarak iki adımda söndü; bu da V1a’nın hücre yüzeyinde doğal olarak dimer oluşturduğunu kuvvetle destekliyor. Bilim insanları arayüzü bozmak için ana temas kalıntılarını mutasyona uğrattıklarında, reseptör tek birimlere doğru kaydı ve hormona ve ilaca daha az duyarlı oldu; bu da dimerin yalnızca yapısal bir süsleme değil, işlevsel olarak önemli olduğunu düşündürüyor. 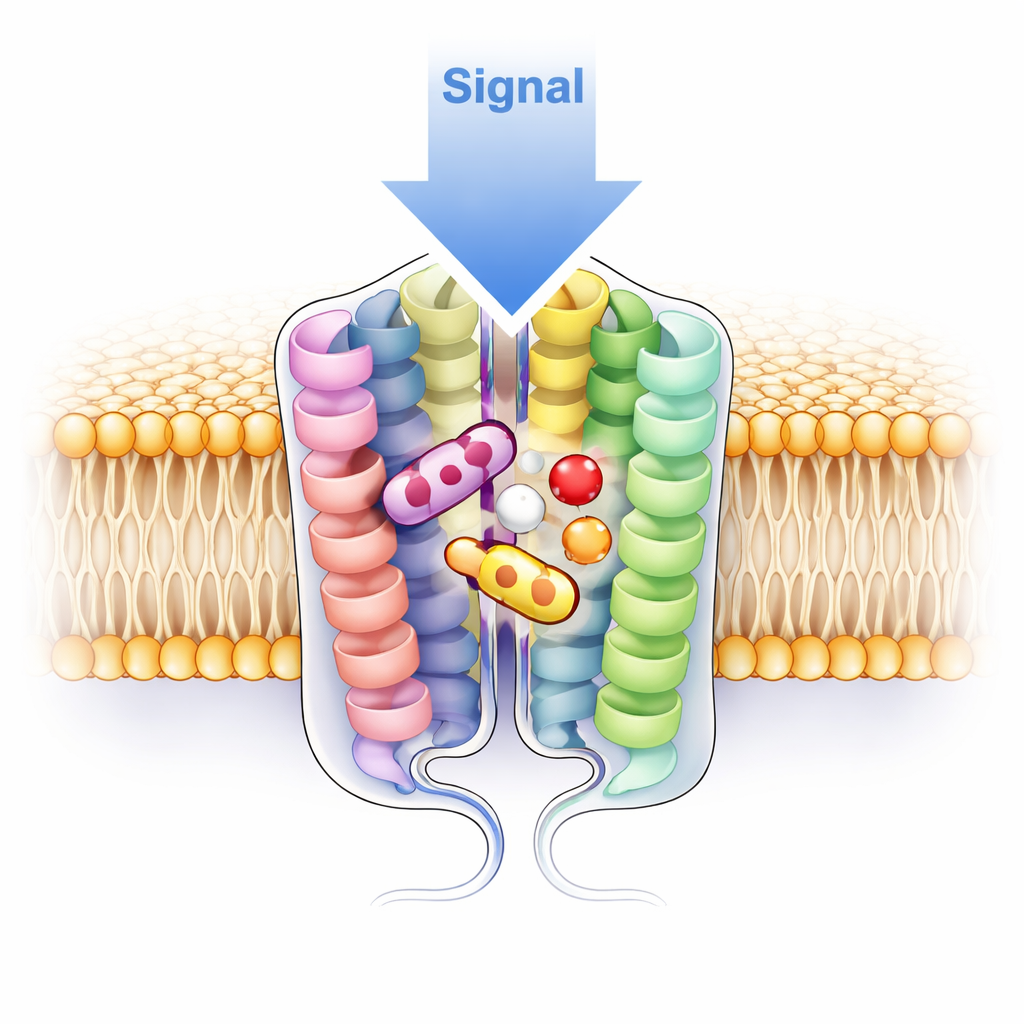
Hormon giriş yolunda esnek bir kapı
Ekip, hormon bağlama cephesinin üstünde yer alan ekstrasellüler döngü 2 (ECL2) adında beklenmedik bir “kapı” bölgesi keşfetti. İlaçsız (apo) durumda bu döngü cebi bir kapak gibi yatay şekilde kapatıyor ve birçok ilgili reseptörde görülen tipik disülfid bağını (kükürt–kükürt bağı) oluşturmuyordu. Bunun yerine döngünün parçaları cebe doğru katlanıyor ve çevredeki helikslerle kurulan bir etkileşim ağı tarafından yerinde tutuluyor; bu durum büyük, yapışkan bağlama boşluğunu kısmen örtüyor. Üç antagonistin herhangi biri bağlandığında, ECL2 yukarı doğru dönüyor ve klasik disülfid bağını oluşturuyor; ilaçların yerleştiği geniş, çözücü dolu bir boşluk yaratıyor. Bu dramatik hareket, V1a’nın rastgele moleküller tarafından istenmeyen aktivasyonu sınırlamak için ECL2’yi dinamik bir bariyer olarak kullanabileceğini ve ilaçların döngüyü düz “temel durumunda” kilitleyecek veya yükselmiş, açık konformasyonu kullanacak şekilde tasarlanabileceğini öne sürüyor.
Üç ilacın aynı reseptörü farklı şekillerde susturması
Doğal hormon oksitosine yakından benzeyen atosiban, cebi tepesinden tabanına kadar uzanır ve kendini hidrojen bağları ve hidrofobik temasların bir kombinasyonuyla sabitler. Oksitosine kıyasla birkaç kilit pozisyonu değiştirerek, reseptör aktivasyonu için gereken iç kayma zincirini tetikleyemiyor: sinyal sırasında hareket eden kritik “mikroanahtar” kalıntılar inaktif pozisyonlarında kilitli kalıyor, G proteinin gireceği iç boşluk açılmıyor ve aktivasyon için önemli bir magnezyum bağlama bölgesi bozuluyor. Buna karşılık, balovaptan ve SRX246 derinlere inen kompakt, peptid dışı moleküller olup farklı stratejiler kullanıyor. Balovaptan, derin bir yarığa sıkıca yerleşen rijit, hidrofobik bir çekirdeğe ve cep girişine doğru uzanan esnek, polar bir kuyruğa dayanıyor. SRX246 ise β-laktam çekirdeği ile sabitlenen modüler, fragman benzeri bir mimari kullanıyor; farklı “bölgeler” alt cepleri tıkıyor ve ekstrasellüler döngülere doğru uzanıyor. Her iki durumda da ilaçlar G protein bağlanmasıyla uyumsuz olan inaktif bir konformasyonu stabilize ediyor. Cep şekli ve kimyasında, özellikle heliks 5 ve 7 üzerindeki iki pozisyondaki ince farklar, balovaptan ve SRX246’nın benzer reseptörlere kıyasla V1a’yı tercih etmesini açıklamaya yardımcı oluyor.
Gelecekteki tedaviler için çıkarımlar
V1a’yı dimer olarak yüksek çözünürlüklü anlık görüntülerle sağlaması, ilaçsız durumda daha önce görülmemiş “düz” bir döngü konformasyonunu ortaya koyması ve üç çok farklı antagonistin reseptörü nasıl kapattığını ayrıntılandırması sayesinde bu çalışma, ilaç tasarımcılarına V1a’yı hedeflemek için kesin bir yapısal harita sunuyor. Bu, ya dimer-spesifik özelliklerden yararlanan ya da reseptörü özellikle inaktif bir temel duruma kilitleyen yeni nesil ilaçlar üretme yollarını işaret ediyor; nihai amaç beyin ve stresle ilişkili bozuklukları daha spesifik ve daha az yan etkiyle tedavi etmektir.
Atıf: Zhong, P., Chu, B., Yu, Z. et al. Molecular basis of antagonism of the dimeric human arginine vasopressin receptor 1A. Nat Commun 17, 1622 (2026). https://doi.org/10.1038/s41467-026-68331-5
Anahtar kelimeler: vazopressin V1a reseptörü, G proteinine bağlı reseptör, reseptör dimerleşmesi, kriyо-EM yapı, nöropsikiyatrik ilaç tasarımı