Clear Sky Science · tr
Stereodiverjan seçiciliğe sahip genelci siklopropanazların hesaplamalı tasarımı
Neden küçük üç halkalı yapılar ilaçlar için önemli
Siklopropanlar—üç üyeli karbon halkaları—küçük, gerilmiş yapı taşlarıdır ve bir ilacın vücutta nasıl davrandığını dramatik şekilde değiştirebilirler. Atomların 3B düzeni (stereokimya) bir molekülün faydalı bir ilaca mı yoksa etkisiz ya da zararlı bir benzerine mi dönüşeceğini belirleyebilir. Bu makale, aynı başlangıç malzemelerinden bu halkaların dört olası 3B biçiminin tamamını güvenilir şekilde üretebilen enzimleri tasarlamak için hesaplamalı bir stratejiyi anlatıyor; bu da ilaç adaylarının daha hızlı ve daha temiz şekilde araştırılmasına kapı açıyor.
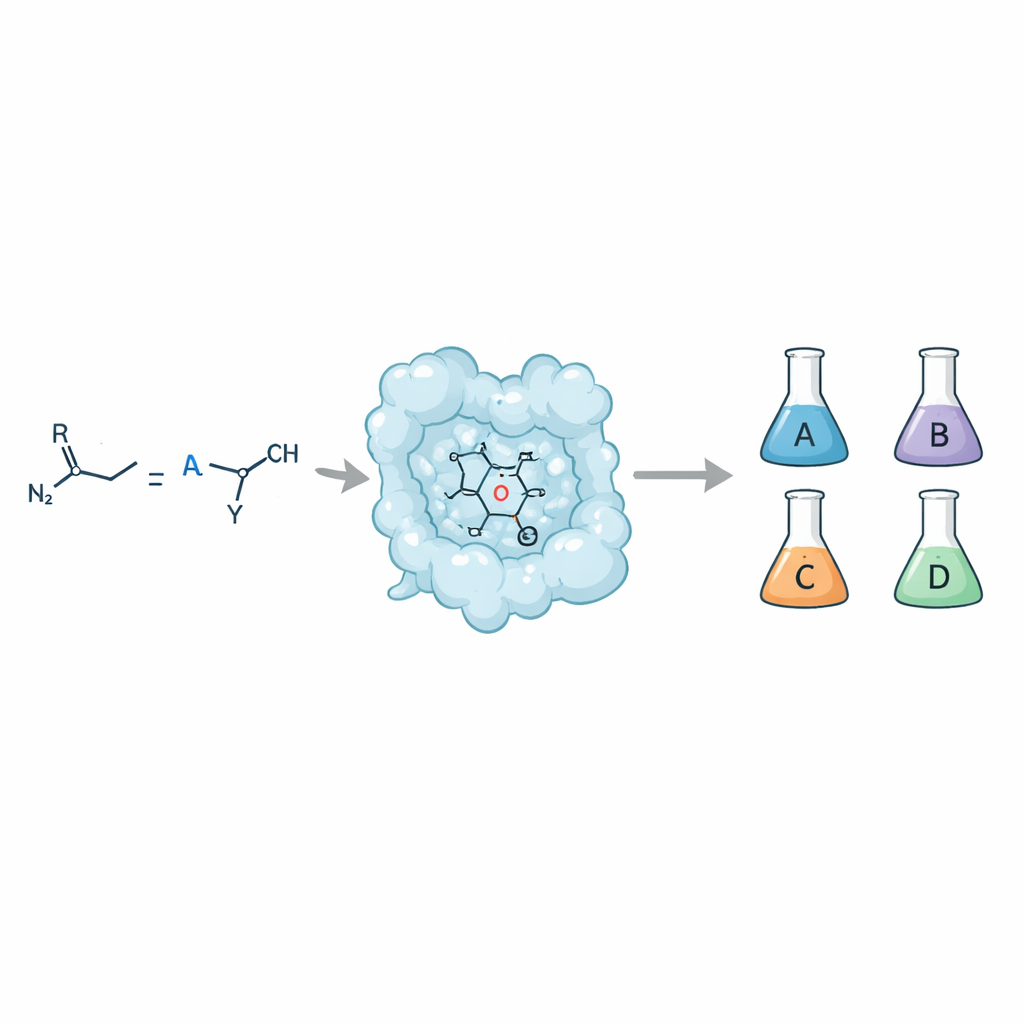
Tek bir reçeteden dört farklı sonuç
Basit bir çift bağlı bağ (olefin) bir diazo bileşiği gibi bir karben vericisiyle reaksiyona girdiğinde, sonuç bir siklopropan halkası olabilir. Ancak o halka, aynı atomlara sahip olmakla birlikte uzayda farklı biçimlenen dört ayrı stereoisomerik form alabilir. Kimyacılar bu formların her birine erişmek ister çünkü bunlar biyolojik hedeflerle çok farklı etkileşimler gösterebilir ve emilim, metabolizma ve güvenlik gibi temel ilaç özelliklerini etkileyebilir. Geleneksel küçük molekül katalizörleri bazen bu kontrolü sağlayabilir, ancak enzimlerle—doğanın kendi katalizörleriyle—bunu başarmak zor olmuştur; özellikle hem yüksek seçiclik hem de çok çeşitli substratlara tolerans hedeflendiğinde.
Bilgisayar ekranında enzim tasarlamak
Yazarlar bu problemi çözmek için mekanizma‑temelli, çok durumlu bir hesaplamalı iş akışı geliştirdiler. Önce her bir siklopropan stereoisomerinin oluşumu için reaksiyon yolundaki yüksek enerjili yapı olan geçiş hallerini nicel olarak modellemek üzere kuantum kimyası hesaplamaları kullandılar. Bu modeller daha sonra farklı heme içeren proteinlerin aktif bölgelerine yerleştirildi ve Rosetta protein tasarım yazılımı her bir proteinin her bir geçiş halini ne kadar stabilize veya destabilize ettiğini değerlendirmek için kullanıldı. Kritik olarak, tasarım skoru istenen geçiş halini hem destekleyen (pozitif tasarım) hem de rekabet edenleri caydıran (negatif tasarım) mutasyonları ödüllendirdi; bu da enzime diğer 3B ürünlere kıyasla birini “tercih etmesini” öğretmiş oldu.
Tam bir enzim araç takımı oluşturmak
Bu yaklaşımla ekip, bir aile “genelci” siklopropanaz enzimi yarattı. Miyoglobin başlangıç alınarak, aktif bölgesi yeniden tasarlandı ve trans-(1R,2R) siklopropanı çok yüksek seçicilikle ve 20’den fazla farklı olefin üzerinde iyi aktiviteyle (aktif olmayan ve elektron fakiri zorlu substratlar dahil) üreten varyantlar elde edildi. Önceden tasarlanmış bir miyoglobin tamamlayıcı trans-(1S,2S) ürününü zaten sağlıyordu. İki sis ürünü elde etmek için yazarlar başka heme proteinlerine yöneldiler. Bakteriyel enzim P450cam yeniden şekillendirilerek selektif olarak cis-(1S,2R) ürününü veren varyantlar elde edildi ve insan indolamin 2,3‑dioksijenaz‑1 (IDO1)—daha önce karben kimyası için kullanılmamış—cis-(1R,2S) ürününü tercih edecek şekilde yeniden amaçlandı. Toplamda bu dört biokatalizör aynı siklopropan ürün setinin her stereoisomerini sunabiliyor; sıklıkla diastereomer ve enantiomer üzerinde %99’a kadar kontrol sağlanabiliyor.
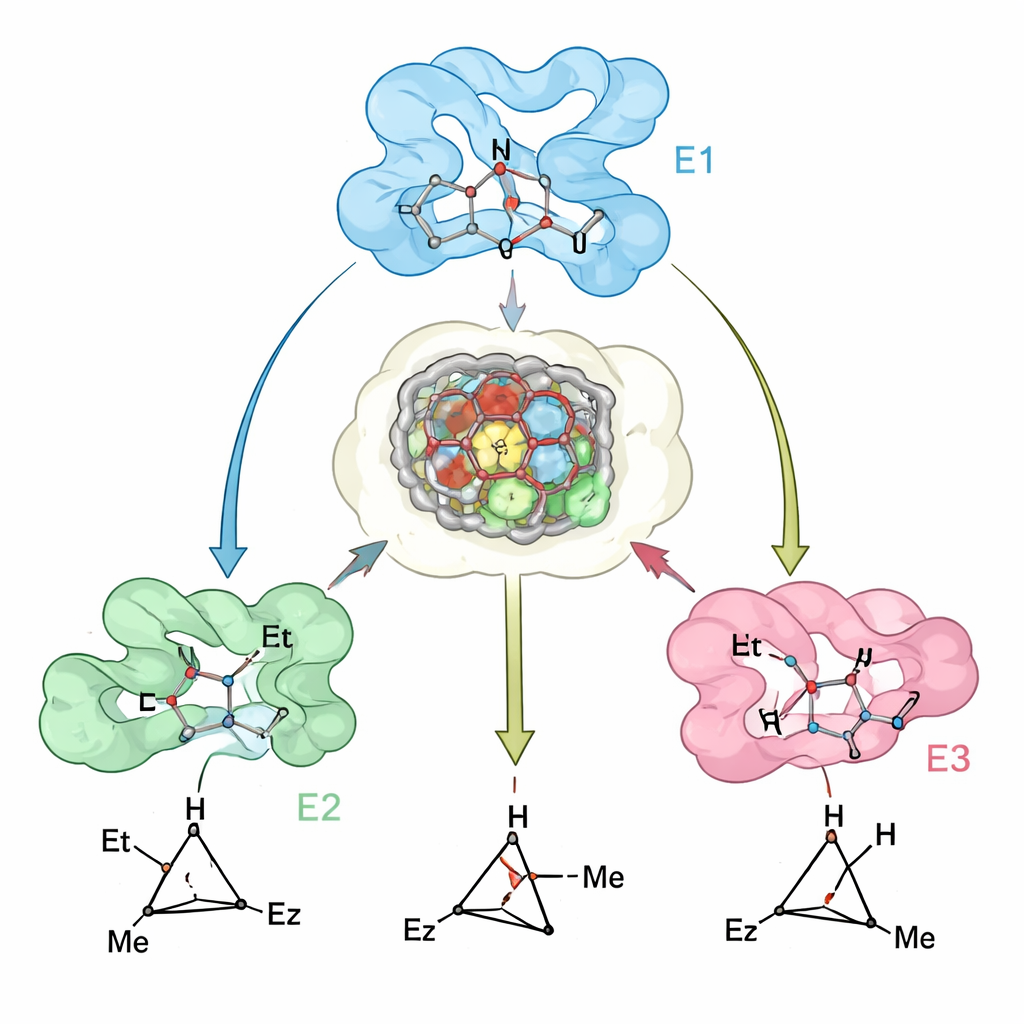
Tasarımın gerçeğe ne kadar uyduğunu görmek
Hesaplamalı modellerinin gerçek enzimleri ne kadar yansıttığını test etmek için araştırmacılar bir ana miyoglobin varyantının kristal yapısını çözdüler ve bunları tahmin edilen yapılarla karşılaştırdılar. Uyum yakındı ve deneysel veriler ince ama önemli bir özelliği vurguladı: protein aktif bölgesi tercih edilen geçiş halini ağırlamaya önceden düzenlenmiş durumda, o sırada yakın döngüler ve helikslerdeki küçük kaymalar “yanlış” geçiş halinin bağlanmasını enerji açısından elverişsiz kılıyor. Tahminlerin daha az doğru olduğu yerlerde—örneğin bazı hacimli substratlar için—farklılıklar modellemede tam yakalanmamış omurga hareketlerine bağlanabiliyordu; bu da gelecekteki tasarım yöntemlerini iyileştirmek için belirgin yollar gösteriyor.
Gelecekteki ilaçlar ve katalizörler için anlamı
Fizik‑temelli geçiş hali modellemesini akıllı protein yeniden tasarımıyla birleştirerek, bu çalışma enzim-katalizli reaksiyonların stereokimyasal sonuçlarının deneme‑yanılma evrimiyle keşfedilmek yerine önceden programlanabileceğini gösteriyor. Ortaya çıkan siklopropanaz seti, kimyacıların geniş bir başlangıç olefininden tam siklopropan stereoisomer setlerini pratik şekilde üretmelerini sağlayarak ilaç keşfinde yapı‑etkinlik çalışmalarını ve doğal ürün sentezini büyük ölçüde basitleştiriyor. Aynı strateji diğer enzim tiplerine ve reaksiyon sınıflarına uyarlanabilir olmalı; bu da karmaşık moleküller üzerinde hassas 3B kontrol sağlayan biokatalizörlerin oluşturulmasını hızlandıracaktır.
Atıf: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Anahtar kelimeler: biokataliz, siklopropanasyon, enzim tasarımı, stereokimya, heme proteinleri