Clear Sky Science · tr
SHOC2-KRAS-PP1C kompleksinin yapısı, RAS izoformuna özgü belirleyicileri ve RAS inhibitörleriyle kompleks oluşumunun hedeflenmesine dair çıkarımları ortaya koyuyor
Hücreler Büyümeye Ne Zaman Karar Verir?
Hücrelerimiz, ne zaman büyüyeceklerine, bölüneceklerine ya da sessiz kalacaklarına karar vermek için içsel bir kablolanma sistemine güvenir. Bu sistemin merkezinde, kanserde sıkça bozulabilen küçük moleküler anahtarlar olan RAS proteinleri bulunur. Bu çalışma, SHOC2, RAS ve PP1C adlı belirli bir protein grubunun anahtar bir büyüme anahtarını nasıl çevirdiğini ve modern kanser ilaçlarının bu süreci daha etkili engelleyecek şekilde nasıl ayarlanabileceğini ve tümörlerin tedaviyi alt etmesini nasıl önleyebileceğini derinlemesine inceliyor.
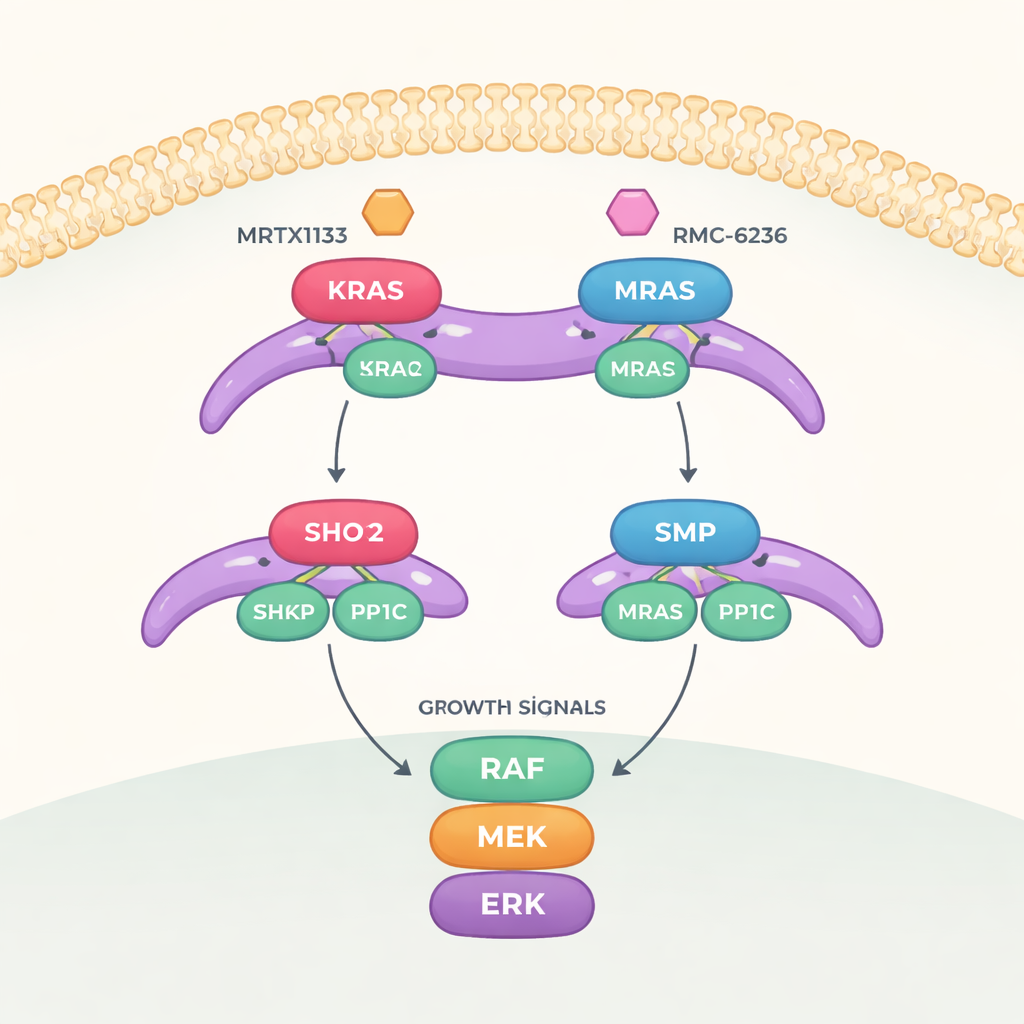
Üç Kritik Parçadan Oluşan Bir Büyüme Anahtarı
Çalışma, hücre yüzeyinden çekirdeğe büyüme mesajları taşıyan MAPK adlı bir sinyal yoluna odaklanıyor. Bu yolun tam olarak açılması için RAF adlı başka bir proteinin “kapalı” halden “açık” hale geçirilmesi gerekir. Bu anahtar, SHOC2 (bileşenleri bir arada tutan bir iskelesel protein), PP1C (bir fosfat etiketini çıkaran enzim) ve aktif bir RAS proteinden oluşan üç parçalı bir kompleks tarafından kontrol edilir. Bir araya geldiğinde bu üçlü RAF üzerindeki belirli bir fosfat işaretini kaldırır ve böylece RAF alt akıştaki büyüme kaskadını etkinleştirebilir.
Daha Düşük Afiniteli Bir Ortak Kanserde Neden Hâlâ Önemli?
Çeşitli RAS proteinleri vardır. MRAS, SHOC2 ve PP1C ile çok sıkı bir kompleks oluştururken, daha iyi bilinen kanser sürücüleri olan KRAS, HRAS ve NRAS aynı kompleksin daha zayıf versiyonlarını oluşturur. Buna rağmen, mutant KRAS, HRAS veya NRAS ile sürülen kanser hücreleri, kompleksleri daha az kararlı olsa bile SHOC2’ye güçlü şekilde bağımlı çıkıyor. Büyük genetik tarama veri setleri, özellikle Q61 ve G13 gibi kilit pozisyonları etkileyen belirli RAS mutasyonlarına sahip birçok tümörün SHOC2 kaybına karşı yüksek duyarlılık gösterdiğini, yani bu birleşimin hayatta kalmaları için elzem olduğunu gösteriyor.
KRAS Kompleksinin Şeklini Ortaya Çıkarmak
Bugüne dek bilim insanları sadece sıkı MRAS bazlı kompleksin yüksek çözünürlüklü yapısını görmüşlerdi. Daha zayıf KRAS versiyonu çok kolay parçalanıyordu ve yakalanamıyordu. Bu çalışmada yazarlar, bileşenler arasındaki temasları hafifçe güçlendiren hastalık bağlantılı mutasyonları kullanarak SHOC2–KRAS–PP1C kompleksini kriyo-elektron mikroskopisiyle görüntüleyebilmek için yeterince stabilize ettiler. Genel mimarinin MRAS kompleksine yakın olduğunu buldular, ancak KRAS’in MRAS’in SHOC2 ve PP1C’yi daha sıkı tutmak için kullandığı birkaç küçük yapısal özelliğe sahip olmadığını gösterdiler. Sonuç olarak KRAS birleşimi daha az temas yüzeyi gömer ve daha az bağ kurar; bu da içsel olarak neden daha az kararlı olduğunu açıklıyor, buna rağmen KRAS’in aşırı etkin olduğu tümörlerde hâlâ son derece önemli kalıyor.
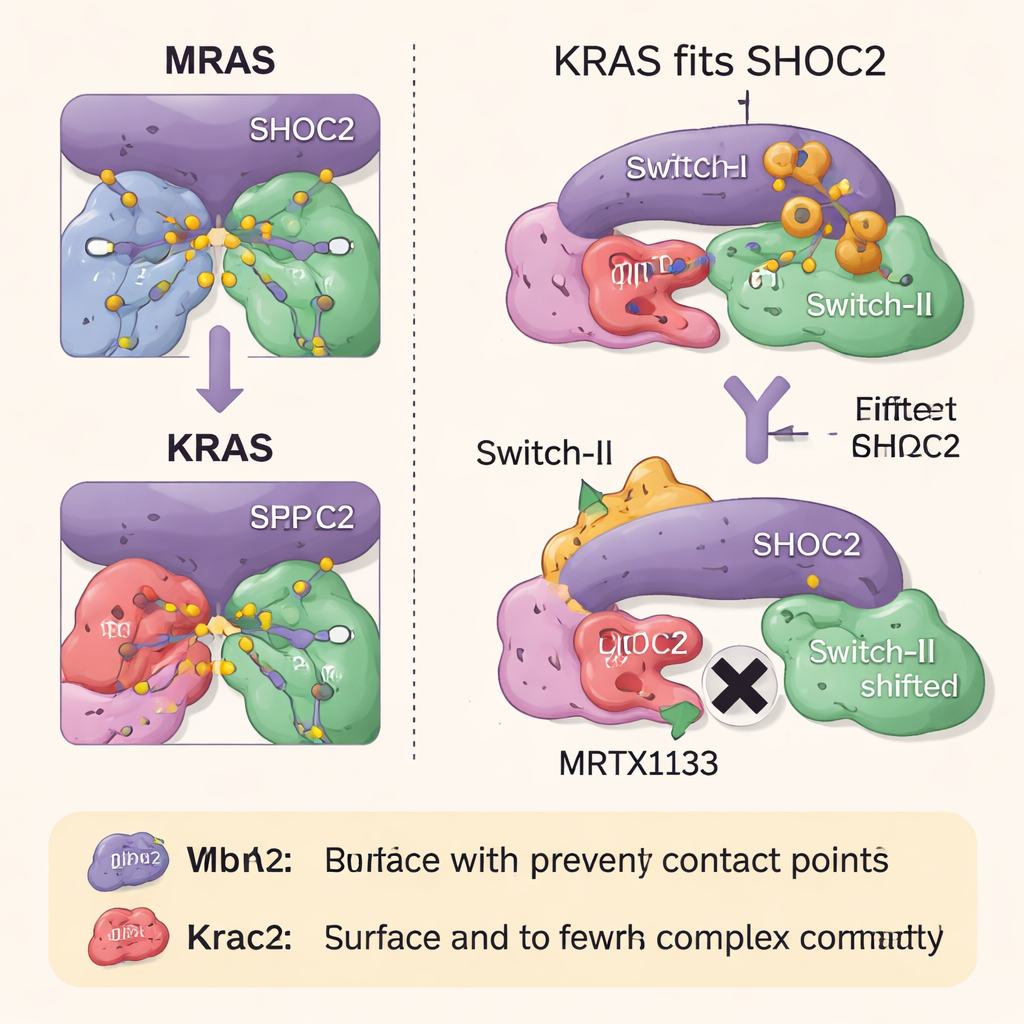
RAS İlaçları Kompleks Oluşumunu Nasıl Engelliyor?
Araştırma ekibi sonra iki sınıf RAS hedefli ilacın bu üçlü kompleksi nasıl etkilediğini inceledi. KRAS’in Switch-II olarak bilinen esnek bölgesine yakın bir cepte bağlanacak şekilde tasarlanmış MRTX1133, bu bölgeyi SHOC2 yüzeyiyle çakışan bir şekle kilitler. Bu, yeni SHOC2–KRAS–PP1C komplekslerinin oluşmasını güçlü şekilde engelliyor, ancak zaten var olanları parçalamada daha az etkilidir. İkinci bir ilaç olan RMC-6236, yardımcı bir protein (siklofilin A) ile birlikte çalışır ve SHOC2 bağlanması için gereken aynı KRAS yüzeylerini de bloke eder. Ancak hiçbir ilaç doğal olarak MRAS’e bağlanmadığı için yüksek afiniteli MRAS kompleksi sağlam kalır ve KRAS inhibe edildiğinde büyüme yolunu yeniden etkinleştirmeye yardımcı olabilir.
Direnci Önlemek İçin Çifte Hedefe Doğru
Çifte hedeflemenin mümkün olup olmadığını test etmek için araştırmacılar, Switch-II cebini MRTX1133’ün artık bağlanabileceği şekilde değiştirilmiş bir MRAS versiyonu mühendislediler. Bu mutant hâlâ SHOC2 ve PP1C ile güçlü bir kompleks oluşturdu, ancak ilaç artık onun oluşumunu engelledi ve tüp içi deneylerde RAF’ı etkinleştirme yeteneğini azalttı. SHOC2’ye bağlanan bileşiklere dair verilerle birlikte, bu sonuçlar hem KRAS bazlı hem de MRAS bazlı kompleksleri kapatacak ilaçlar tasarlamanın gerçekçi olduğunu gösteriyor. Bir bilim dışı okuyucu için ana mesaj, kanser hücrelerinin özellikle bir anahtar ilaçla hedeflendiğinde büyüme sinyallerini akıtmak için birden çok, birbirine yakın anahtar kullandığıdır. Bu protein düzeneklerinin kesin şekillerini ve temas noktalarını anlayarak, araştırmacılar artık yedek yolların her ikisine birden saldıran terapiler planlayabilir; bu da RAS kaynaklı kanserlerin uyum sağlamasını ve direnç geliştirmesini zorlaştırır.
Atıf: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Anahtar kelimeler: RAS sinyalleşmesi, KRAS inhibitörleri, MAPK yolu, protein kompleksleri, ilaç direnci