Clear Sky Science · tr
Krıyo‑EM ile tersinir lipid aracılı pH‑anahtarlaması: koneksin‑46/50
Sağlık ve hastalık için neden küçük hücre kanalları önemli
Hücrelerimiz her saniye, aralık bağlantıları adı verilen mikroskobik tüneller yoluyla elektriksel sinyaller ve küçük moleküller değiş tokuş eder. Bu kanallar kalbin eş‑zamanlı atmasını, beynin toksik yan ürünleri temizlemesini ve göz merceğinin şeffaf kalmasını sağlar. Hücre içi koşullar asitleştiğinde —örneğin inme, kalp krizi veya katarakt oluşumu sırasında— birçok kanal kapanır; bunun nasıl algılandığı ve asiditeye nasıl yanıt verildiği ise uzun süredir gizemini koruyordu. Bu çalışma, yüksek çözünürlüklü krıyo‑elektron mikroskopisi kullanarak, göz merceğindeki belirli bir kanalın asite nasıl kapandığını ve bu sürecin tamamen nasıl tersine çevrilebildiğini neredeyse atom atom ortaya koyuyor.
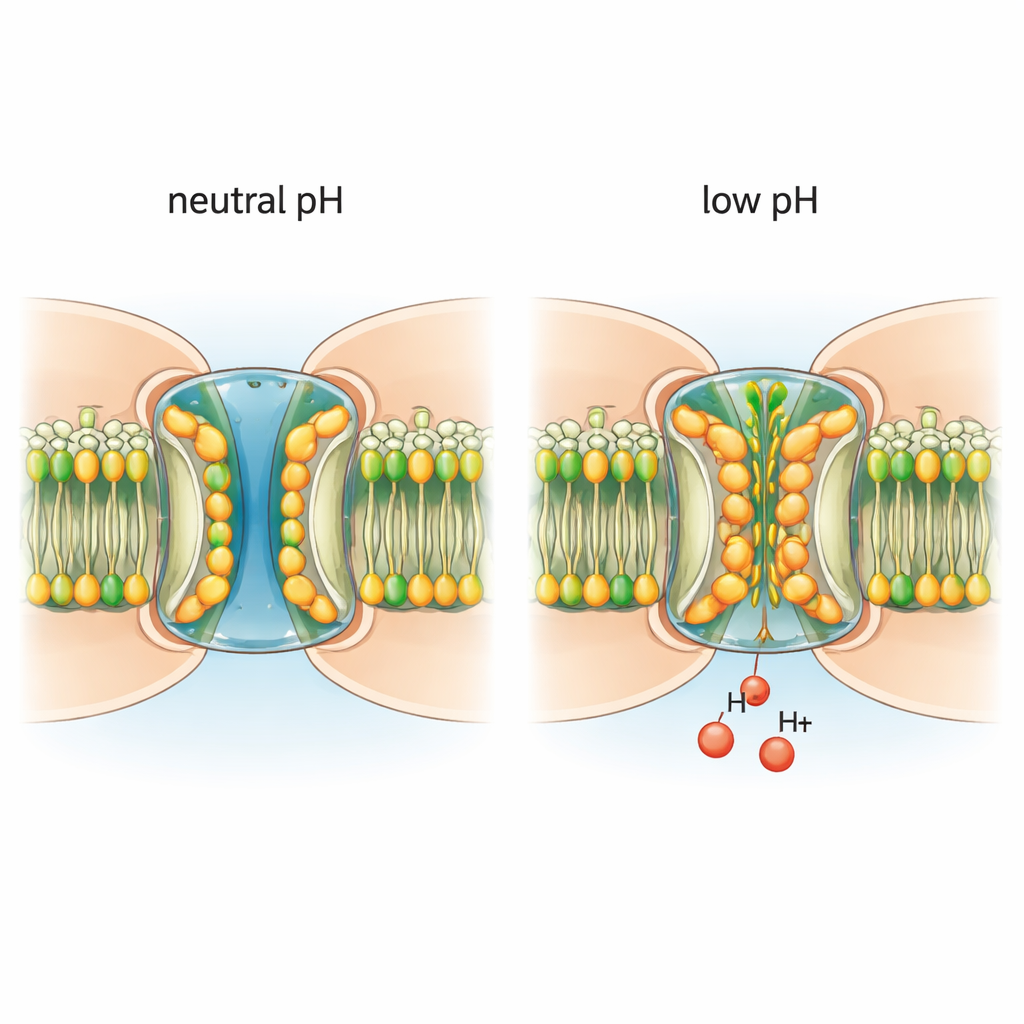
Dokuları eş‑zamanlı tutan hücresel tüneller
Aralık bağlantıları, koneksin adı verilen proteinlerden yapılır; bu proteinler iki komşu hücrenin zarlarını geçen halka şeklinde kanallar oluşturmak üzere bir araya gelir. Bu çalışma, göz merceğinde kanal oluşturan birbirine yakın iki koneksin türü olan koneksin‑46 ve koneksin‑50 çiftine odaklanır. Bu kanallar iyonların ve küçük moleküllerin hücreler arasında doğrudan akmasına izin vererek mercek şeffaflığının ve doku sağlığının korunmasına yardımcı olur. Ancak hücreler stres altındayken aynı kanallar zararlı sinyallerin yolları haline gelebilir. Dokuları korumak için hücre içi ortam asidik hale geldiğinde aralık bağlantıları kapanır. Bu “pH‑anahtarlamasının” ince ölçekli mekanizmasını anlamak, dokuların stresten nasıl kurtulduğunu ve belirli mutasyonların neden katarakt gibi hastalıklara yol açtığını çözmek için önemlidir.
Krıyo‑EM ile kanalların hareketini görmek
Araştırmacılar, yaşlı koyun merceklerinden izole ettikleri natif koneksin‑46/50 kanallarını saflaştırıp model bir zar içinde yerleştirdiler. Krıyo‑elektron mikroskopisi kullanarak, kanalın açık gözenek lehine olan nötr koşullar altında ve anahtarlamayı tetikleyen hafif asidik koşullar altında neredeyse atomik çözünürlükte görüntüler aldılar. Nötr pH’da kanallar çoğunlukla stabil bir açık durumda bulunuyor; merkezi tünel iyonlar ve küçük moleküller için yeterince geniş ve gözenek girişini döşeyen esnek bir segment olan N‑terminal domaini görünür durumdaydı. Bu koşullarda gözenek temizdi: yolu tıkayan ekstra moleküller yoktu ve çevreleyen membran lipidleri düzenli katmanlar halinde organize olmuştu.
Asit lipidleri gözenek içine çeker
Ortam hafifçe asidik hale getirildiğinde kanalın mimarisi çarpıcı şekilde değişti. Çevreleyen zarın lipid molekülleri gözenek içine çekildi, N‑terminal segmentlerin arasına ve altına kaydı. Bu giren lipidler, N‑terminalleri içe doğru iten ve kanalı daraltarak akışı engellemeye yardımcı olan iki katmanlı hidrofobik bir “conta” oluşturdu. Ek lipidler, komşu protein alt birimlerinin arayüzlerine takılarak membrandan gözenek içine giriş yolları işlevi gördü gibi görünüyordu. Önemli olarak, kanallar gerçek bir lipid zarı olmayan deterjan ortamına konulduğunda düşük pH bu yapısal değişiklikleri artık indüklemedi. Bu, gerçek lipidlerin yalnızca yan rol oynamadığını; pH‑anahtarlama sürecinin gerekli ortakları olduğunu gösterir.
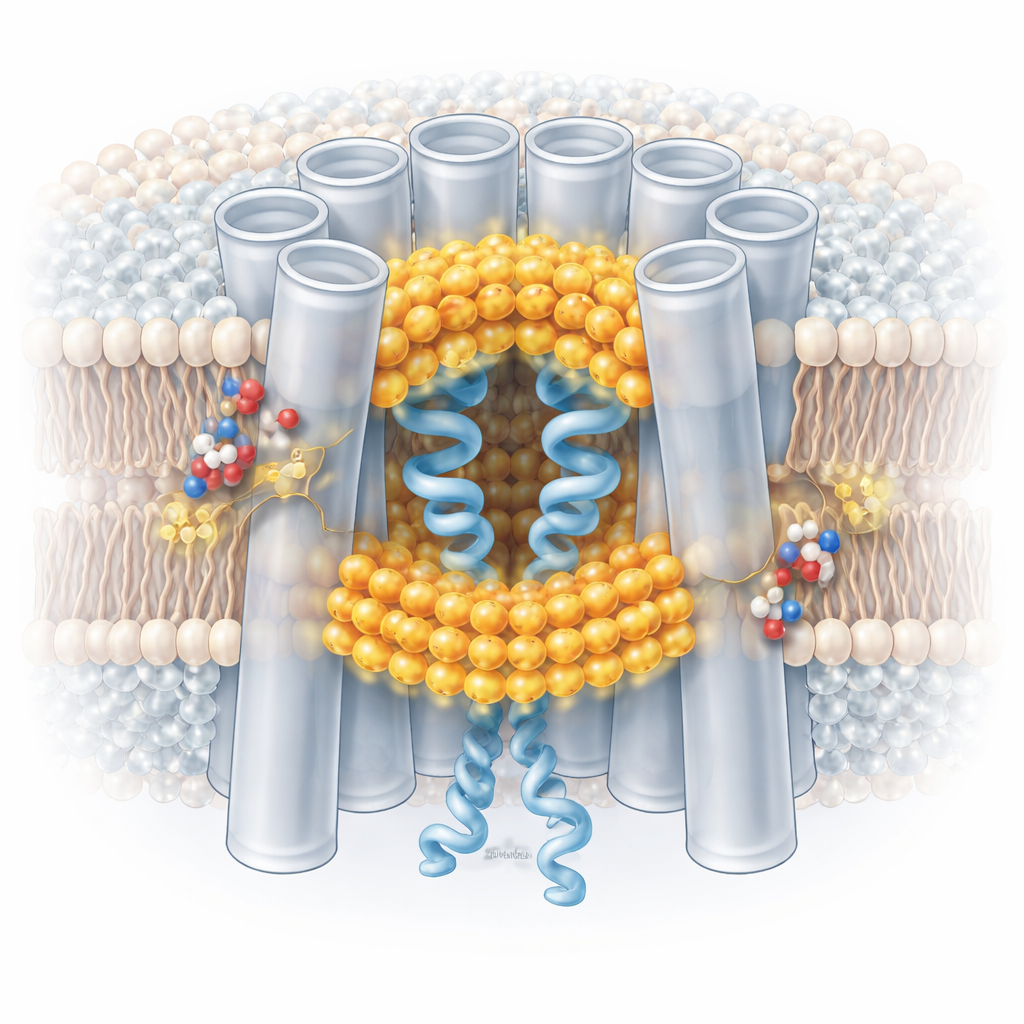
Tersinir ve ince ayarlanmış bir güvenlik anahtarı
Milyonlarca bireysel kanal parçacığını izleyerek yazarlar, düşük pH’ın kanalları basitçe tamamen açık halden tamamen kapalı hale çevirmediğini buldu. Bunun yerine, popülasyonu bir karışım durumlarına kaydırıyor: bir kanal içindeki bazı alt birimler lipid‑tarafından stabilize edilmiş, anahtarlanan konformasyonlar gösterirken diğerleri daha açık kalıyor. Anahtarlama davranışı büyük ölçüde kooperatif değil—kanalın her yapıtaşı bir derece bağımsız olarak yanıt verebiliyor. Asidik koşullar bu anahtarlanan konformasyonları destekliyor, ancak pH nötre döndürüldüğünde gözenek lipidleri zar içine geri çekiliyor ve kanallar açık duruma geri dönüyor. Düşük pH’da pozitif yük kazanan korunmuş histidin aminoasitleri, bu süreci başlatan arayüz lipidlerini toplayıp stabilize etmeye yardımcı oluyor gibi duruyor; bu da olası bir moleküler pH sensörü sunuyor.
Katarakt ve doku koruması için çıkarımlar
Bu bulgular, lipidlerin asitliğe yanıt olarak aralık bağlantılarındaki akışı tersinir biçimde kontrol eden hareketli tıkacıklar gibi davrandığı bir modeli destekliyor. Göz merceğinde böyle bir mekanizma, hasarlı hücreleri izole etmeye ve toksik sinyallerin yayılmasını önlemeye yardımcı olabilir; ancak kronik veya yanlış düzenlenmiş anahtarlama yaşa bağlı katarakt oluşumuna katkıda bulunabilir. Benzer lipid nüfuzları ilgili kanal ailelerinde de görüldüğünden, çalışma daha genel bir ilkeye işaret ediyor: stres altında hücre zarları, hayati kanalları açıp kapatmaya yardımcı olacak dinamik bileşenler sağlayabilir; bu da hastalıkta açık ya da kapalı durumları stabilize eden ilaçlar için yeni fikirler sunuyor.
Atıf: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Anahtar kelimeler: aralık bağlantıları, koneksin 46/50, pH anahtarlama, katarakt, krıyo‑EM