Clear Sky Science · tr
SARS-CoV-2’nin nükleotid analoglarına dayalı antiviral ilaçlara karşı direncinin mekanizması
Virüsün Önemli Antiviral İlaçları Nasıl Alt Ettiği
COVID-19 virüsü, genetik materyalini düzeltebilen nadir RNA virüsleri grubuna dahildir; bu da bazı en etkili antiviral ilaçlarımıza karşı alışılmadık derecede dirençli olmasını sağlar. Bu çalışma, SARS‑CoV‑2’nin nükleotid analogları olarak adlandırılan yaygın bir ilaç sınıfını atom düzeyinde nasıl tespit edip çıkardığını inceleyerek, diğer virüslere karşı iyi çalışan ilaçların neden koronavirüs enfeksiyonlarında genellikle daha düşük performans gösterdiğini açıklıyor.
Viral RNA Üzerinde Bir Çekişme
SARS‑CoV‑2, ~30.000 harflik RNA genomunu çoğaltmak için replikasyon–transkripsiyon kompleksi adlı büyük bir moleküler makine kullanır. Bunun merkezinde yeni RNA zincirleri inşa eden RNA bağımlı RNA polimeraz (RdRp) ve hataları düzelten, kırpma yapan ayrı bir birim olan eksonükleaz (ExoN) bulunur. Hepatit C için geliştirilenler de dahil birçok antiviral hap, doğal RNA yapı taşlarına oldukça benzeyen şekilde tasarlanmıştır; RdRp tarafından eklenebilirler, ancak kopyalamayı durduracak ya da hatalar oluşturacak ince değişiklikler taşırlar. Ne yazık ki koronavirüsler ExoN’e sahiptir; bu enzim bu sahte yapı taşlarını RNA zincirine eklendikten sonra tanıyıp keserek viral replikasyonu kurtarabilir.
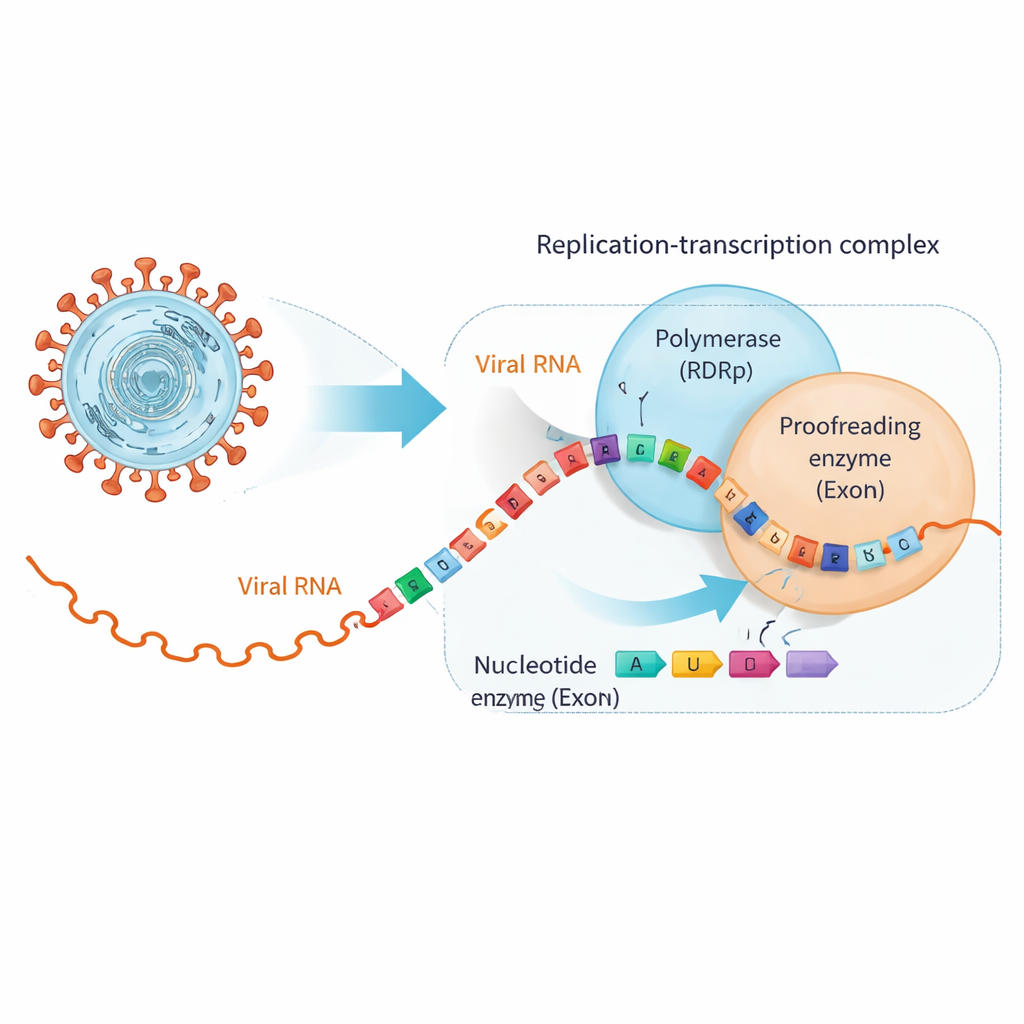
Yararlı İlaçlar RNA’yı Partner Değiştirmeye Zorluyor
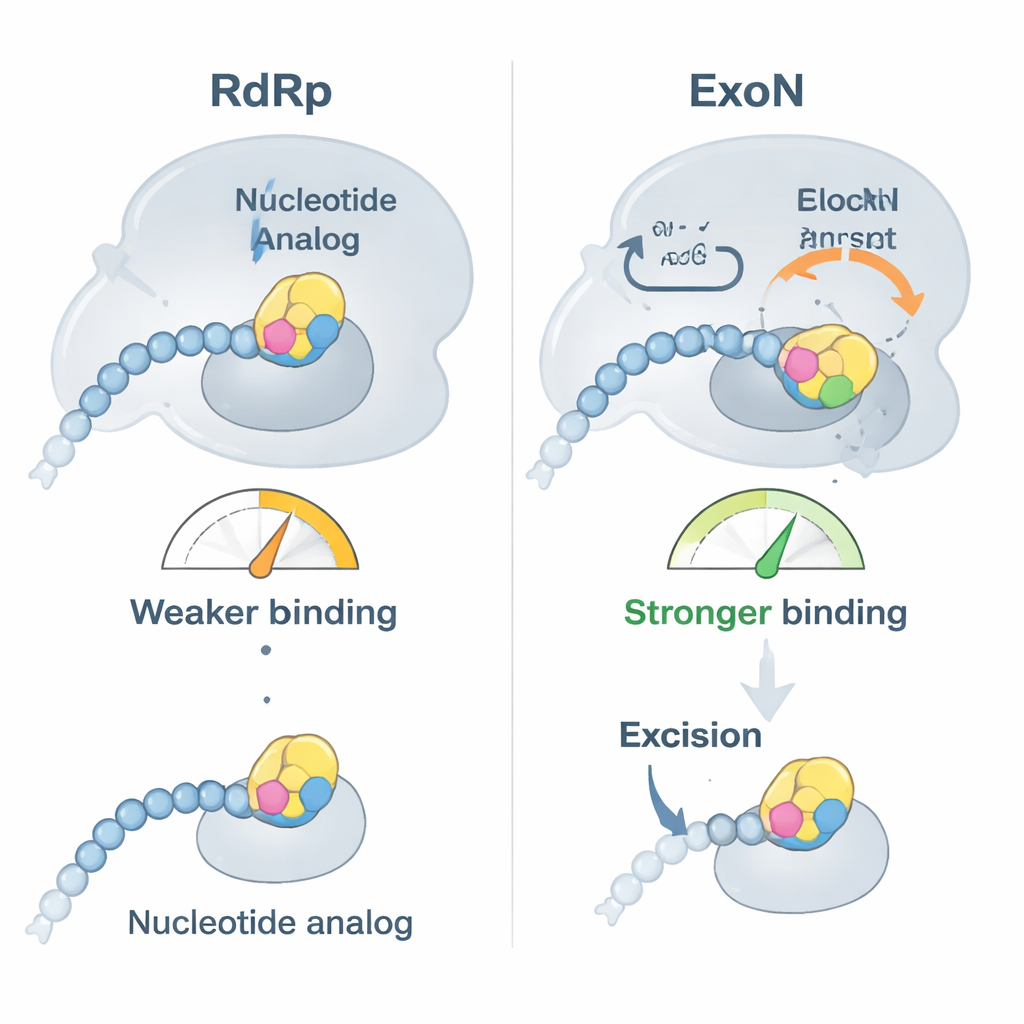
Araştırmacılar, bozuk RNA yapı taşı olarak tasarlanmış klinik açıdan önemli iki antiviral olan bemnifosbuvir ve sofosbuvir üzerine odaklandı. Önce gösterdiler ki SARS‑CoV‑2’nin polimerazı bu analogları RNA zincirinin ucuna kolaylıkla ekliyor ve zincirin uzamasını büyük ölçüde durduruyor; bu amaçlandığı gibidir. Ancak bağlanma testleri ilginç bir dönemeç ortaya koydu: bir analog RNA ucunda durduğunda, RNA artık polimeraza eskisi kadar sıkı bağlanmıyor, bunun yerine ExoN’e daha sıkı bağlanıyor. Etkilenmiş RNA, kopyalama makinesinden uzaklaştırılarak düzeltenin eline veriliyor ve bu da problemli nükleotidin kesilip viral replikasyonun devam etmesine olanak tanıyor.
Durdurulmayan ama Yavaşlatılan Bir Düzeltme
Biyokimyasal zaman kursu deneyleri, ExoN’in bemnifosbuvir ve sofosbuvir’i RNA’dan çıkardığını, ancak normal nükleotidleri çıkarmaya kıyasla daha yavaş yaptığını gösterdi. Hücre dışı reaksiyonlarda her iki analog da daha fazla RNA sentezini güçlü şekilde engelledi—ancak aktif bir ExoN eklendiğinde, duraklamış RNA zincirlerinin önemli bir kısmı kurtarılarak uzatıldı. Etkinliği bozulan bir ExoN mutantı bunu yapamadı; bu da düzeltilme aktivitesinin ilaçların etkisini büyük ölçüde geri alan unsur olduğunu doğruladı. Polimerazın ExoN ile birlikte bulunması, analogların çıkarılmasını hızlandırdı; bu da iki viral enzimin engelleri temizlemek ve replikasyonu sürdürmek için birlikte çalıştığını düşündürüyor.
Atomik Çözünürlükte Düzeltmeni İzlemek
ExoN’in bu ilaçları nasıl tanıyıp yanıt verdiğini anlamak için ekip, bemnifosbuvir veya sofosbuvir ile biten RNA zincirlerine bağlı ExoN kompleksinin yapısını yüksek çözünürlüklü kriyo‑elektron mikroskobisi ile çözdü. Bireysel kimyasal grupları görecek kadar net olan bu yapılar, her iki ilacın modifiye şeker halkasının ExoN proteininin kısa bir döngüsü tarafından oluşturulan hidrofobik bir cebe oturduğunu ortaya koydu. Bu ekstra sıkı uyum, ilaç içeren RNA’nın ExoN’e daha güçlü bağlanmasını açıklar. Ancak bu durum beklenmeyen bir yan etkiye de yol açar: söz konusu döngüyü çekerek, ilaçlar yakınlardaki bir katalitik döngünün hassas düzenini bozuyor ve önemli bir histidin kalıntısını yerinden oynatıyor. Bu histidin kesme sitesinden uzaklaştığında, ExoN’in aktif merkezi kısmen devre dışı kalıyor; böylece analogun çıkarılması yavaşlıyor ama tamamen engellenmiyor.
Viral Düzeltme Aktivitesini Ayarlayan Yerleşik Bir Anahtar
Hassas döngü içindeki tek tek amino asitlerin değiştirilmesi önemini doğruladı. Dört korunan kalıntıda yapılan değişiklikler ExoN’in hem standart RNA uçlarını hem de ilaçla sonlanan uçları kesme yeteneğini büyük ölçüde azalttı ve ExoN’in hangi son nükleotidi çıkarmayı tercih ettiğini de değiştirdi. Bu, döngüyü allosterik bir düzenleyici — RNA ucunda hangi tür nükleotid olduğunu algılayan ve enzimin aktivitesini ayarlayan yerleşik mekanik bir anahtar — olarak tanımlıyor. Yapılar ayrıca ExoN’in farklı bazları (A, U, C veya G) esnek hidrojen bağları aracılığıyla tanıdığını, ancak guanin benzeri bazları daha güç barındırdığını gösteriyor; bu, bemnifosbuvir’in guanozini taklit etmesi nedeniyle önem taşıyor.
Gelecekteki COVID-19 İlaçları İçin Ne Anlama Geliyor
Uzman olmayanlar için temel mesaj şudur: SARS‑CoV‑2, replikasyonu durdurma görevini yaptıktan sonra belirli ilaçları genomundan çekip çıkarabilen sofistike bir "imla denetleyicisine" sahiptir. Bemnifosbuvir ve sofosbuvir virüsün kopyalama makinesini zayıflatsa da, aynı zamanda RNA’yı kısmen etkilerini geri alabilen düzeltmene yönlendirirler. Viral düzeltmenin bu ilaçları nasıl kavradığını ve küçük bir düzenleyici döngünün enzimi aktif ve daha az aktif durumlar arasında nasıl anahtarladığını ortaya koyarak, bu çalışma ya ExoN’e zayıf bağlanan, ya onu inaktif bir konformasyonda kilitleyen ya da guanin benzeri yapıların işlenmesindeki zorluğundan yararlanan yeni antiviral nükleotidler tasarlamak için bir yol haritası sunuyor. Bu tür yeni nesil moleküller virüsün “silmesini” çok daha zorlaştırabilir ve COVID‑19 ile gelecekteki koronavirüs salgınlarının tedavisini iyileştirebilir.
Atıf: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Anahtar kelimeler: SARS-CoV-2, antiviral direnç, nükleotid analogları, RNA düzeltilmesi, koronavirüs replikasyonu