Clear Sky Science · tr
Splicing faktörü geni SF3B1’deki de novo varyantlar nörogelişimsel bozukluklarla ilişkilidir
Bir Gen Beynin Erken Planını Nasıl Bozar
Gebelik ve doğum normal görünse bile bazı çocuklarda neden öğrenme güçlüğü, nöbetler veya beslenme sorunları gelişir? Bu çalışma, hücrelerin genetik mesajları işlemesine yardımcı olan SF3B1 adlı tek bir geni inceliyor. Araştırmacılar, bu gendeki yeni, spontan değişikliklerin beyin hücrelerinin DNA talimatlarını okuma biçimini ince ince karıştırabileceğini ve daha önce tanımlanmamış bir nörogelişimsel sendroma yol açabileceğini gösteriyor.
Genetik Mesajların Usta Editörü
Vücudumuzdaki her hücre, protein üretebilmeden önce ham genetik metni net talimatlara dönüştürmek zorundadır. RNA kesme olarak bilinen bu düzenleme adımı, kodlamayan bölümleri çıkarır ve kullanışlı parçaları birbirine ekler. SF3B1 hücresel “splicing makinesinin” merkezi bir bileşenidir. Bugüne kadar SF3B1’deki değişiklikler çoğunlukla kanserlerde rol oynadığı için bilinmekteydi; tümör hücreleri yaşam boyunca bu gende mutasyonlar edinebiliyordu. Yeni çalışma farklı bir soruyu soruyor: zararlı bir SF3B1 değişikliği konsepsiyondan itibaren vücuttaki her hücrede mevcutsa ne olur?
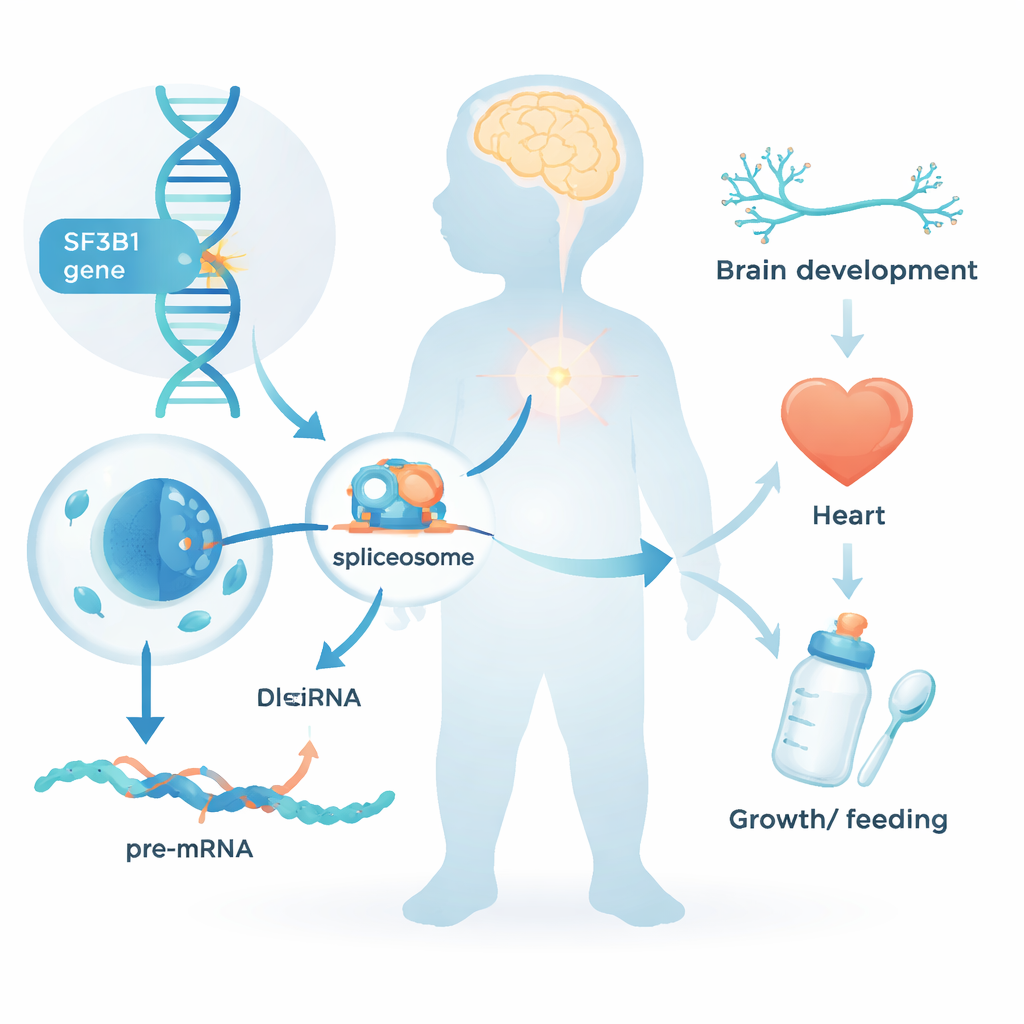
Yeni Tanımlanmış Bir Çocukluk Sendromu
Araştırma ekibi, çoğunluğu de novo yani ebeveynlerden miras alınmamış nadir SF3B1 varyantlarını taşıyan 26 çocuk ve genç erişkinin verilerini topladı. Neredeyse tamamında nörogelişimsel sorunlar vardı: oturma, yürüme veya konuşma öğrenme gecikmeleri; çoğunlukla hafif ila orta derecede entelektüel engel; ve vakaların yaklaşık yarısında nöbetler. Birçok hastada düşük kas tonusu ve bazen mide tüpü ile beslenme gereksinimi de görüldü. Yüz özellikleri çocuktan çocuğa tamamen aynı olmasa da ince farklılıklar gösteriyordu; dikkat çekici ortak özelliklerden biri yüksek veya yarık damaktı. Bazı katılımcılarda kalp kusurları, büyüme geriliği veya küçük kafa çevresi gibi bulgular da vardı; bu da SF3B1 değişikliklerinin yalnızca beyni değil, daha geniş etkileri olduğunu gösteriyor.
İki Tür Genetik Değişiklik, İki Klinik Görünüm
Araştırmacılar SF3B1 varyantlarını iki geniş gruba ayırdı. Bir grup, çalışan SF3B1 protein miktarını azaltması beklenen erken stop işaretleri gibi "fonksiyon kaybı" değişikliklerini içeriyordu. İkinci grup ise proteindeki tek bir aminoasidin değiştiği missense varyantları içeriyordu. Çocukların tıbbi özelliklerini kümelendirerek incelediklerinde, missense varyant taşıyanların daha ciddi ve daha karmaşık sorunlara eğilimli olduğunu; kalp ve gastrointestinal anormalliklerin, kısa boyun ve mikrosefali oranlarının daha yüksek olduğunu gözlemlediler. Öte yandan fonksiyon kaybı varyantları bazen hafif etkilenmiş veya görünürde sağlıklı bir ebeveynden miras alınmıştı; bu da bazı bireylerde SF3B1 miktarının azalmasının göreceli olarak hafif belirtilerle uyumlu olabileceğini düşündürüyor.
Tam Bir Çöküşten Çok İnce Ayar Hataları
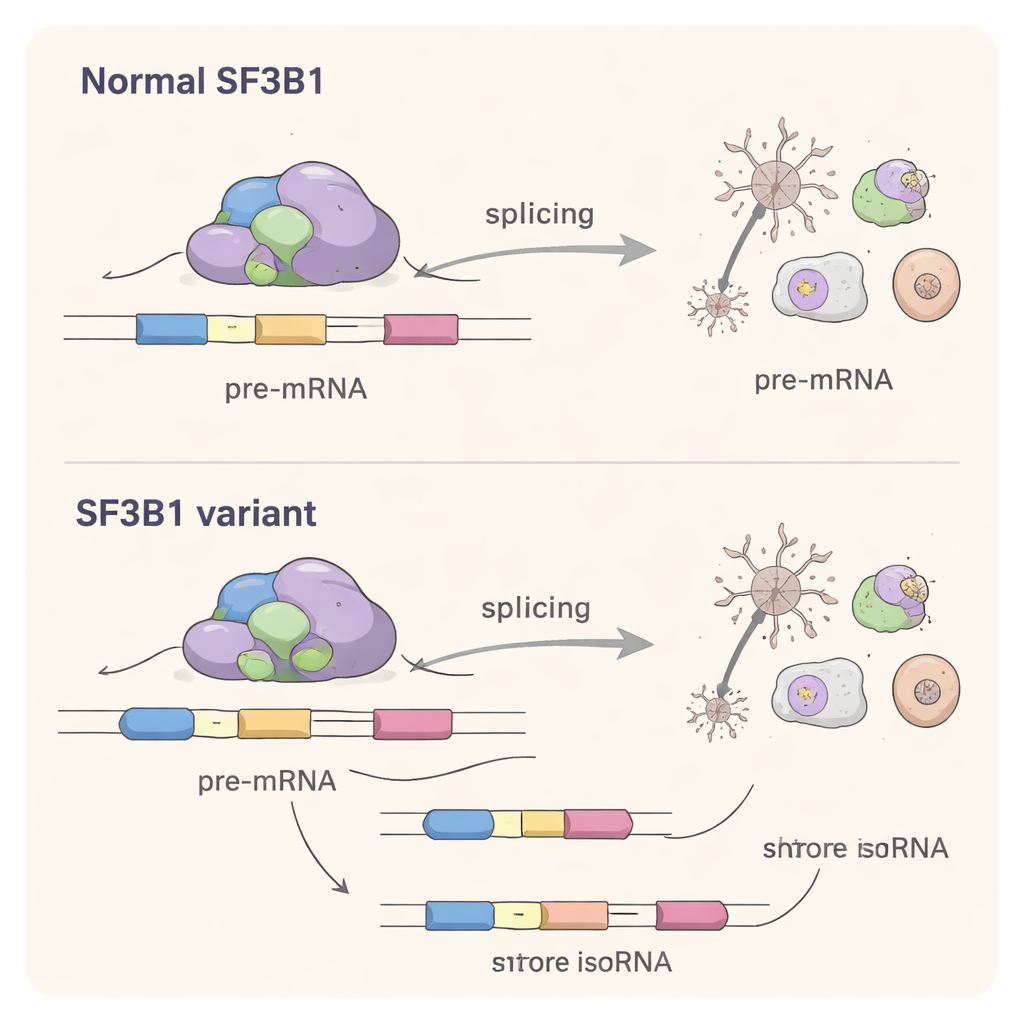
Missense varyantların hücre içindeki etkisini anlamak için bilim insanları bunları laboratuvar hücre hatlarında yeniden oluşturdular. Şaşırtıcı biçimde, değişmiş SF3B1 proteinleri, normal SF3B1 susturulmuş hücreleri kurtarmak için splicing işini yeterince yapabiliyordu. Bu, basit bir fonksiyon kaybı açıklamasını dışladı. Derin RNA dizileme kullanarak ekip ardından hücredeki tüm mesajları inceledi. Missense varyantların, yüzlerce genin kesilme biçimini ince kumanda ile kaydırdığını, özellikle ekzon uçlarında hangi splice site’lerin seçildiğini değiştirdiğini ve ara sıra ekzon atlamaya yol açtığını buldular. Bozulmanın ölçeği, klasik kanserle ilişkili SF3B1 K700E mutasyonunda görülenin altındaydı ama yine de kayda değerdi: etkilenen birçok gen beyin gelişimi, sinir devre oluşumu ve RNA işleme ile protein sentezi gibi temel süreçlerde görev alıyor.
Kanser ile Beyin Bozuklukları Arasında Paylaşılan Bir Mekanizma
Nörogelişimsel SF3B1 varyantlarının çoğu iyi bilinen kanser mutasyonlarından farklı pozisyonlarda meydana gelse de aynı temel süreci bozuyorlar: RNA’da splice site’lerin doğru tanınması. Çalışma, bu gelişimsel varyantların kendi "splicing imzasına" sahip olduğunu; genellikle kanserde tercih edilenlerden daha normale yakın alternatif splice site’leri seçtiklerini gösteriyor. Bu, mutasyona uğramış proteinin normal kopyayla yarıştığı ve splicing mekanizmasını aynı anda birçok gen için hafifçe yanlış tercihlere doğru ittiği bir değişiklik‑fonksiyonu (change‑of‑function) mekanizmasını düşündürüyor.
Bu Aileler ve Gelecek Araştırma İçin Ne Anlama Geliyor
Etkilenen aileler için bu çalışma, artık genetik kliniklerde test edilebilecek yeni bir nörogelişimsel bozukluk nedeni olarak SF3B1’i tanımlıyor; bu, uzun süren tanı aramalarını sonlandırma potansiyeli taşıyor. Daha geniş anlamda, çalışma SF3B1’i hem kanseri hem de çocukluk çağı beyin bozukluklarını tetikleyebilen splicing genlerinin küçük ama büyüyen listesine ekliyor; bunun ne zaman ve nasıl değiştiğine bağlı olarak farklı hastalık tablolarına yol açabiliyor. Belirli SF3B1 varyantlarının RNA kesme biçimini nasıl yeniden şekillendirdiğini haritalayarak, çalışma hedefli yanlış‑kesme düzeltmelerine yönelik gelecekteki terapilere zemin hazırlıyor.
Atıf: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Anahtar kelimeler: RNA kesme, SF3B1, nörogelişimsel bozukluklar, de novo varyantlar, splicesomopatiler