Clear Sky Science · tr
Pulmoner fibrozis tedavisi için viskoelastik hidrojel ile hazırlanmış CAR-makrofaj
Vücudun Temizlik İşçilerini Hassas Onarım Ekiplerine Dönüştürmek
Pulmoner fibrozis, normal, esnek akciğer dokusunun yavaşça sert bir yara dokusuyla yer değiştirdiği yıkıcı bir akciğer hastalığıdır. İnsanlar nefes almakta zorlanır; günümüz ilaçları ise çoğunlukla sadece kötüleşmeyi yavaşlatır. Bu çalışma yeni bir fikri araştırıyor: vücudun kendi temizlik hücreleri olan makrofajları, genetik olarak mühendislik uygulanmış “akıllı temizlikçiler” haline getirmek ve sonra onların gücünü özel olarak tasarlanmış yumuşak bir jel ile artırmak. Birlikte, bu yaklaşımlar hücrelerin yara oluşturan suçluları arayıp bulmalarına ve hasarlı akciğerlerdeki sert dokuyu gevşetmelerine yardımcı oluyor.
İyileşme Zararlı Olduğunda
Sağlıklı akciğerlerde fibroblastlar hava keseciklerini destekleyen ince kollajen ağını korumaya yardım eder. Pulmoner fibroziste bu hücreler aşırı aktif hale gelir ve hava boşluklarını daraltan kalın kollajen iplikleri döşerler. Mevcut ilaçlar bu süreçleri baskılayabilir ama nadiren tersine çevirir. Yazarlar, aşırı aktif fibroblastlarda bol bulunan ancak normal dokuda nadir görülen hücre yüzeyi bir işaretçisi olan fibroblast aktivasyon proteini (FAP) üzerine odaklanıyor. Eğer bağışıklık hücreleri FAP’ı tanıyacak şekilde eğitilebilirse, skarlaşmayı sürdüren “kontrolden çıkmış” fibroblastları seçici olarak ortadan kaldırırken sağlıklı hücreleri koruyabilirler.
Makrofajları Yarıkurucuları Hedef Alacak Şekilde Yeniden Programlamak
Makrofajlar normalde ölü hücreleri, mikrop ve hücresel artıklarını yutan devriye gezen bağışıklık hücreleridir. Araştırma ekibi onları FAP’ı tanıyan kimerik antijen reseptörü (CAR) ile donattı ve böylece CAR‑makrofajlar (CAR‑M) oluşturdu. Laboratuvar ortamında bu CAR‑M’ler FAP açısından zengin fibroblastları verimli şekilde yuttu ve öldürdü; FAP düzeyi düşük hücreleri ise büyük ölçüde görmezden geldi. Ayrıca modifiye edilmemiş makrofajlara kıyasla kollajen açısından zengin jelleri daha güçlü biçimde parçaladılar; bu da iki yönlü bir fayda öneriyor: skar oluşturan hücreleri ortadan kaldırmak ve doğrudan skar matriksini parçalamak. Bu etkiler hem standart hücre dizilerinde hem de dokulardaki gerçek duruma daha yakın olan primer fare makrofajlarında gözlendi. 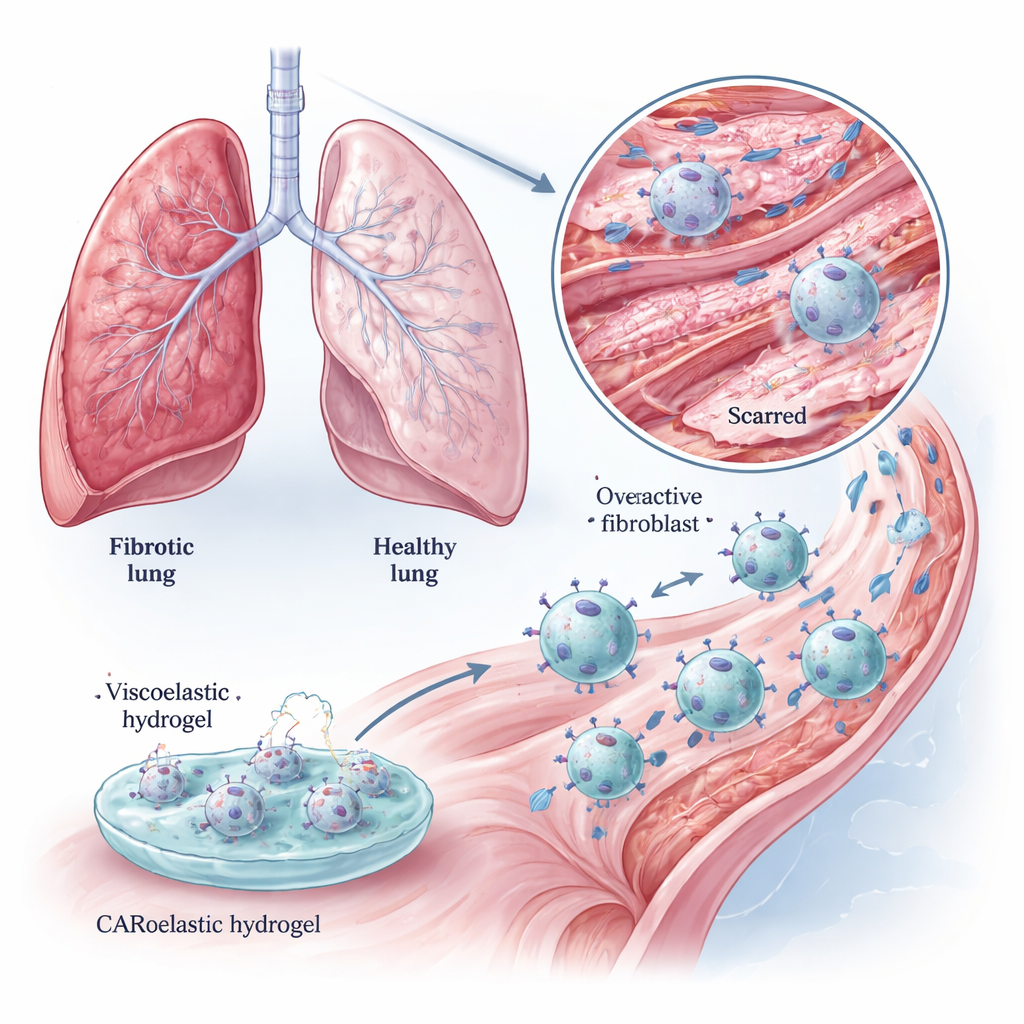
Bağışıklık Hücrelerini Yumuşak, Viskoelastik Bir Jel ile Hazırlamak
Hücreleri genetik olarak değiştirmek güçlü ama karmaşıktır. Araştırmacılar bu yüzden salt fiziksel bir uyarının —yumuşak, viskoelastik bir hidrojelin— CAR‑M davranışını daha da ayarlayıp ayarlamayacağını sordular. Jelatin–alginat bazlı bir hidrojel geliştirdiler; bu jelin “kayıp modülü”, gerilim altında nasıl yavaşça gevşediğini ölçen parametre, genel sertlik değişmeden hassas biçimde ayarlanabiliyordu. CAR‑M’ler doğru viskoelastisiteye sahip jellerde kısa süre kültüre edildiğinde, hedef fibroblastları öldürme yetenekleri yaygın kimyasal uyarıcılardan daha fazla arttı ve bu artış en az iki gün sürdü. Bu “Gel‑CAR‑M”ler aynı zamanda bağışıklık aktivasyonu ve doku yeniden şekillenmesiyle ilişkili genleri açarken, fibrozisle ilişkilendirilen genleri kapattılar; bu durum jelde geçirilen deneyimin hücrelere daha anti‑skar bir kimlik olarak iz bıraktığını düşündürüyor.
Daha Yumuşak Bir Yüzey Hücre Davranışını Nasıl Yeniden Kabloluyor
Jelin neden önemli olduğunu anlamak için ekip CAR reseptörlerinin hücre yüzeyindeki fiziksel durumunu inceledi. Floresan bir prob, hidrojel ile hazırlanmış CAR‑M’lerin membran geriliminin daha düşük olduğunu —hücrenin dış katmanının daha gevşek olduğunu— gösterdi. Bu koşullar altında CAR molekülleri sıkı kümelerden yayılıp daha izole tek birimler ve çiftler hâline geldi. Biyokimyasal testler, bu dağılmış reseptörlerin içsel sinyal tetiklemeyi daha kolay başlatan formları tercih ettiğini ve özellikle aktivasyon ve öldürme kapasitesini kontrol eden ERK gibi yolakları etkinleştirdiğini gösterdi. Membran gerilimindeki düşüşü küçük bir molekül ile taklit etmek, aynı reseptör yayılmasını ve geliştirilmiş hedef hücre öldürmesini yeniden üretti; bu da membranın mekanik rahatlamasının hücreleri hedefleriyle hiç karşılaşmadan önce “ön‑hazırlayabileceği” fikrini destekliyor. 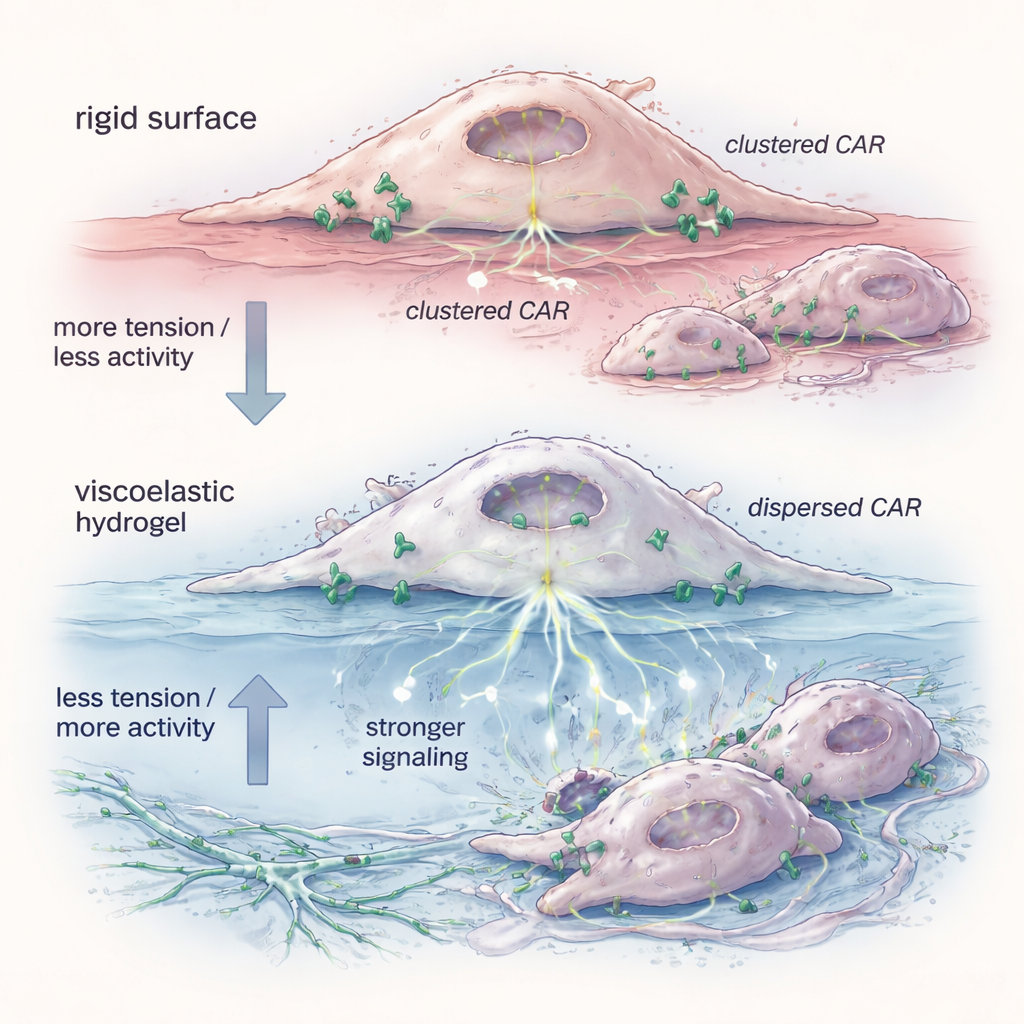
Farelerde Yara İlişmiş Akciğerleri Onarmak
Nihai test, ilaç kaynaklı pulmoner fibrozis fare modeli oldu. Deneklere sıradan makrofajlar, standart CAR‑M’ler veya hidrojel ile hazırlanmış Gel‑CAR‑M’ler verildi. Tedavi edilen tüm fareler tedavi edilmemiş kontrollere göre iyileşti, ancak Gel‑CAR‑M’ler en iyi performansı gösterdi: akciğerlerinde daha az kollajen, daha normal hava boşlukları ve daha az FAP‑pozitif fibroblast vardı. Akciğer dokusundan alınan gen ifadeleri, Gel‑CAR‑M’lerin enflamatuar sinyalleri yatıştırdığını ve skar ilişkili genlerin ekspresyonunu standart CAR‑M’lerden daha etkili şekilde azalttığını gösterdi. İzlenen hücreler akciğerde en az bir hafta varlığını sürdürdü ve 12 haftaya kadar uzatılmış güvenlik kontrollerinde önemli organ hasarı, kan anomalileri veya otoimmünite belirtileri bulunmadı.
Hücre Tabanlı Anti‑Fibrozis Terapilerinde Yeni Bir Yön
Uzman olmayanlar için kilit mesaj şudur: hedefe yönelik hücre mühendisliği ile akıllı materyallerin birleşimi, doğal bağışıklık hücrelerini son derece etkili fakat genetik olarak aşırı karmaşık olmayan yara‑savaşçı araçlara dönüştürebilir. Mühendislik uygulanmış makrofajları kısa bir süre dikkatle ayarlanmış yumuşak bir jel üzerinde dinlendirerek araştırmacılar, yüzey reseptörlerini mekanik olarak daha yanıt verici bir moda “önayarladılar”. Akciğer fibrozisi olan farelerde bu, zararlı fibroblastların daha iyi uzaklaştırılması, fazla kollajenin parçalanması ve normal akciğer yapısının kısmi olarak geri kazanılması ile sonuçlandı — belirgin güvenlik sorunları olmadan. İnsan denemelerine ulaşmadan önce hâlâ yapılması gereken çok iş olmakla birlikte, bu strateji terapötik hücrelerin fiziksel ortamının ince ayarının bir gün fibrotik akciğer hastalığı tedavilerini daha güçlü ve daha kesin hale getirebileceğini öne sürüyor.
Atıf: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Anahtar kelimeler: pulmoner fibrozis, CAR makrofaj terapisi, viskoelastik hidrojel, fibroblast aktivasyon proteini, hücre mekanobiyolojisi