Clear Sky Science · tr
Yeni DNA metilasyonunun TCL1A tarafından inhibisyonunun moleküler temeli
Hücreler Nehatırlayacaklarına Nasıl Karar Verir?
Vücudunuzdaki her hücre temelde aynı DNA’yı taşır, ama sinir hücreleri, kan hücreleri ve deri hücreleri çok farklı davranır. Hücrelerin kimliklerini “hatırlamalarına” yardımcı olan yollardan biri DNA’ya eklenen kimyasal işaretlerdir; buna DNA metilasyonu denir. Bu çalışma, küçük bir protein olan TCL1A’nın bu metil işaretlerini yazan enzimleri nasıl kapattığını atomik ayrıntıda ortaya koyuyor. Hem DNA metilasyonu hem de TCL1A kanserler ve üreme bozukluklarıyla ilişkili olduğundan, bu moleküler çekişmenin anlaşılması sonunda yeni tedavilere ilham verebilir.
Hücrenin DNA İşaretleme Makineleri
DNA metilasyonu, genomun kenarına çizilmiş bir kurşun kalem işareti gibi çalışarak bazı genleri susturmaya ve hücreler gelişirken genomu kararlı tutmaya yardımcı olur. DNMT3A ve DNMT3B adındaki iki enzim, erken gelişimde ve kök hücrelerin özelleşmesi sırasında yeni metil etiketlerini yerleştiren başlıca “yazıcılar”dır. Bu enzimler mutasyona uğrar veya yanlış düzenlenirse DNA üzerindeki işaretlerin düzeni bozulabilir ve bu durum gelişim sendromlarına ve kan hastalıklarına katkıda bulunabilir. TCL1A, bağışıklık hücresi kanserlerinde sıkça aşırı üretilmesiyle tanınan bir proteindir. Önceki çalışmalar TCL1A’nın DNMT3A ve DNMT3B’ye bağlanıp onların aktivitesini azaltabileceğini düşündürmüştü, ama bunu tam olarak nasıl yaptığı bilinmiyordu.
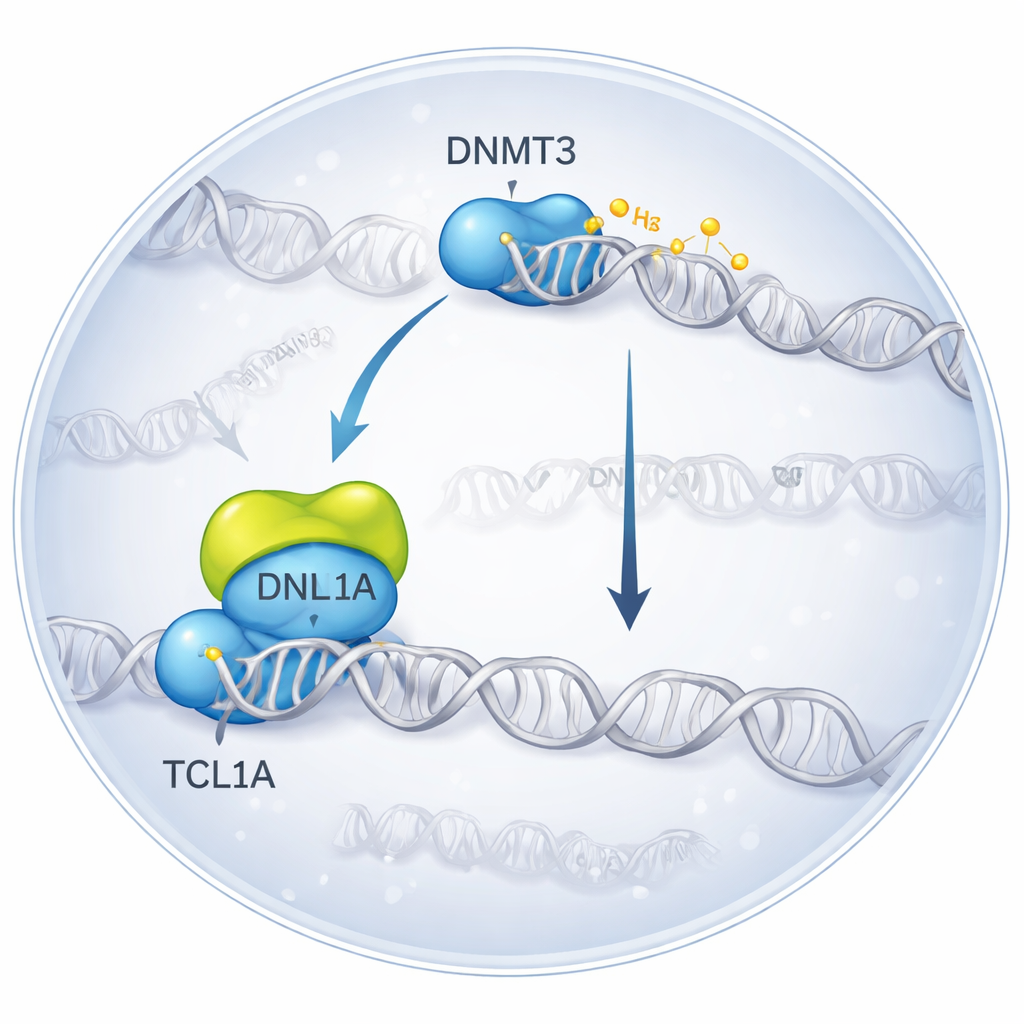
3B’de Moleküler Bir Karşılaşmayı Dondurmak
Araştırmacılar, DNMT3A’nın TCL1A’ya bağlandığı kompleksin görüntüsünü elde etmek için molekülleri şok‑hızlı dondurarak görüntüleyen kriyo‑elektron mikroskopisini kullandılar. İki DNMT3A molekülünün eşleştiğini ve her iki tarafta bir TCL1A dimerinin DNMT3A’nın katalitik bölümüne tutunduğunu buldular—bu bölüm normalde yardımcı proteinler ve DNA ile etkileşen bölgedir. Bu bağlanma yüzeyi, DNMT3A’nın aktivitesini artıran diğer bir ortak partner olan DNMT3L’nin bağlandığı noktayla örtüşüyor. Biyokimyasal testlerde TCL1A eklenmesi, DNMT3L varlığında bile DNMT3A ve DNMT3B’nin DNA’yı metilleme yeteneğini keskin biçimde azalttı; bu da yapısal kompleksin güçlü şekilde inhibe edilmiş bir duruma karşılık geldiğini doğruladı.
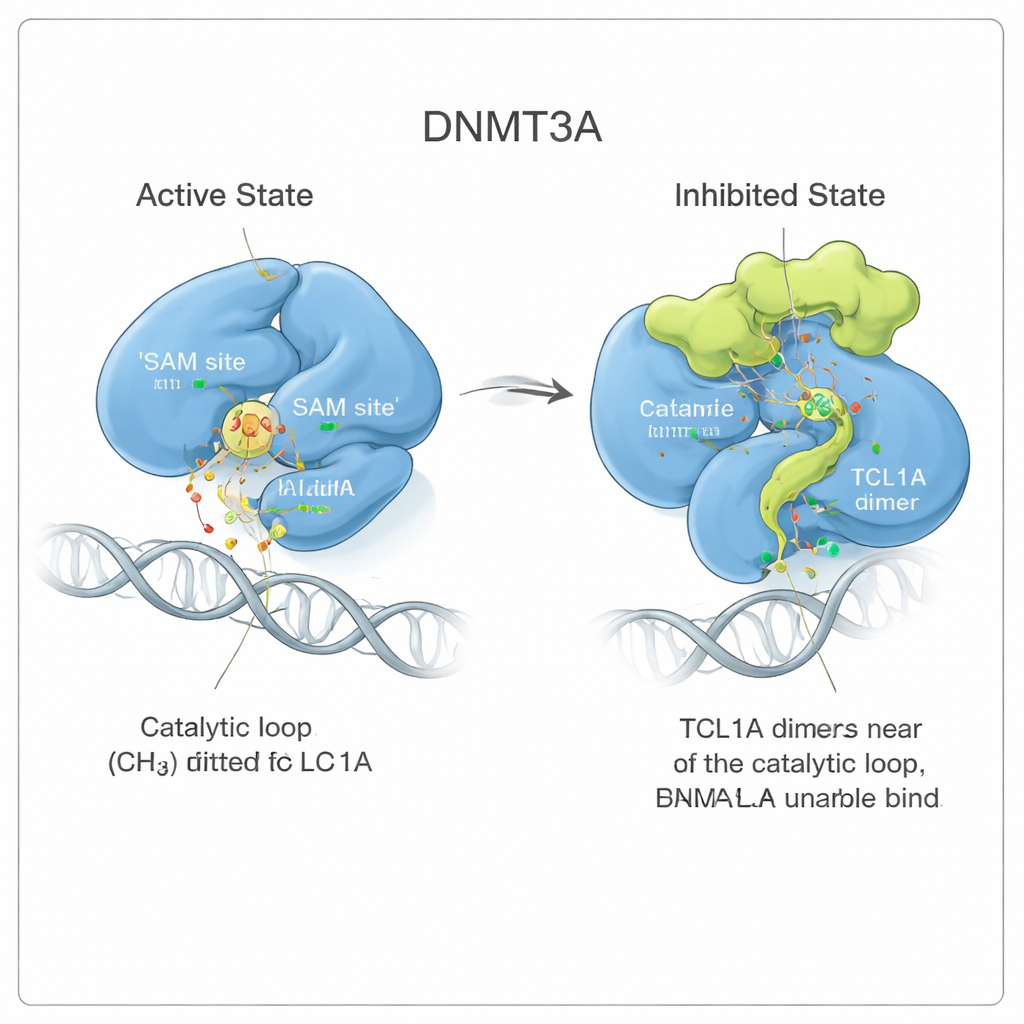
Enzimi Tıkayan Bir Şekil Değişimi
Daha yakından bakıldığında, ekip TCL1A bağlanmasının aktif sitin üzerine bir kapak gibi basitçe oturmadığını gördü. Bunun yerine, DNMT3A’nın şeklinde ince ama geniş kapsamlı bir değişikliği tetikliyor. Enzimin hedef‑tanıma halkası ve katalitik halka olarak bilinen iki esnek bölgesi, DNMT3A DNA’ya bağlıyken işgal ettikleri pozisyonlardan uzaklaşıyor. Aktif formda bu halkalar DNA’ya yaslanır ve metil grubunu bağışlayan küçük molekül yakıt SAM için bir cep oluştururlar. TCL1A bağlandığında katalitik halka SAM cebine katlanarak onu bloke ediyor ve aynı zamanda DNA’nın enzime ulaşmasını zorlaştırıyor. Bağlanma ölçümleri, TCL1A ile eşleşmiş DNMT3A’nın artık DNA’ya veya SAM’a anlamlı şekilde tutunamadığını doğruladı.
Hareket Halinde Dinamik Bir Tıkanmayı İzlemek
Bu inhibe olmuş konformasyonun ne kadar kararlı olduğunu anlamak için yazarlar uzun moleküler dinamik simülasyonları çalıştırdılar; bunlar çözeltideki moleküllerin fizik‑temelli filmleri gibidir. DNMT3A aktivatörü DNMT3L’ye bağlıyken katalitik halka aktif pozisyonunda sabit kaldı. TCL1A varlığında ise o halka çok daha hareketli hale geldi, sallanıyor ama tekrarlayan biçimde SAM cebini işgal ederek bir süzgeci tıkayan deniz otu gibi davranıyordu. Bu sürekli hareket SAM için mevcut alanı ondan fazla on kat daralttı; bu da TCL1A’nın DNMT3A’nın doğal esnekliğini kullanarak katı bir engelleme yerine dinamik bir inhibisyon biçimi dayattığı modelini destekliyor.
Gelişen Hücreler ve Hastalıklar Üzerine Sonuçları
Araştırmacılar daha sonra bu moleküler engellemenin gerçek hücreler için ne anlama geldiğini sordular. Fare embriyonik kök hücrelerini, hücrelerin farklılaşmaya başlarken normalde DNA metilasyonunu artırdıkları bir evrede insan TCL1A üretecek şekilde mühendislik ettiler. Genom çapında metilasyon haritalama, TCL1A’yı fazla eksprese eden hücrelerin olağan yüksek DNA metilasyon seviyesini elde edemediğini ve bunun Dnmt3a ile Dnmt3b genlerinin her ikisinin yok edildiği hücrelere çok benzediğini gösterdi. DNMT3 enzimlerine zayıf bağlanan mutant bir TCL1A versiyonu ise az etki yaptı; bu da fiziksel etkileşimin kilit olduğunu vurguladı. Bu bulgular yapısal mekanizmayı genom genelinde geniş epigenetik değişikliklerle ilişkilendiriyor.
Sağlık Açısından Anlamı
Bir arada ele alındığında bu çalışma, TCL1A’nın yeni DNA metilasyonu işaretlerini yerleştiren enzimler üzerinde nasıl güçlü bir fren işlevi görebileceğini ortaya koyuyor. Kritik bir ara yüze tutunarak TCL1A, DNMT3A ve DNMT3B’deki esnek halkaları yeniden konumlandırıyor; böylece bu halkalar artık DNA şablonuna veya kimyasal yakıta bağlanamıyor ve hücrelerde tümsel bir metil etiket kaybı ortaya çıkıyor. Normal gelişimde bu tür hassas kontrol, metilasyonun ne zaman ve nerede ekleneceğini dengelemeye yardımcı olabilir. TCL1A yanlış yere konumlandığında veya aşırı üretildiğinde—bazı kan kanserleri ve nadir üreme bozukluklarında görüldüğü gibi—aynı mekanizma hücrenin epigenetik programını bozabilir. Bu etkileşimin atomik çözünürlükte anlaşılması, TCL1A’nın etkilerini taklit eden veya tersine çeviren moleküller tasarlama yolunu açarak sağlıklı DNA metilasyon paternlerinin geri kazanılmasını potansiyel olarak sağlayabilir.
Atıf: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Anahtar kelimeler: DNA metilasyonu, DNMT3A, TCL1A, epigenetik, kanser