Clear Sky Science · tr
Protein X-ışın kristallografisi için örnek teslim yöntemleri: örnek tüketimine özel bir odak
Hareket Halindeki Molekülleri İzlemek
X-ışını kristallografisi, yaşamı çalıştıran küçük makineler olan proteinlerdeki atom düzenini görmeyi sağlar. Seri kristallografi adı verilen daha yeni bir yaklaşım bir adım öteye gider: ilaç işleyen enzimler veya fotosentetik proteinlerin suyu bölmesi gibi proteinlerin “moleküler filmlerini” yakalayabilir. Ancak bir sorun var. Birçok önemli proteinin üretilmesi ve kristalleştirilmesi zordur ve mevcut deneyler değerli materyali miligramlardan gramlara kadar tüketebilir. Bu derleme makalesi aldatıcı derecede basit bir soruyu sorar: kristalleri güçlü X-ışını ışınlarına mümkün olduğunca az atıkla nasıl teslim edebiliriz?
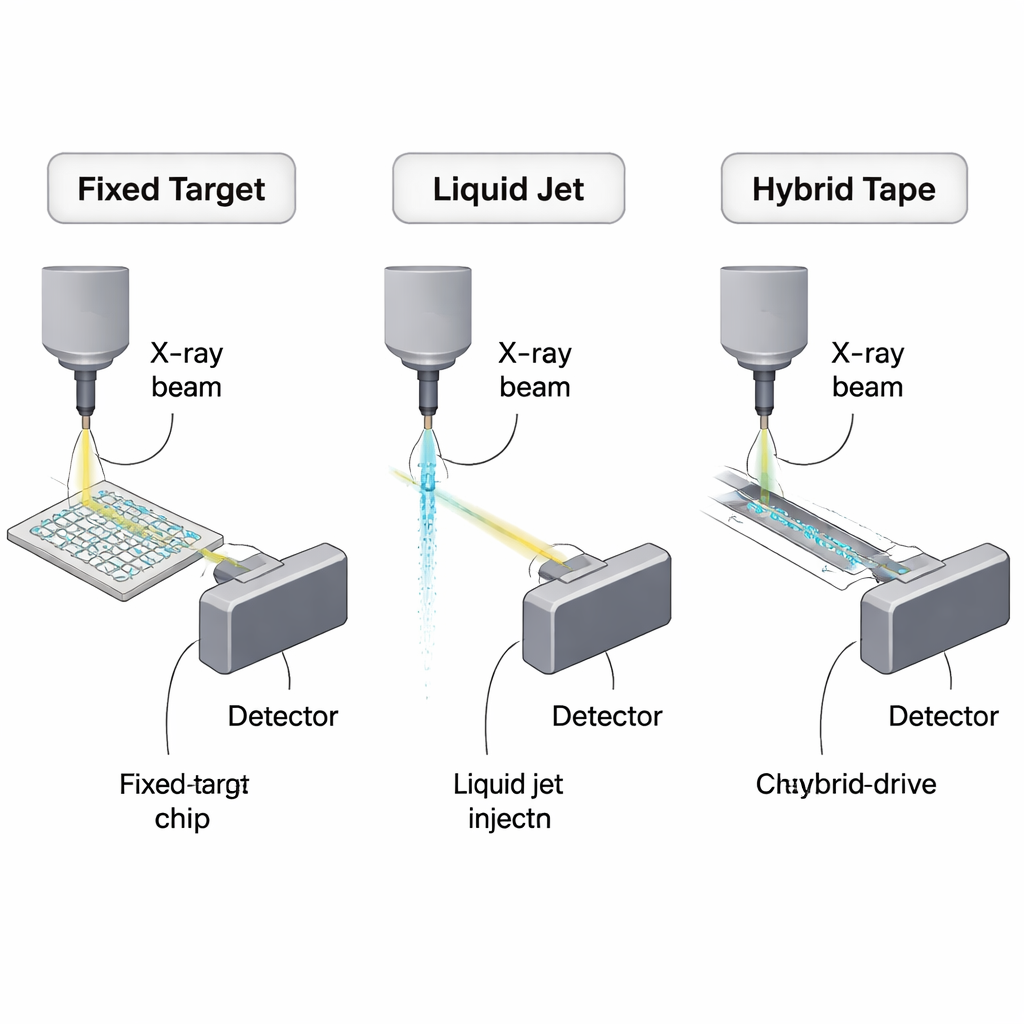
Seri Kristallografinin Daha İyi Teslimata İhtiyacı Neden Var
Geleneksel kristallografi, bir X-ışını demetinde döndürülen tek bir büyük kristale dayanıyordu. Seri kristallografi ise sahneyi tersine çevirir: bir büyük kristal yerine, her biri yalnızca bir kez kullanılan binlerce mikrokristal, sinkrotronlardan veya X-ışını serbest elektron lazerlerinden (XFEL) gelen ultraparlak X-ışını darbeleriyle taranır veya atılır. Bu, oda sıcaklığında veri toplama ve kimyasal reaksiyonların hızlı “anlık görüntülerini” mümkün kılar, ama aynı zamanda X-ışını darbe dizilerine yetişecek hızlarda sürekli kristal yenilenmesi gerektirir; bu diziler saniyede milyonlara ulaşabilir. Kristal süspansiyonunun büyük kısmı aslında ışınla hiç karşılaşmaz ve atılır; bu yüzden örnek tüketimini azaltmak alan için merkezi teknik ve ekonomik bir meydan okuma haline gelmiştir.
Sabit Hedefler: Her Damlayı Uzatan Minik Yongalar
Temel stratejilerden biri mikrokristalleri sabit hedefler adı verilen küçük katı destekler üzerine tutturmaktır. Kristalleri ışının yanından püskürtmek yerine, araştırmacılar bunları silikon veya polimer yongalar üzerinde diziler halinde yerleştirir ve her kristalin X-ışını odağına bir kez gelmesi için yongayı hareket ettirir. En iyi senaryoda, bir model protein için yaklaşık 10.000 mikrokristalin prensipte yalnızca yaklaşık 450 nanogram protein kullanarak eksiksiz bir veri seti sağlayabileceği düşünülür. Gerçek cihazlar henüz bu kadar tutumlu olmasa da, ihtiyaçları onlarca mikrograma ila birkaç onda bir miligrama kadar düşürerek—erken seri deneylere kıyasla katlarca daha iyi—özellikle etkili olurlar. Derleme, silikon ağlar, ultra ince polimer filmler ve çok katmanlı plastik yongaları karşılaştırır; düşük arka plan saçılımı, yonga üzerinde kristal büyümesi ve oda sıcaklığı çalışmalarıyla uyumluluk gibi güçlü yönlerini, kuruma, yonga malzemesinden kaynaklanan istenmeyen saçılım ve manuel pipetlemeden kaynaklanan ekstra “ölü hacim” gibi pratik sorunlarla tartar.
Sıvı Jetler ve Viskoz Akımlar: Hızlı ama Çok Tüketen
Başka bir yöntem ailesi kristalleri sıvı içinde askıda tutar ve onları sürekli olarak ışının önünden geçirir. Gaz-dinamik sanal memeler, hızlı XFEL darbe dizilerine ayak uydurabilen saç teli inceliğinde jetler yaratır; bunlar zaman çözünürlüklü çalışmalar ve karışım-entegrasyon (mix-and-inject) deneyleri için başlıca araçlardır, çünkü reaksiyonlar maruz kalmadan hemen önce hızlı karıştırma ile tetiklenebilir. Ancak jetler sürekli çalıştıkları için akışın çoğu hiçbir zaman bir X-ışını darbesiyle kesişmez. Titiz ayarlamalarla bile, pratik deneyler teorik minimumdan çok daha fazla protein tüketir—genellikle yoğun kristal süspansiyonunun onlarca ila yüzlerce mikrolitresi. Bu yükü hafifletmek için araştırmacılar daha verimli tasarımlar geliştirmiştir: kristal akışını fedakâr bir sıvıyla sarmalayan çift akışlı memeler, daha düşük akış hızlarında çalışan elektro-örme “MESH” enjektörleri ve jel veya lipidik kübik fazlara gömülü kristalleri mikrolitre/dakika veya daha yavaş hızlarda iten yüksek viskoziteli ekstrüderler gibi. Bu viskoz yöntemler kırılgan membran proteinleri ve sinkrotronlarda oda sıcaklığı çalışmaları için özellikle değerlidir, ancak daha kalın akışları arka plan saçılımını artırır ve en hızlı X-ışını kaynakları için daha az uygundur.
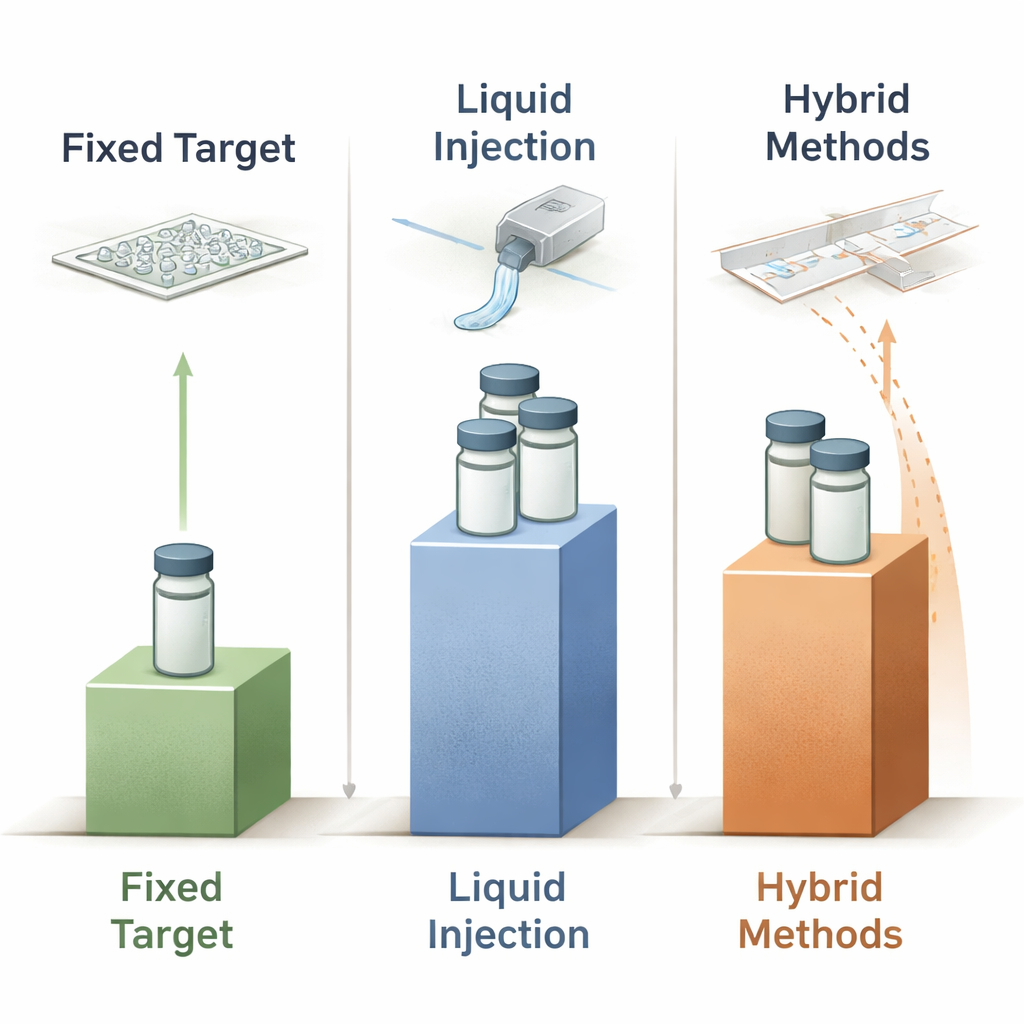
Damla, Bant ve Hibritler: Darbeleri Tek Tek Eşleştirmek
Üçüncü ve giderek daha yaratıcı olan sınıf “hibrit” yaklaşımlar katı destekleri kontrollü sıvı veya damla teslimiyle birleştirir. Örneğin bant-sürücü (tape-drive) sistemleri, hareket eden bir polimer film üzerine damlalar veya ince sıvı şeritleri bırakır; film ışından geçerken hareketin zamanlaması reaksiyon adımlarını veya gaz maruziyetini belirli gecikmelerde incelemeyi sağlar. İhtiyaca göre damla (drop-on-demand) sistemleri daha ileri giderek, akustik veya piezoelektrik cihazlar kullanarak yalnızca bir X-ışını darbesinin beklendiği anda nanolitre veya hatta pikolitre damlacıklar püskürtür ve atığı dramatik şekilde azaltır. Bazı tasarımlar, bant üzerindeki daha önceden yerleştirilmiş kristal içeren damlaya ışına ulaşmadan hemen önce bir ligand damlası karıştırarak zaman çözünürlüklü enzimolojiye dikkatle paylandırılmış reaktiflerle olanak tanır. LAMA gibi bazı hibritler ise yonga üzerine önceden monte edilmiş kristallere doğrudan küçük substrat damlacıkları ekler. Bu tasarımlar arasında bildirilen protein kullanımı geniş bir aralık gösterir—yaklaşık miligram düzeylerinden tam zaman çözünürlüklü seriler için birkaç miligrama kadar—damlalar, kristaller ve X-ışını darbelerinin senkronizasyonundaki mühendislik zorluklarıyla birlikte hem vaatleri hem de mevcut sınırlamaları yansıtır.
Teorik Norma Ne Kadar Yakınız?
Sabit hedefler, sıvı enjektörler ve hibrit sistemler arasındaki düzinelerce yayımlanmış deneyi karşılaştırarak yazarlar, mevcut hiçbir yöntemin ideal 450 nanogram kriterine yaklaşmadığını; en iyi cihazların bile kabaca iki mertebe daha fazla kullandığını gösterir. Yine de belirgin eğilimler ortaya çıkar. Sabit hedefler tipik olarak en az proteini kullanır ve zaman çözünürlüklü karıştırmanın gerekli olmadığı veya yonga üzerinde tasarlanabileceği durumlarda caziptir. Sıvı jetler hâlâ en talepkâr zaman çözünürlüklü XFEL çalışmalarına hakimdir, ancak özellikle çok sayıda zaman noktasına ihtiyaç duyulduğunda örnek açısından yoğun kalır. Hibrit damla ve bant düzenleri, özellikle damla zamanlaması X-ışını kaynağıyla sıkı şekilde senkronize edildiğinde göreli tasarruflar sunar. Geleceğe bakıldığında makale, ilerlemenin daha iyi mikroakışkan kontrolünden, israf yaratan işlem adımlarını ortadan kaldıracak otomasyondan ve deneyleri ve teslimat sistemlerini birlikte tasarlamak için kompakt X-ışını kaynakları ile veri odaklı optimizasyondan geleceğini savunur; böylece protein kullanımı teorik sınıra doğru daha da yaklaşacaktır.
Atıf: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Anahtar kelimeler: seri kristallografi, protein X-ışın kristallografisi, örnek teslimi, X-ışını serbest elektron lazeri, mikroakışkanlar