Clear Sky Science · tr
RAD23A azaltımı, TDP-43 proteinopatisi fare modelinde yaşam süresini uzatır ve patolojiyi hafifletir
Bu araştırma aileler ve hastalar için neden önemli
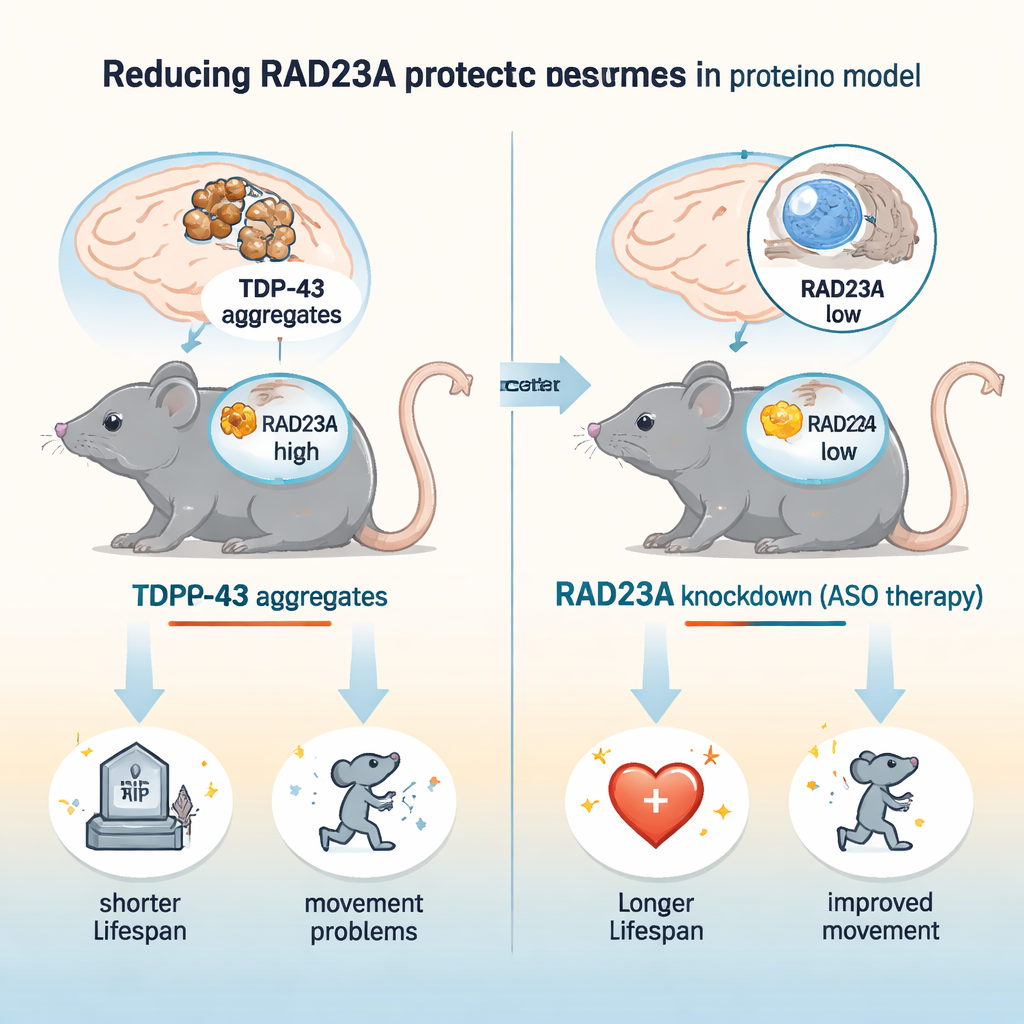
Amiyotrofik lateral skleroz (ALS) ve frontotemporal demans (FTD) dahil birçok demans ve motor nöron hastalığı, beyin hücrelerindeki proteinlerin yanlış katlanması, birleşmesi ve yavaşça nöronları zehirlemesiyle ilişkilidir. Temel suçlulardan biri, normalde RNA yönetimine yardımcı olan ancak agregatlaştığında toksik hâle gelen TDP-43 adlı bir proteindir. Bu çalışma umut verici bir soruyu gündeme getiriyor: hasarlı proteinlerin nasıl işlendiğini kontrol etmeye yardımcı olan başka bir protein olan RAD23A’yı azaltarak beyin hücrelerini daha dirençli hâle getirebilir miyiz? Yazarlar, farelerde RAD23A düzeylerini düşürmenin yaşamı uzatabildiğini, hareketi iyileştirdiğini ve TDP-43 kaynaklı bir modelde beyin hasarını azalttığını göstererek yeni bir tedavi stratejisi olasılığını işaret ediyor.
Hastalıklı nöronlarda protein trafiğinde tıkanma
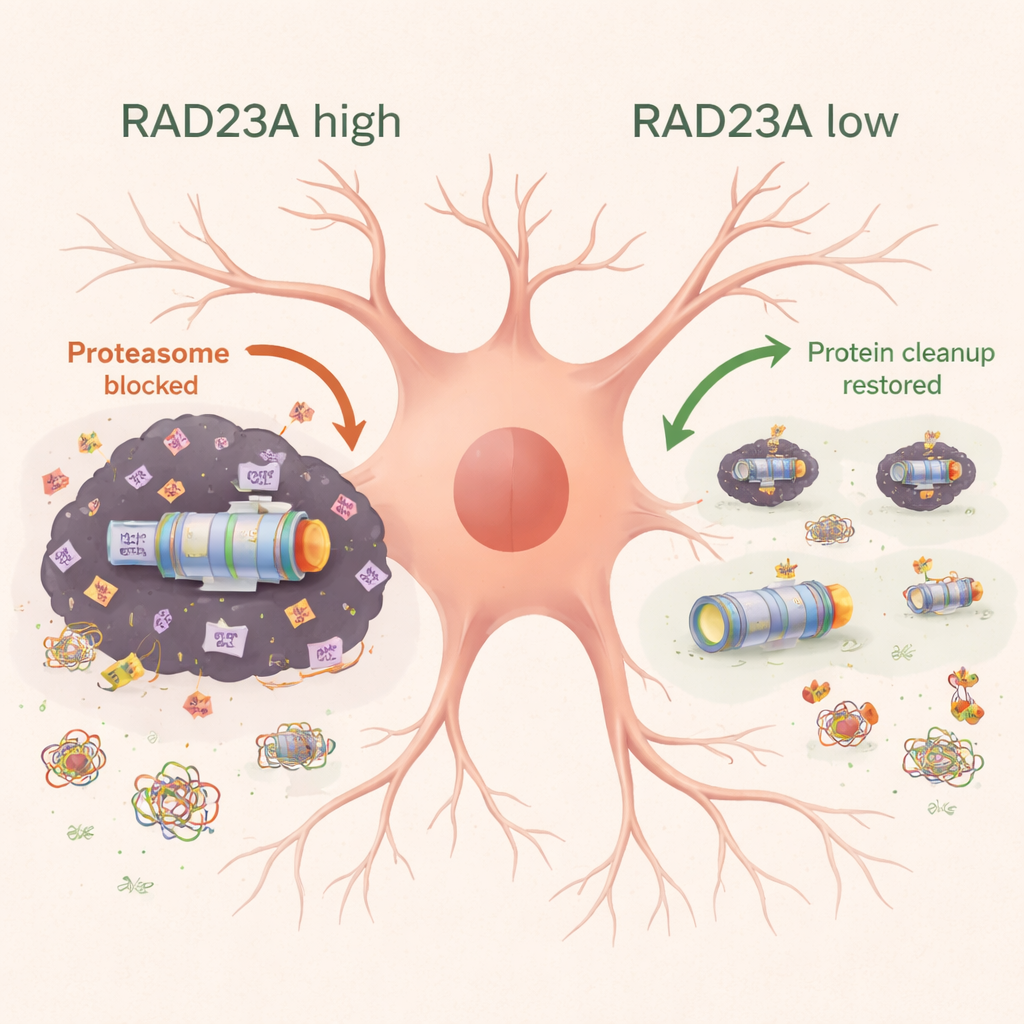
Nörodejeneratif hastalıklar genellikle hücrenin atık-bertaraf mekanizmasının temizleyemediği yanlış katlanmış protein yığınlarıyla belirgindir. ALS ve FTD’de TDP-43 çekirdekten çıkar, yapışkan kümeler oluşturur ve genellikle proteinleri hücrenin ana öğütücüsü olan proteazoma yönlendiren ubiquitin ile yoğun şekilde işaretlenir. RAD23A, ubiquitin işaretli yükü proteazoma taşıyabilen birkaç “taşıyıcı” proteinden biridir. Ancak kurtçuk ve kültürdeki nöronlar üzerinde yapılan önceki çalışmalar, RAD23 benzeri proteinlerin kaybının aslında TDP-43 kaynaklı hasara karşı koruma sağlayabileceğini öne sürmüştü; bu paradoksu canlı memeli beyininde keşfetmeyi amaçlayan çalışma budur.
TDP-43 fare modelinde RAD23A’yı azaltmak
Araştırmacılar, nöronlarda insan TDP-43’ü aşırı üreten ve hareket bozuklukları, omurga eğriliği, tremor ve erken ölüm geliştiren TAR4/4 adlı yerleşik bir fare modelini kullandılar; bu, ALS/FTD’nin temel özelliklerini yansıtır. RAD23A’yı iki yolla azalttılar: yenidoğan farelere Rad23a RNA’sını azaltan antisens oligonükleotidler (ASO’lar) enjekte ederek ve Rad23a geninin tamamen ortadan kaldırıldığı genetik yok etme hattı ile çiftleştirerek. Tek bir ASO tedavisi beyin ve omurilikte RAD23A düzeylerini yaklaşık dörtte üç oranında düşürdü. Bu TDP-43 farelerinde RAD23A düşürülmesi yaşam süresini yaklaşık %50 uzattı ve yürüyüş bozuklukları, tremor, omurga eğriliği ve arka ayak kavrama davranışının başlangıcını ve şiddetini geciktirdi. İlginç olarak, RAD23A’nın tam genetik kaybı ek bir fayda sağlamadı; bu da kısmi azaltmanın optimal olduğunu ve uzun vadede tam yokluğun kompansatuvar değişiklikleri tetikleyebileceğini düşündürüyor.
Daha az inflamasyon, daha temiz protein yönetimi ve daha sakin bir genom
Motor korteksin mikroskobik incelemesi, TDP-43 farelerinde nöron kaybı ve astroglia ile mikroglianın güçlü aktivasyonu olduğunu gösterdi; bunlar beynin destek ve bağışıklık hücreleridir. RAD23A’yı azaltmak nöron sayısını korudu ve inflamasyon ile hücre ölümü belirteçlerini azalttı. Biyokimyasal analizler, TDP-43 aşırı üretiminin hücreleri ubiquitin işaretli, deterjanla çözünmeyen proteinlerle doldurduğunu ve proteazom altbirimlerini bu agregatlara çekerek hücrenin hasarlı proteinleri temizleme yeteneğini zayıflattığını ortaya koydu. RAD23A’yı azaltmak toplam ubiquitinli protein yükünü düşürdü, daha fazla proteazomun çözünür, çalışan havuzda kalmasını sağladı ve birkaç proteazom aktivitesini normale doğru geri getirdi. Aynı zamanda, RAD23A düşürülmesi hem toplam hem de agregatlaşmış TDP-43 formlarını, özellikle toksik 25 kilodaltonluk fragmanı azalttı ve TDP-43’ü sitoplazmadan çekirdeğe doğru kaydırdı. Tüm genom RNA dizilemesi, TDP-43’ün tetiklediği binlerce gen ifadelerindeki değişikliğin RAD23A azaltıldığında kısmen geri döndüğünü gösterdi; özellikle nöronal fonksiyon, mitokondriyal enerji üretimi ve aggrefaji gibi agregat temizleme yollarında yer alan genler etkilenmişti.
Gizli “çözünmeyen” proteomun yeniden şekillenmesi
Normal deterjanlara dirençli inatçı agregatlara daha yakından bakmak için ekip, fare korteksinin çözünmeyen fraksiyonunda sıkışmış proteinleri kataloglamak üzere ağır izotop kütle spektrometrisi kullandı. İnsan TDP-43’ün ekspresyonu proteazom bileşenlerini, iskelet ve taşıma proteinlerini ve diğer hücresel makineleri bu agregatlara çekti. RAD23A düşürüldüğünde, bu çözünmeyen proteomun genel bileşimi değişti: daha az proteazom ve taşıma ile ilişkili protein el konulmuş, bazı ribozomal ve stresle ilişkili proteinler ise agregatlarda artmıştı. Önemli olarak, bu yeniden şekillenme RNA düzeylerindeki değişiklikleri basitçe yansıtmıyordu; bu da RAD23A’nın esasen mevcut proteinlerin çözünür ve agregatlaşmış durumlar arasında nasıl paylaştırıldığını etkilediğini, her proteinden ne kadar üretildiğini doğrudan değiştirmediğini öne sürüyor.
Gelecekteki terapiler için olası anlamı
Birlikte ele alındığında, bu bulgular RAD23A’yı stres altındaki nöronlarda protein kalite kontrolünün güçlü bir ayarlayıcısı olarak resmediyor. TDP-43 kaynaklı bir fare modelinde RAD23A’yı kısmen azaltarak yazarlar toksik protein kümelerini azaltabildiler, protein-bertaraf mekanizmasının işlevini geri getirebildiler, zararlı gen ifade değişikliklerini yatıştırabildiler, beyin inflamasyonunu sınırlayabildiler ve yaşam ile motor fonksiyonunu uzatabildiler. Anormal TDP-43 birikimi hem kalıtsal hem de sporadik ALS, FTD ve ilişkili bozukluklarda yaygın olduğundan, RAD23A’yı insanla uyumlu antisens ilaçlarla hedeflemek, temel ve gerekli bir protein olan TDP-43’ü doğrudan engellemeden nöronları korumanın bir yolunu sunabilir. Diğer modellerde ve insanlarda test edilmesi gereken çok şey olsa da, bu çalışma RAD23A’yı nörodejenerasyonun ortak yoluna yeni ve umut verici bir müdahale noktası olarak ortaya koyuyor.
Atıf: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Anahtar kelimeler: TDP-43, ALS, protein agregasyonu, proteazom, antisens terapisi