Clear Sky Science · tr
Doku morfolojisi ile mekansal transkriptomiklerin birleştirilmesi
Dokulara İki Farklı Yoldan Bakmak
Hekimler ve araştırmacılar artık bir dokuda hangi genlerin aktif olduğunu bilmenin ötesinde, bu genlerin tam olarak nerede açıldığını da öğrenmek istiyor. Aynı zamanda hastane mikroskopları, patologların her gün kullandığı doku yapısına ilişkin zengin görüntüler yakalıyor. Bu yazı, yeni bir alanın bu iki bakışı — ayrıntılı gen aktivite haritaları ile sıradan mikroskop görüntüleri — nasıl birbirine bağlamaya çalıştığını ve bu birleşmenin daha erken tanılar, gelişmiş kanser sınıflandırması ve hastalıkların nasıl ortaya çıkıp yayıldığına dair daha derin içgörüler sağlayabileceğini anlatıyor.
Dağınık Hücrelerden Gen Aktivite Haritalarına
Yıllarca güçlü “omik” yöntemler dokuları tek hücre karışımlarına öğütmeyi gerektiriyordu; bu da her hücrenin dokuda nereden geldiğine dair bilgiyi yok ediyordu. Mekansal transkriptomik bunu değiştirerek her hücrenin konumunu korurken gen aktivitesini ölçmeyi sağladı. Sonuç, her birinin gen ifade profili ve kesin koordinatları olan bir nokta ızgarasıdır. Tek başına bu mekansal gen verisi hâlihazırda hücresel çeşitlilik ve hastalık mimarisine dair yeni desenler ortaya koydu. Ancak bir kez ölçüldüğünde değişmiyor ve deneyi tekrarlamak pahalı. Buna karşılık, yaygın olarak kullanılan hematoksilin ve eozin (H&E) gibi standart boyalarla elde edilen doku görüntüleri ucuz, bol ve hücre şekli, yoğunluk ve doku düzeni hakkında görsel ipuçları içeriyor.
Görüntüleri ve Genleri Birleştirmenin İki Yolu
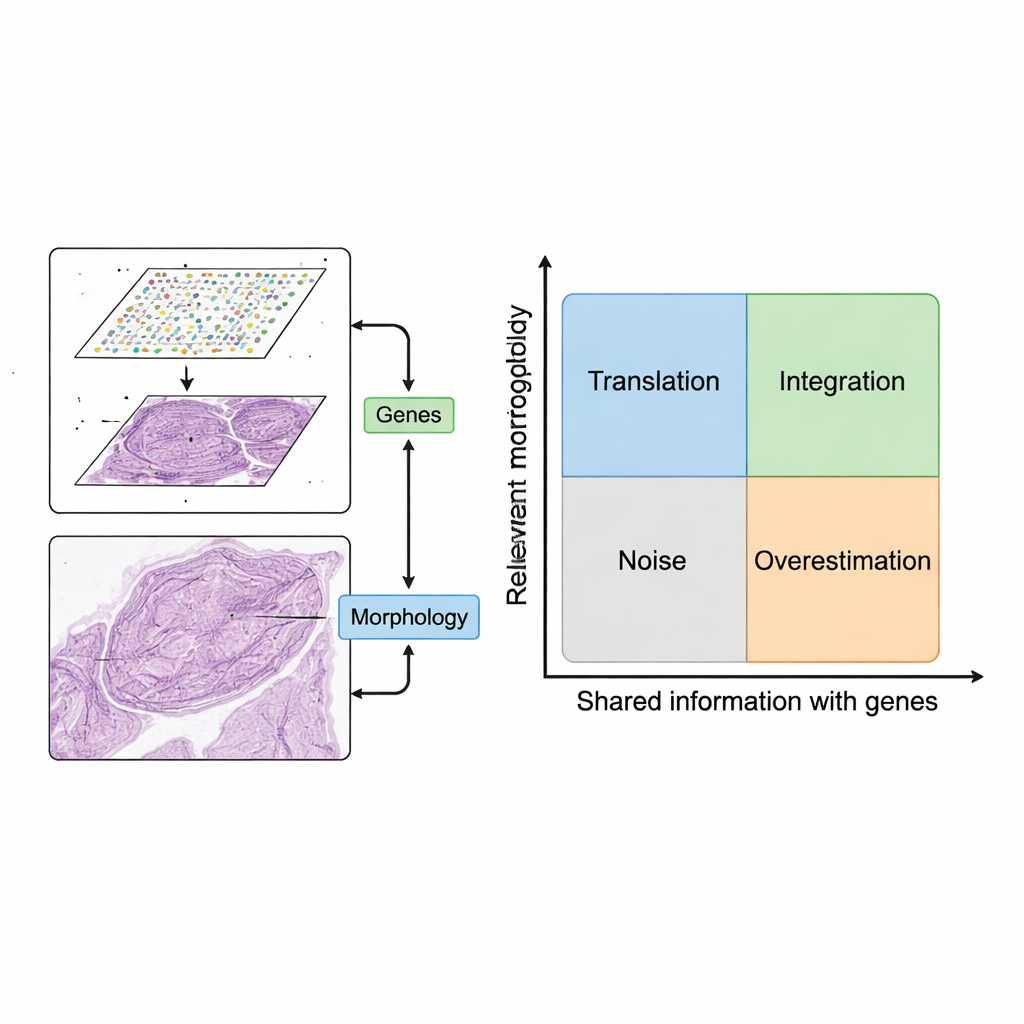
Derleme, bu iki veri kaynağını birlikte kullanmak için basit ama güçlü bir çerçeve öneriyor. İlk olarak, görüntü yamaları yakınlardaki gen ifade noktalarıyla eşleştiriliyor. Daha sonra bilgisayar modelleri görüntülerden — şekil, doku ve organizasyonu yakalayan desenler — özellikler çıkarıyor ve bunları gen ifadesindeki desenlerle karşılaştırıyor. Yazarlar iki arzulanan senaryoyu tanımlıyor. “Çeviri”de, görüntü özellikleri ilgili gen aktivitesini yakından izler; böylece modeller yalnızca doku görüntüsünü kullanarak hangi genlerin aktif olduğunu tahmin edebilir. Bu, eksik gen ölçümlerini doldurmak, orijinal ızgaradan daha ince çözünürlük elde etmek ya da ekstra laboratuvar çalışması yapmadan rutin klinik lamlardan gen aktivitesini çıkarmak için kullanılabilir. “Entegrasyon”da ise görüntü özellikleri gen verilerinin kaçırdığı, örneğin yavaş yapısal değişiklikler veya ince doku organizasyonu gibi faydalı bilgileri yakalar ve dokunun içinde daha net bölgeler veya “alanlar” tanımlamaya yardımcı olur.
Ek Bilgi Ne Zaman Yarar Sağlar — Ne Zaman Zararlı Olur
Her görüntü özelliği kullanılmaya değmez. Yazarlar, iki eksenli kavramsal bir harita sunuyor: bir eksen görüntü özelliğinin biyolojik soru için ne kadar alakalı olduğunu, diğer eksen ise gen bilgileriyla ne kadar örtüştüğünü gösteriyor. Ne alakalı ne de genlerle ilişkili olan özellikler gürültüye eşdeğerdir; örneğin boyama artefaktları. Gen desenlerini takip eden ama önemsiz genlere (örneğin temel ev işi genleri) bağlı olan özellikler ise modellerin kağıt üzerinde iyi görünmesini sağlayabilir ama klinik değeri azdır. Yöntemleri çeviri, entegrasyon, gürültü ve aşırı değerlendirme olmak üzere dört çeyreğe ayırarak, çerçevenin görüntülerle genlerin gerçekten ne zaman ek içgörü sağladığını ve ne zaman zaten bilinenleri tekrar ettiğini veya örtbas ettiğini netleştirdiği gösteriliyor.
Mevcut Araçlar, Testler ve Büyüme Zorlukları
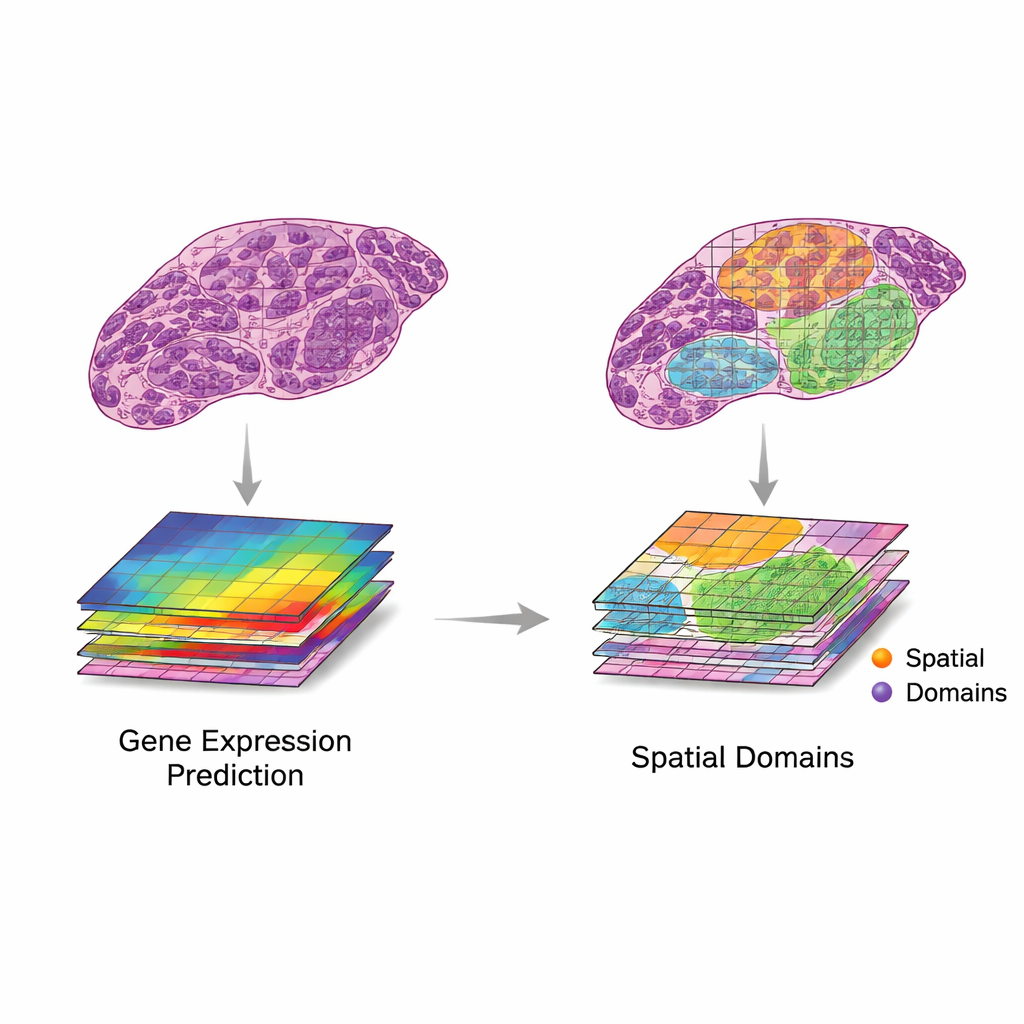
Hızla ilerleyen bir yapay zekâ dalgası şimdi gerçek verilere çeviri ve entegrasyonu uygulamaya çalışıyor. Erken sistemler konvolüsyonel sinir ağlarına dayanırken, yenileri transformerlar, grafik sinir ağları ve küçük hücresel yapılardan tüm lam bağlamına kadar ayrıntı alabilen çok ölçekli modelleri kullanıyor. Bu yöntemler H&E görüntülerinden gen aktivitesini tahmin etmek, süper-çözünürlük haritaları üretmek ve farklı davranış gösteren doku bölgelerini belirlemeye yardımcı olmak için kullanıldı. Performansı değerlendirmek için araştırmacılar, tahmin edilen ve gözlemlenen gen seviyeleri arasındaki korelasyon veya yapay zekâ tarafından tanımlanan bölgeler ile uzman patoloğun etiketleri arasındaki uyum gibi istatistiksel ölçütlere dayanıyor. Ancak veri kümeleri hâlâ küçük ve değişken, çalışmalar arasında karşılaştırma zor. Bildirilen birçok kazanç aşırı uyumdan kaynaklanıyor olabilir veya klinikte az önemi olan genler ve desenlerde başarılı olunmasıyla sınırlı olabilir.
Bunun Nereye Götürebileceği
Yazarlar, mekansal gen haritalarının doku görüntüleriyle birleştirilmesinin umut verici ancak hâlâ erken aşamada bir çaba olduğunu sonuçlandırıyor. Bugünün modelleri genellikle yalnızca orta düzey doğruluk sağlıyor ve rutin tıbbi kullanım için henüz hazır olduklarını kanıtlamadılar. Gelecekte ilerleme muhtemelen milyonlarca patoloji lamı üzerinde eğitilmiş büyük “temel modeller” gibi daha iyi görüntü özelliklerinden ve hasta bakımını gerçekten etkileyen genlere ve desenlere odaklanmaktan gelecek. Dikkatle tasarlanmış entegrasyon bir gün dokunun şimdi nasıl göründüğü ile genlerin gelecekte ne olacağını öngörmesi arasında uyumsuzluklar tespit ederek hastalığın erken uyarı işaretlerini ortaya çıkarabilir. Kısacası, bu çalışma rutin mikroskopik görüntüleri doktorların hastalığı daha kesin anlaması ve tedavi etmesine yardımcı olacak zengin, gen bilgisiyle desteklenmiş haritalara dönüştürme yol haritasını ortaya koyuyor.
Atıf: Chelebian, E., Avenel, C. & Wählby, C. Combining spatial transcriptomics with tissue morphology. Nat Commun 16, 4452 (2025). https://doi.org/10.1038/s41467-025-58989-8
Anahtar kelimeler: mekansal transkriptomik, doku morfolojisi, dijital patoloji, gen ekspresyonu tahmini, görüntüleme yapay zekâsı