Clear Sky Science · tr
N-terminal asetilasyonun etkisini aydınlatmak: proteinden fizyolojiye
Minik kimyasal işaretçilerin protein davranışını nasıl değiştirebildiği
Vücudunuzdaki her hücre, doğru katlanması, doğru yere gitmesi, moleküler makineler halinde bir araya gelmesi ve hasar gördüğünde uzaklaştırılması gereken proteinlerle doludur. Bu derleme makalesi, birçok proteinin bir ucunda meydana gelen ince ama son derece yaygın bir kimyasal değişikliği—N-terminal asetilasyon—inceliyor ve bu küçük “kapakçığın” hücre büyümesi ve stres tepkilerinden kalp gelişimi ve beyin işlevine kadar her şeyi nasıl kontrol etmeye yardımcı olduğunu gösteriyor.
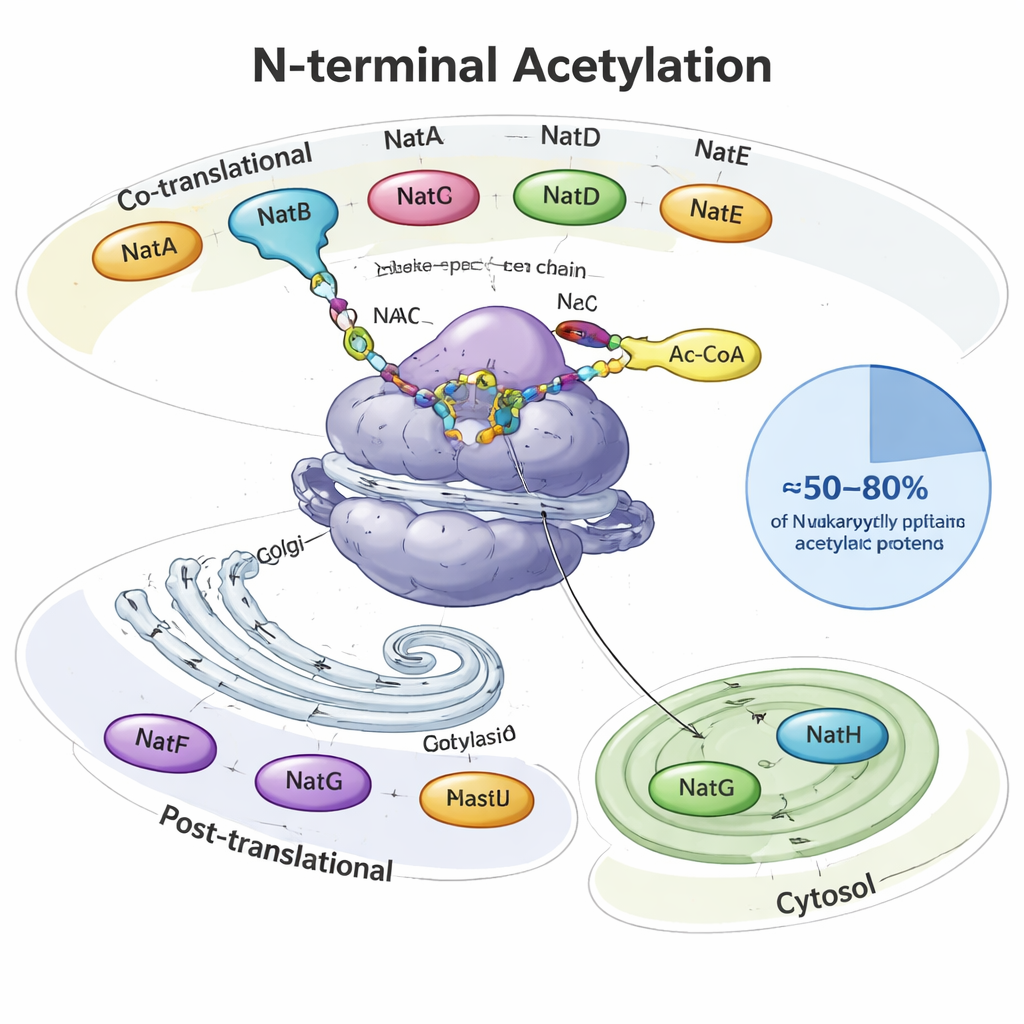
Çoğumuzun adını bile duymadığı protein kapağı
Bir protein sentezlendiğinde, ribozom adı verilen hücrenin protein fabrikasından bir iplik gibi çıkar. Çok başında—N-terminusunda—birçok ökaryotik protein bir asetil grubu, yani küçük iki karbonlu bir kapak alır. N-terminal asetiltransferazlar (NAT'ler) adı verilen özel enzimler bu işi yapar ve ortak bir metabolik molekül (asetil‑CoA) bağışçı olarak kullanılır. Maya, bitki ve hayvanlarda sekiz ana NAT türü (NatA–NatH) bu işi paylaşır. Bazıları protein henüz üretilirken hareket ederken, diğerleri sonradan çalışır ve Golgi aygıtı veya bitki plastidleri gibi belirli konumlara yerleşmiştir. Birlikte, hücresel proteinlerin yaklaşık yarısından dörtte beşine kadarını modifiye ederler; her NAT iki ila dört amino asidin başlangıç dizilerini tanır.
Her birinin kendine özgü uzmanlığı olan pek çok enzim
NatA, NatB ve NatC işin ağır yükünü çeker; ribozomda hemen hareket ederek “N-terminal asetilom”un geniş alanlarını kapsarlar. Sadece NatA, genellikle ilk metiyoninin budanmış olduğu insan proteinlerinin yaklaşık %40’ını modifiye edebilir. NatB ve NatC, ilk metiyoninlerini koruyan proteinler üzerinde etkilidir, ancak yanlarındaki amino asit tercihleri farklıdır. Diğer NAT'ler daha seçicidir: NatD yalnızca DNA’yı paketleyen birkaç histon proteinine odaklanır, NatF Golgi’deki transmembran proteinleri hedefler, NatG bitki plastidlerinin içinde çalışır ve NatH (NAA80) hücre iskeletinin önemli bir bileşeni olan aktin üzerinde özel iki adımlı bir olgunlaşmayı tamamlar. Makale, yardımcı alt birimlerin bu enzimleri ribozomlara veya membranlara nasıl demirlediğini ve hangi proteinlere etki edeceklerini nasıl ince ayar yaptığını gösteren yapısal ve biyokimyasal çalışmaları bir araya getirir.
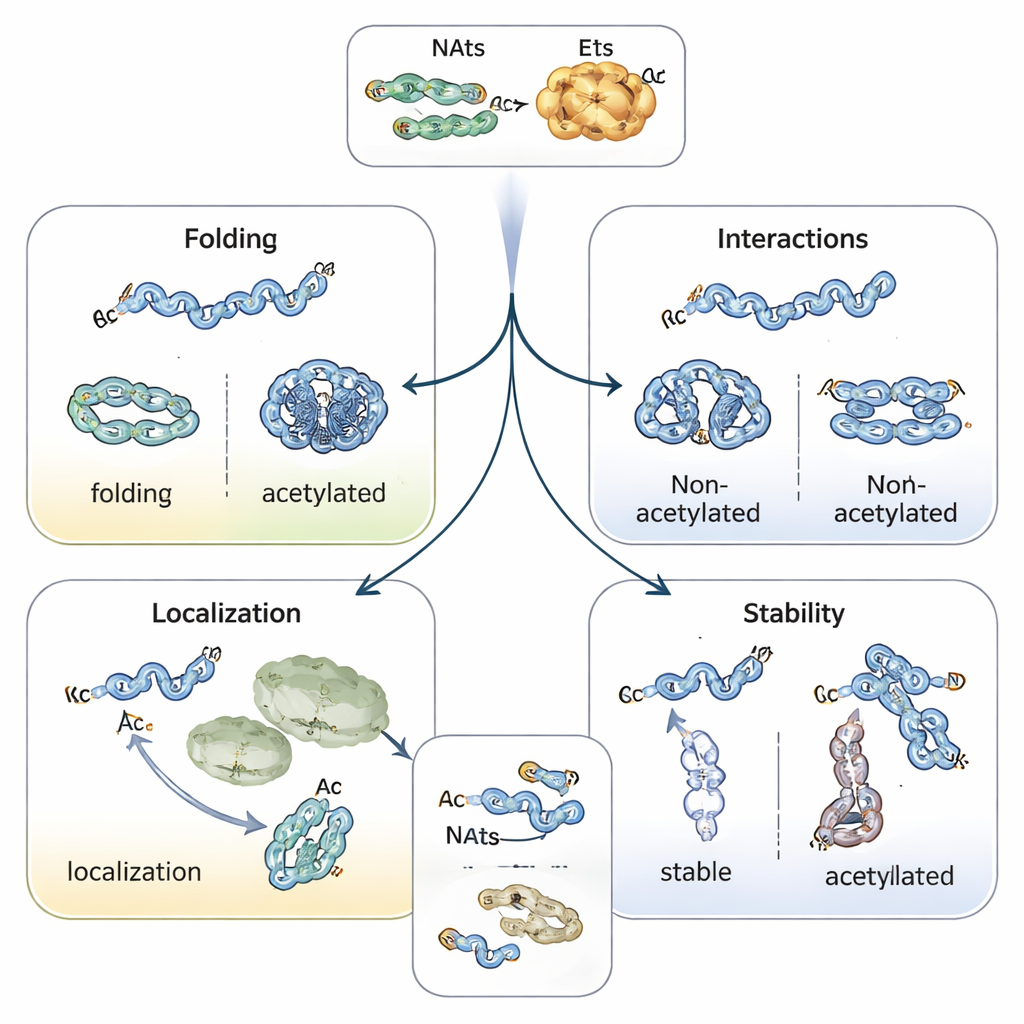
Protein katlanmasını, yerini ve ömrünü yönlendirmek
Bir asetil kapakçık eklemek, proteinin başlangıcının kimyasal doğasını değiştirir; sıklıkla helikal yapıları stabilize eder ve proteinlerin nasıl katlandığını etkiler. Örneğin, Parkinson ile ilişkili alfa-sinüklein proteini, N-terminusu asetillenmiş olduğunda daha az kümelenme eğiliminde olur ve daha güvenli bir şekil benimser. Aktinle ortak çalışan tropomiyozin, düzgün asetillendiğinde aktin filamentlerine çok daha iyi bağlanır ve bunları düzenler. Bitkilerde ve hayvanlarda N-terminal asetilasyon, proteinlerin kloroplastlar, lizozomlar veya Golgi gibi hedefleri bulmasına yardımcı olan bir adres etiketi görevi görebilir. Belki de en çarpıcı rolü proteinlerin ne kadar süre hayatta kaldığını belirlemesidir: korunmasız bir N-terminus, ubiquitin etiketleme enzimleri tarafından bir “yıkım sinyali” olarak okunabilirken, asetilasyon bu sinyali maskeleyip proteini stabilize edebilir—veya bazı durumlarda, protein yanlış katlanmışsa ya da doğru kompleks içinde değilse yalnızca o zaman tanınan koşullu bir etiketi oluşturabilir.
Hücre fizyolojisinden gelişim ve hastalığa
N-terminal asetilasyon çok sayıda protekle bağlantılı olduğundan, NAT'lerin bozulması tüm organizma için geniş sonuçlar doğurur. Model türlerde NatA, NatB veya NatC’nin ortadan kaldırılması genellikle ciddi gelişimsel kusurlara, değişmiş stres tepkilerine veya hatta ölümcül sonuçlara yol açarken, NatF ve NatH gibi daha özelleşmiş enzimler beyin kalsifikasyonları veya işitme kaybı gibi daha sınırlı sorunlara neden olur. İnsanlarda birkaç NAT genindeki kalıtsal mutasyonlar entelektüel gerilik, kalp kusurları veya kas zayıflığıyla seyreden nadir nörogelişimsel sendromların temelini oluşturur. Aynı makine sıklıkla kanserlerde aşırı aktiftir; yükselmiş NAT seviyeleri kötü prognoz ile ilişkilendirilir ve tümör büyümesini, metastazı ve tedaviye direnç geliştirmeyi teşvik edebilir. N-terminal asetilasyondaki değişiklikler ayrıca alfa-sinüklein ve huntingtin gibi agregasyona eğilimli proteinleri etkileyerek bu modifikasyonu nörodejeneratif hastalık mekanizmalarına bağlar.
Gelecek yönelimleri ve tıbbi vaat
Yazarlar, bu N-terminal kapakları ekleyen çekirdek enzimlerin çoğunu artık bilsek de, belirli protein hedeflerinin ve düzenleyici kuralların yalnızca bir kısmını anladığımız sonucuna varıyorlar. Öne çıkan tema, proteinin başındaki asetilasyonun sıklıkla onu erken yok olmadan koruması, aynı zamanda kalite kontrol için bağlama bağlı sinyaller oluşturmasıdır. Hangi ubiquitin ligazlarının hangi N-terminal desenleri okuduğunu belirlemek ve herhangi bir enzimin bu kapakları çıkarıp çıkaramayacağını keşfetmek temel açık sorulardır. NAT'ler protein stabilitesi, gen düzenlemesi ve hücre stres tepkilerinin kesişim noktasında bulunduğundan, seçici NAT inhibitörleri—ve belki gelecekte belirli hastalıkla ilişkili proteinlerin N-terminal asetilasyonunu ince ayar yapacak araçlar—kanser, kalp hastalığı ve nörodejenerasyon için yeni tedaviler açısından umut verici yollar olarak ortaya çıkmaktadır.
Atıf: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Anahtar kelimeler: protein modifikasyonu, N-terminal asetilasyon, protein kalite kontrolü, nörodejeneratif hastalık, kanser biyolojisi