Clear Sky Science · tr
m6A RNA metilasyonu çölyak hastalığında antiviral yanıtı modüle ediyor
Bir Virüs ve Glüten Güçlerini Birleştirdiğinde
Çölyak hastalığı genellikle basit bir besin sorunu olarak düşünülür: glüten yerseniz bağırsaklarınız zarar görür. Bu çalışma, yaygın bir bağırsak virüsü türü ile RNA moleküllerimiz üzerindeki küçük bir kimyasal etiketi arasında iş birliği olduğunu ve bunun bağışıklık sistemini kalıcı hasara itebileceğini gösteriyor. Bu gizli kontrol katmanını anlamak, neden yalnızca bazı insanların çölyak hastalığı geliştirdiğini açıklamaya yardımcı olabilir ve glütensiz diyeti aşan yeni tedavilere işaret edebilir. 
Genetik Mesajlarımızdaki Gizli Bir Etiket
Hücrelerimiz sürekli genleri okur ve bunları hangi proteinlerin yapılacağını söyleyen kısa "mesajlar" olan RNA'lara kopyalar. Bu mesajlar sabit değildir; bir mesajın ne kadar güçlü okunacağını değiştiren yüksek ışıkçılar gibi davranan kimyasal işaretlerle süslenebilirler. En yaygın işaretlerden biri m6A olarak adlandırılan, RNA harflerinde küçük bir değişikliktir. Virüslerin enfekte hücrelerde bu RNA işaretlerini değiştirdiği biliniyor ve önceki çalışmalar m6A'yı çölyak bağırsaklarındaki glüten kaynaklı iltihapla ilişkilendirmişti. Bu makalenin yazarları, bir virüsün tetiklediği m6A değişikliğinin bağışıklık sistemini yiyeceğe toleranstan saldırıya çevirtip çeviremediğini sordular.
Çölyak Hastası Verilerinden Kanıt
Araştırmacılar önce aktif çölyak hastalığı olan kişiler ile çölyak olmayan kontrollerin kan ve bağırsak biyopsilerini inceledi. Çölyak hastalarının, bağırsakları enfekte eden çift iplikçikli RNA virüsü reovirüse karşı daha yüksek düzeyde antikor taşıdığı bulundu; bu, daha sık veya daha güçlü maruziyete işaret ediyor. Bu hastaların bağırsak dokusunda, özellikle IRF7 adı verilen ana antiviral uyarı geninin daha yüksek düzeyde açık olduğu; ayrıca STAT1 ve bağışıklık hücrelerini çeken CXCL10 gibi iltihaplı moleküllerin arttığı görüldü. Aynı zamanda m6A işaretlerini ekleyen ve okuyan mekanizma daha aktifti ve RNA üzerindeki toplam m6A düzeyleri yüksekti. Antiviral genlerin ifadesi, m6A ile ilişkili genlerin ifadeleriyle birlikte artıp azaldı; bu da aynı kontrol sisteminin hem viral savunmayı hem de otoimmün hasarı yönlendiriyor olabileceğine işaret etti.
Glütenin Viral Alarmı Nasıl Güçlendirdiği
Neden-sonuç ilişkisini araştırmak için ekip laboratuvarda yetiştirilen bağırsak hücrelerinde çölyak benzeri bir model kurdu. Sentetik bir çift iplikçikli RNA kullanarak viral enfeksiyon taklidi yaptılar, ardından yemekten sonra bağırsakta ortaya çıkacak sindirilmiş glüten parçacıklarını eklediler. Sadece viral taklit hem IRF3 hem de IRF7'yi artırdı; bunlar antiviral yanıtların iki ana anahtarıdır. Ancak üzerine glüten eklendiğinde IRF7 güçlü bir ekstra sıçrama gösterdi, IRF3 ise göstermedi. Araştırmacılar bu koşullarda IRF7 RNA'sının belirli bir bölgesinde m6A işaretlerinin arttığını ve bu RNA'nın m6A yazan enzim (METTL3) ve silen enzim (ALKBH5) ile fiziksel etkileşimde bulunduğunu keşfettiler. METTL3'ü artırmak veya ALKBH5'i azaltmak gibi m6A'yı yükseltmek, IRF7 düzeylerini daha da yükseltti; bu da glüten-artı-virüs sinerjisini doğrudan bu RNA modifikasyonuna bağladı. 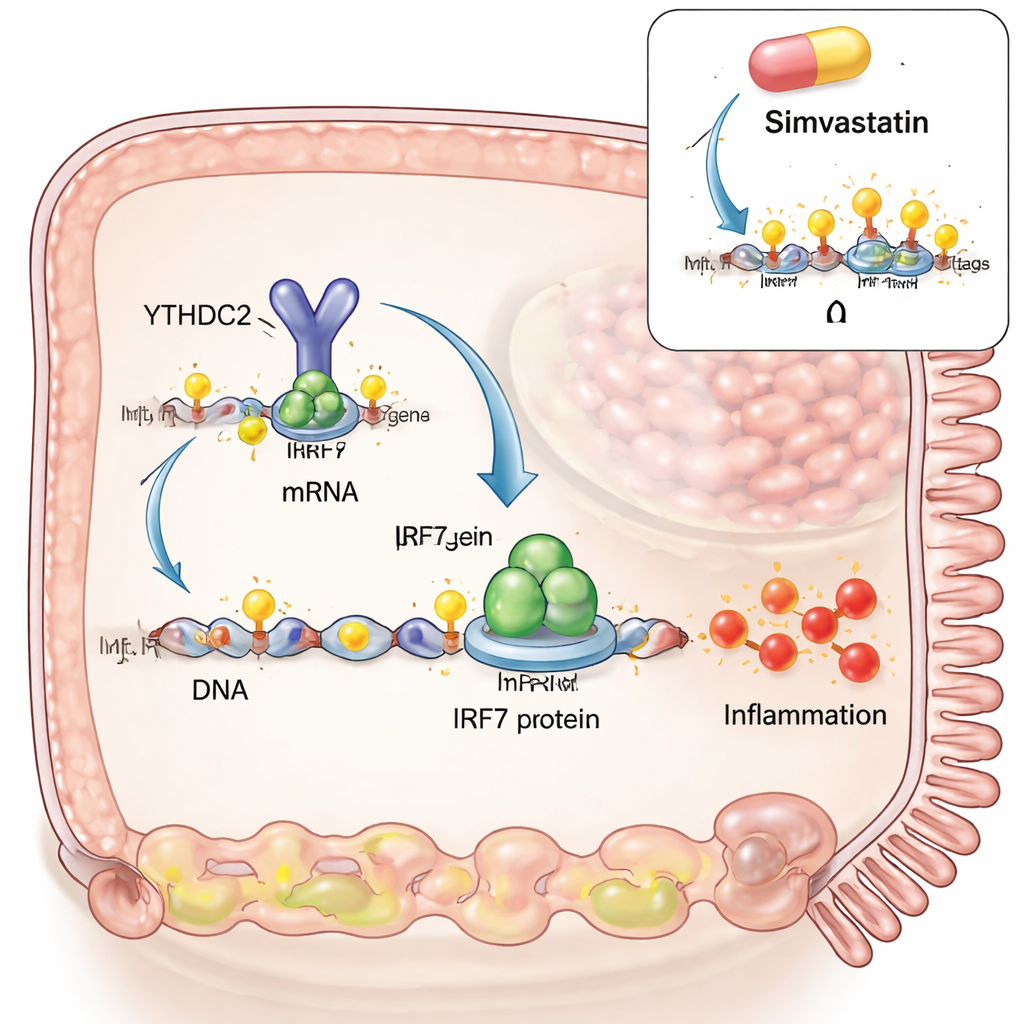
Moleküler Aracı ve Sürpriz Bir İlaç
İleriye dönük olarak yazarlar, IRF7 RNA'sındaki m6A işaretlerinin hücrenin davranışını nasıl değiştirdiğini sordular. Aynı protein kodunu taşıyan ancak m6A bölgeleri olmayan bir IRF7 RNA versiyonu tasarladılar. Bu RNA benzer miktarda transkript üretti, ancak çok daha az IRF7 proteini ve STAT1 ile CXCL10 gibi aşağı akım iltihap genlerini tetikleyemedi. Eksik halka, genellikle protein kodlayan bölgede m6A'ya bağlanan ve verimli çeviriyi destekleyen bir okuyucu proteini olan YTHDC2 idi. m6A bölgeleri olmadan YTHDC2 IRF7 RNA'sına tutunamıyordu. Hücre modelinde m6A yazarı METTL3'ü engellemek IRF7 proteini ve CXCL10'u azaltarak iltihap çıktılarını düşürdü. Yakın zamanda diğer dokularda m6A'yı azalttığı gösterilmiş bir kolesterol düşürücü ilaç olan simvastatin de IRF7 RNA'sındaki m6A'yı azalttı, hücrelerde IRF7 proteinini düşürdü ve taze alınan çölyak bağırsak biyopsilerinde IRF7 ilişkili genleri zayıflattı. Büyük ölçekli gen ifadesi karşılaştırmaları, simvastatinin çölyak dokusunu glütensiz diyet uygulayan hastalara daha çok benzeyen bir profile ittiğini gösterdi.
Çölyak Hastaları İçin Anlamı
Bu çalışma, bağırsak virüsü ile glütenin RNA kontrolünün ince ayarlı bir katmanında birlikte hareket ettiği bir tablo çiziyor. Duyarlı kişilerde viral enfeksiyon, intestinal hücrelerde IRF7 RNA'sının m6A etiketlenmesini artırıyor gibi görünüyor. Ardından glüten maruziyeti bu etiketli sinyali daha da güçlendiriyor; bunun sonucu daha fazla IRF7 proteini, daha güçlü antiviral alarmlar ve bağırsak örtüsüne karşı otoimmün saldırıya katkıda bulunan daha yüksek seviyede iltihap mesajcıları oluyor. m6A işaretlerini genetik olarak veya simvastatin gibi bir ilaçla azaltmak, en azından laboratuvar ve ex vivo modellerde bu zincirleme reaksiyonu yumuşatabiliyor. Halk için temel mesaj, çölyak hastalığının yalnızca ne yediğinizle ilgili olmadığı; enfeksiyonların ve RNA üzerindeki ince kimyasal işaretlerin bağışıklık sisteminin tolerans ya da saldırı kararını nasıl şekillendirdiğiyle de ilgili olduğudur. Bu RNA işaretlerini hedeflemek bir gün glütensiz diyete ek olarak kullanılabilir ve daha geniş bir otoimmün hastalık yelpazesi için yeni tedavilere ilham verebilir.
Atıf: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Anahtar kelimeler: çölyak hastalığı, RNA metilasyonu, antiviral bağışıklık, IRF7, simvastatin