Clear Sky Science · tr
CRISPR-AuNP: HSPC’lerde maliyet-etkin ve modüler viral olmayan gen düzenleme için altın nanoparçacık platformunun fizikokimyasal optimizasyonu
Gen Düzenlemeyi Daha Fazla Hastaya Ulaştırmak
CRISPR gibi gen düzenleme araçları kalıtsal kan hastalıkları olan kişilerin yaşamlarını zaten değiştirdi, ancak tedaviler hâlâ pahalı, teknik olarak zorlu ve büyük ölçüde birkaç uzman merkezle sınırlı. Bu makale, CRISPR’i kan oluşturan kök hücrelere laboratuvar tezgâhında yalnızca birkaç saatte karıştırılabilecek küçük altın bazlı parçacıklarla iletmenin yeni bir yolunu anlatıyor. Amaç, güçlü gen düzenleme yaklaşımlarını daha basit, daha ucuz ve dünyanın daha fazla yerine konuşlandırılması daha kolay hale getirmek.
Kan Kök Hücrelerinin Önemi
Kan oluşturan kök ve progenitör hücreler kemik iliğinde yaşar ve vücuttaki tüm farklı kan hücresi tiplerini sürekli olarak yeniler. Doktorlar bu hücrelerde hastalığa neden olan mutasyonları güvenli bir şekilde düzeltebilirse, tek seferlik bir tedavi çekik hücre anemisi ve bazı bağışıklık yetmezlikleri gibi durumlar için ömür boyu süren bir kür sağlayabilir. Günümüzde bu hücrelere CRISPR ulaştırmanın en yaygın yolu elektroporasyona dayanıyor; bu işlem hücre zarlarında delikler açmak için elektrik darbeleri kullanıyor. Güçlü olmakla birlikte elektroporasyon hücrelere zarar veriyor, pahalı cihazlar ve özel reaktifler gerektiriyor ve kaynak kısıtlı ortamlara kolayca ölçeklenip aktarılmıyor. Daha güvenli viral vektörler birçok gen terapisi için mükemmel olsa da, sürekli olarak düzenleme araçları ürettikleri için CRISPR teslimine daha az uygun; bu da hedef dışı değişiklik riskini artırıyor.
Küçük Bir Altın Taşıyıcı İnşa Etmek
Araştırmacılar yüzeyinde CRISPR bileşenleri taşıyan daha önce rapor edilmiş bir altın nanoparçacık sistemini geliştirmeyi amaçladılar. Önceki tasarımlarda, CRISPR kesme proteinini hedefe yönlendiren kılavuz RNA doğrudan altın çekirdeğe sabitleniyor ve ardından Cas9 proteini ile eşleştiriliyordu. Bu, bir tür CRISPR enzimi için makul düzeyde işe yarıyordu, ancak birçok terapötik stratejinin merkezinde yer alan Cas9 ile zayıf performans gösteriyordu. Partikül montajı sırasında kullanılan asidik koşullar altında Cas9 ve kılavuz RNA’nın davranışını yakından inceleyerek ekip, kılavuz RNA çiftinin altın yüzeyde kararsız hale geldiğini ve bunun da partiküle çok az veya hiç aktif Cas9 bağlanmamasına yol açtığını keşfetti. Konfokal mikroskopi ayrıca partiküllerin hücresel bölmelerden kaçmasına yardımcı olması amaçlanan polimer kaplamanın görevini yapmadan önce soyulabileceğini gösterdi.
Platformun Aşama Aşama Yeniden Tasarımı
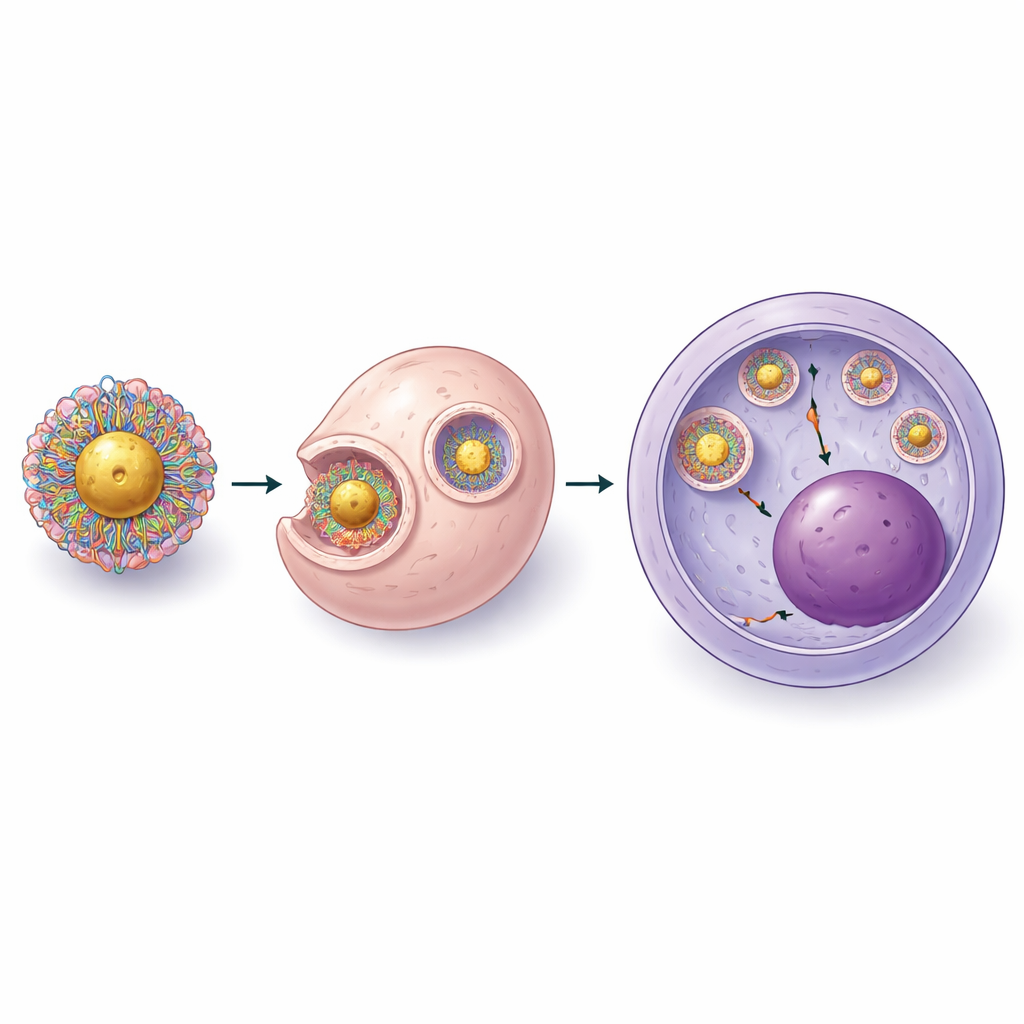
Bu sorunları aşmak için bilim insanları sistemi üç aşamada baştan inşa ettiler. İlk olarak, çıplak RNA’yı altına sabitleyip sonra proteini eklemek yerine, altına temas ettirmeden önce tam CRISPR ribonükleoprotein komplekslerini (protein artı kılavuz RNA) oluşturdular. Bu komplekslerin partiküllere bağlanmasına izin verirken kesme proteinini aktif tutan hafif asidik bir koşul belirlediler. Ardından, yüklü partikülleri hücresel bölmelerden kaçış için gerekli pozitif yüklü zincirleri ile kümeleşmeyi önleyen esnek, su-sever polietilen glikol (PEG) segmentlerini birleştiren özel tasarlanmış polimerlerle sardılar. Boyut, yüzey yükü ve protein içeriğini ölçerek, çözelti stabilitesini korurken partikül başına düzinelerce CRISPR kompleksini tekrarlanabilir şekilde yükleyebildiklerini gösterdiler.
Hücrenin Savunmasını Aşmak
Daha iyi yüklemeye rağmen, ikinci nesil partiküller yine de kilit bir engelle mücadele ediyordu: CRISPR’in hücrenin iç veziküllerinden çıkarak DNA’nın bulunduğu bölgeye ulaşması. Bu nedenle ekip polimer katmanının kimyasını ve polimerdeki pozitif gruplarla CRISPR kompleksindeki negatif gruplar arasındaki oranı sistematik olarak ayarladı. Kısa PEG zincirlerinin ve kontrollü sayıda kükürt içeren bağlayıcıların eklenmesinin hem partikül stabilitesini hem de endozomal membranları bozma yeteneğini hücreye zarar vermeden iyileştirdiğini keşfettiler. Son, üçüncü nesil tasarımda önce CRISPR ve polimerin kompakt komplekslerini oluşturdular, sonra bunları yoğunlaştırılmış altın çekirdeklere bağladılar. Elektron mikroskopisi her altın küre etrafında ince bir CRISPR ve polimer kabuğu gösterdi ve canlı kök hücrelerde görüntüleme yükün hücre içine kaçabildiğini ve çekirdeğe ulaşabildiğini doğruladı.
Çoklu CRISPR Araçlarında Düzenleme Sonuçları
Optimumlaştırılmış partiküllerin ne kadar iyi çalıştığını test etmek için araştırmacılar, neredeyse tüm kan hücrelerinin yüzeyinde bulunan ve akış sitometrisi ile kolayca ölçülebilen beta-2-mikroglobulin adlı bir geni hedeflediler. Üçüncü nesil altın platformlarını kullanarak primer insan kan kök ve progenitör hücrelerinde bu genin %10’un üzerinde hassas bozulmalar elde ettiler—birçok terapötik uygulama için anlamlı kabul edilen düzeyler—ve yüksek hücre sağkalımını korudular. Bu verimlilik elektroporasyonla ulaşılabilen seviyeden düşük olsa da, altın sistemi özel ekipman gerektirmiyor ve hücrelere asgari stres veriyordu. Önemli olarak, aynı platform Cas9, Cas12a ve daha yeni bir enzim olan Cas12a-M29-1 dahil farklı CRISPR proteinleriyle benzer düzenleme düzeyleri ve tespit edilebilir toksisite olmadan kullanılabildi; bu da tasarımın modüler doğasını vurguluyor.
Gelecekteki Tedaviler İçin Anlamı
Basitçe söylemek gerekirse, bu çalışma elektriksiz veya viral olmadan hassas kan kök hücrelerine CRISPR araçları taşıyabilen, dikkatle tasarlanmış küçük bir altın bazlı taşıyıcı inşa etmenin mümkün olduğunu gösteriyor; hazır bulunan malzemelerle milyon hücre başına yetmiş doların altında bir maliyetle tezgâhta birleştirilebiliyor. Daha yüksek düzeyde düzeltilmiş hücreler gerektiren hastalıklar için özellikle günümüzün en iyi klinik yöntemlerinin verimliliğine ulaşmak üzere daha fazla iyileştirme gerekse de, bu tezgâhta monte edilen platform sofistike gen düzenlemeyi uygulama konusundaki pratik engelleri azaltıyor. Sürekli iyileştirme ve güvenlik testleri ile bu tür nanoparçacıklar CRISPR temelli terapilerin faydalarını uzman merkezlerin ötesine yaymaya yardımcı olabilir ve kür sağlayan tedavileri dünya çapında daha erişilebilir hale getirebilir.
Atıf: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Anahtar kelimeler: CRISPR gen düzenleme, altın nanoparçacıklar, hematopoetik kök hücreler, viral olmayan teslimat, nanoterapi