Clear Sky Science · tr
Kuproptozla Mücadele: Metabolik Yeniden Yapılanmadan Kanser Tedavisinde Terapötik Sömürüye
Yararlı Bir Metalin Kanser Karşısında Dönüşmesi
Bakır genellikle elektrik kablosu ve sıhhi tesisat bileşeni olarak bilinir, ancak hücrelerimizde de sessizce dolaşır; enzimlerin enerji üretmesine ve hasardan korunmamıza yardımcı olur. Bu derleme makale, şaşırtıcı bir kıvrımı inceliyor: doğru koşullar altında aşırı bakır kanser hücrelerini özel bir ölüm türüne sürükleyebilir. "Kuproptoz" adı verilen bu süreci anlamak, standart tedavileri alt etmiş tümörleri hedef almanın yeni yollarını açabilir.
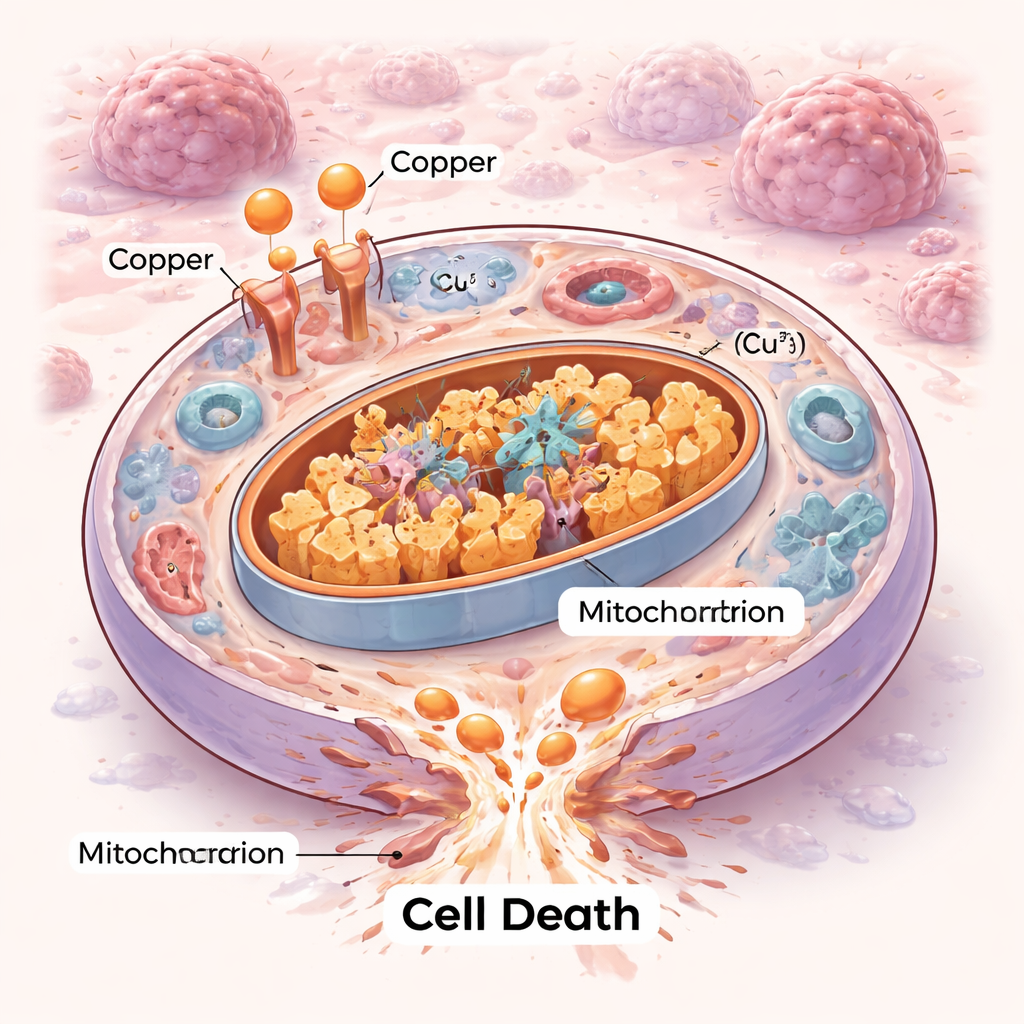
Hücrelerin Ölebileceği Yeni Bir Yol
Hücreler hep aynı biçimde ölmez. On yıllardır araştırmacılar apoptoz gibi düzenli öz‑yıkım programlarını ve ferroptoz gibi daha yeni formları haritalandırdı. Kuproptoz bu alana yeni bir bölüm ekliyor. Burada aşırı bakır hücrenin enerji merkezlerine —mitokondrilere— doluşur ve normalde yakıtı yakmaya yardımcı olan belirli metabolik enzimlere bağlanır. Bu bağlanma söz konusu enzimlerin kümelenmesine ve mitokondrilerin işlevi için gerekli küçük demir‑kükürt bileşenlerinin kararsızlaşmasına neden olur. Sonuç, hücrenin onaramadığı türden bir iç trafik sıkışıklığı ve mekanik çöküş; bu da klasik intihar yolları yerine proteotoksik stres yoluyla ölümle sonuçlanır.
Kanser Hücreleri Bakırı ve Enerjiyi Nasıl Kontrol Eder
Bakır hem gerekli hem de tehlikeli olduğundan hücreler onu güvenle taşımak için ayrıntılı bir lojistik ağı sürdürür. Özel taşıyıcılar bakırı hücre içine getirir, şaperon proteinler onu mitokondrilere ve diğer hedeflere eşlik ettirir ve metallothioneinler ile glutathione gibi depolama molekülleri fazla olanı tutar. Tümörler sıklıkla bu sistemi yeniden düzenler. Bazıları yüksek enerji taleplerini karşılamak için girişimleri veya şaperonları artırır; diğerleri ise bakır yükünü önlemek için ihracatçıları veya depolama proteinlerini çoğaltır. Aynı zamanda birçok kanser metabolizmasını değiştirir —hücre yüzeyinde şeker yakımından daha derin mitokondriyal solunuma geçiş yapar. Derleme, kuproptozun hâlâ büyük ölçüde mitokondriye bağımlı hücrelerde en güçlü şekilde vurduğunu ve bu metabolik profile sahip tümörleri özellikle hassas kıldığını açıklıyor.
Bakır Hassasiyetini Ayarlayan Ana Anahtarlar
Hücredeki önemli “karar vericiler” kuproptozun gerçekleşip gerçekleşemeyeceğini etkiler. Örneğin tümör baskılayıcı p53, hücreleri hızlı şeker fermantasyonundan daha düzenli mitokondriyal yakıt kullanımına doğru itme eğilimindedir. Bunu yapmak ve bakır bağlayan enzimlerin işlenmesini değiştirmek yoluyla p53, kanserleri bakır kaynaklı ölüme daha duyarlı hale getirebilir — oysa p53'ün mutant biçimleri genellikle tersini yapar. Buna karşılık, yeterince oksijensiz tümör merkezlerinde aktive olan hipoksi faktörü HIF‑1α, kilit mitokondriyal enzimleri azaltıp bakır bağlayıcı kalkanları artırarak hücreleri kuproptozdan kaçırmaya yardımcı olur. Wnt/β‑catenin ve AKT gibi diğer yollar, bakır ihracını yönlendirerek veya kritik proteinleri kimyasal olarak değiştirerek direnç teşvik eder; böylece bu proteinler artık bakır aşırı yüklenmesine yanıt vermez. Birlikte, bu ağlar bir termostat gibi davranır; bir tümörün bakır bazlı tedaviye duyarlılığını yükseltir veya düşürürler.
Bakır, Bağışıklık Sistemi ve Daha Akıllı İlaç Dağılımı
Bakırın rolü yalnızca kanser hücrelerini doğrudan öldürmekle sınırlı değildir; aynı zamanda tümör çevresindeki bağışıklık ortamını da şekillendirir. Kontrollü bakır stresi, ölen kanser hücrelerini daha “görünür” kılabilir; tehlike sinyalleri salınımı T hücrelerini, dendritik hücreleri ve makrofajları çekip aktive eder. Bakır ayrıca tümörlerin anti‑kanser T hücrelerini kapatmak için kullandığı PD‑L1 gibi immün kontrol noktalarının düzeylerini etkileyebilir; bu da bakır hedefli ilaçların modern immünoterapi ile kombinasyonuna fırsatlar sunar. Serbest bakır sağlıklı dokulara zarar verebileceğinden araştırmacılar hassas araçlar geliştiriyor — bakırı seçici olarak kanser hücrelerine taşıyan küçük molekül iyonoforlar ve bakır veya bakır‑tetiklemeli ilaçları hedefe yönelik partiküller veya hidrojeller içinde paketleyen nanomedikal platformlar. Bu teknolojiler, vücudun geri kalanını güvenli bir aralıkta tutarken tümör içinde bakırı ölümcül seviyelere çıkarmayı amaçlar.
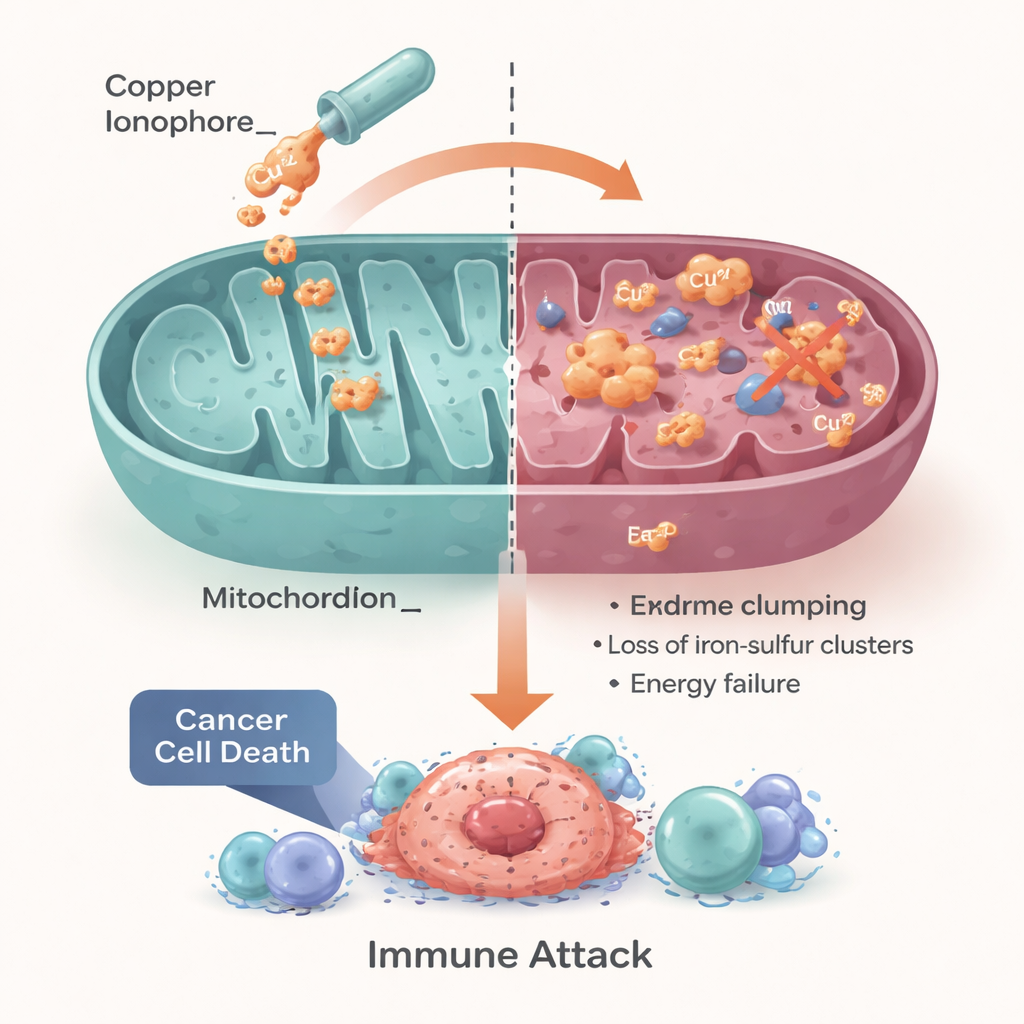
Hücresel Bir Zayıflığı Tedaviye Dönüştürmek
Yazarlar, kuproptozun temel bir hücresel ihtiyacı —bakır ve enerji yönetiminin hassas dengelenmesini— kanser için potansiyel bir Aşil topuğu haline getirdiği sonucuna varıyor. Bozulmuş bakır işleyişine sahip veya mitokondriyal metabolizmaya aşırı bağımlı kanserler, disülfiram ve elesklomol gibi yeniden amaçlandırılmış ilaçlar ile yeni nesil nanopartiküller dahil olmak üzere bakır bazlı stratejilere özellikle hassas olabilir. Ancak başarı, doğru hastayı doğru yaklaşımla eşleştirmeye; bakır taşıyıcıları, mitokondriyal aktivite ile tümörün immün ve oksijen durumunu raporlayan biyobelirteçler kullanmaya bağlı olacaktır. Bu engeller aşılabilirse, kuproptozu kullanmak günümüzde sınırlı seçeneği olan tümörleri tedavi etmek için onkologlara metal destekli yeni bir kaldıraç sağlayabilir.
Atıf: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Anahtar kelimeler: kuproptoz, bakır metabolizması, kanser tedavisi, tümör metabolizması, kanser immünoterapisi