Clear Sky Science · tr
Lizozomlardaki dinamik manyeto-mekanik kuvvet, antitümör bağışıklık için makrofajların kalıcı olarak yeniden kutuplanmasını tetikler
Bağışıklık Sistemini Uyandırmak İçin Nazik Kuvvetler Kullanmak
Kanser sıklıkla vücudun savunma mekanizmalarını uyutarak hayatta kalır. Bu çalışma, onları yeniden uyandırmanın beklenmedik bir yolunu keşfediyor: manyetik olarak hareket ettirilen nanopartiküllerle bağışıklık hücrelerinin içindeki küçük bölmeleri fiziksel olarak çekiştirerek. Araştırmacılar yalnızca ilaçlara güvenmek yerine, makrofaj adı verilen bağışıklık hücrelerini uzun süreli tümör savaşçılarına yeniden programlamak için hücre içindeki mekanik kuvvetleri dikkatle ayarlıyorlar.
Solid Tümörlerin Tedavisinin Neden Zor Olduğu
Kontrol noktası bloke edici antikorlar ve mühendislik ürünü bağışıklık hücreleri gibi modern kanser immünoterapileri bazı kanser türlerinde tedaviyi dönüştürdü. Ancak akciğer kanseri gibi katı tümörleri olan birçok hasta için bu yaklaşımlar yalnızca azınlığı faydalandırıyor. Bunun başlıca nedenlerinden biri tümör mikroçevresi. Tümörler, bağışıklığı zayıflatan hücreler ve sinyallerle dolu koruyucu bir niş tarafından çevrilidir. Tümörlere saldırabilen (M1- benzeri durum) veya onları destekleyebilen (M2- benzeri durum) makrofajlar sıklıkla tümöre yardım eden M2 moduna itilir. Bu “kötü” programlamayı kalıcı olarak tersine çevirmek, geleneksel biyokimyasal ilaçlarla tek başına zor olmuştur.
Nano parçacıkları Küçük Mekanik Motorlara Dönüştürmek
Araştırma ekibi, pozitif yüklü bir polimerle kaplanmış çinko katkılı demir oksit nanoskopik parçacıklardan oluşan manyetik nanomotorlar tasarladı; bu parçacıklar makrofajlar tarafından kolayca yutuluyor ve hücrenin geri dönüşüm ve sinyal merkezleri olan lizozomlarda yoğunlaşıyor. Hücre içine girdiklerinde, dışarıdan uygulanan dönen manyetik alan bu parçacıkların çubuk benzeri zincirler halinde dizilmesini ve dönmesini sağlayarak lizozom içindeki yoğun sıvıyı karıştırıyor ve küçük girdaplar yaratıyor. Bilgisayar simülasyonları ve model membran deneyleri, dönüş frekansı dikkatle ayarlandığında lizozomal membran üzerindeki kayma geriliminin ideal bir noktaya getirilebileceğini gösterdi: membranı kısa süreliğine sızdırır hale getirecek kadar güçlü, ancak kalıcı olarak yok edecek kadar şiddetli olmayan.
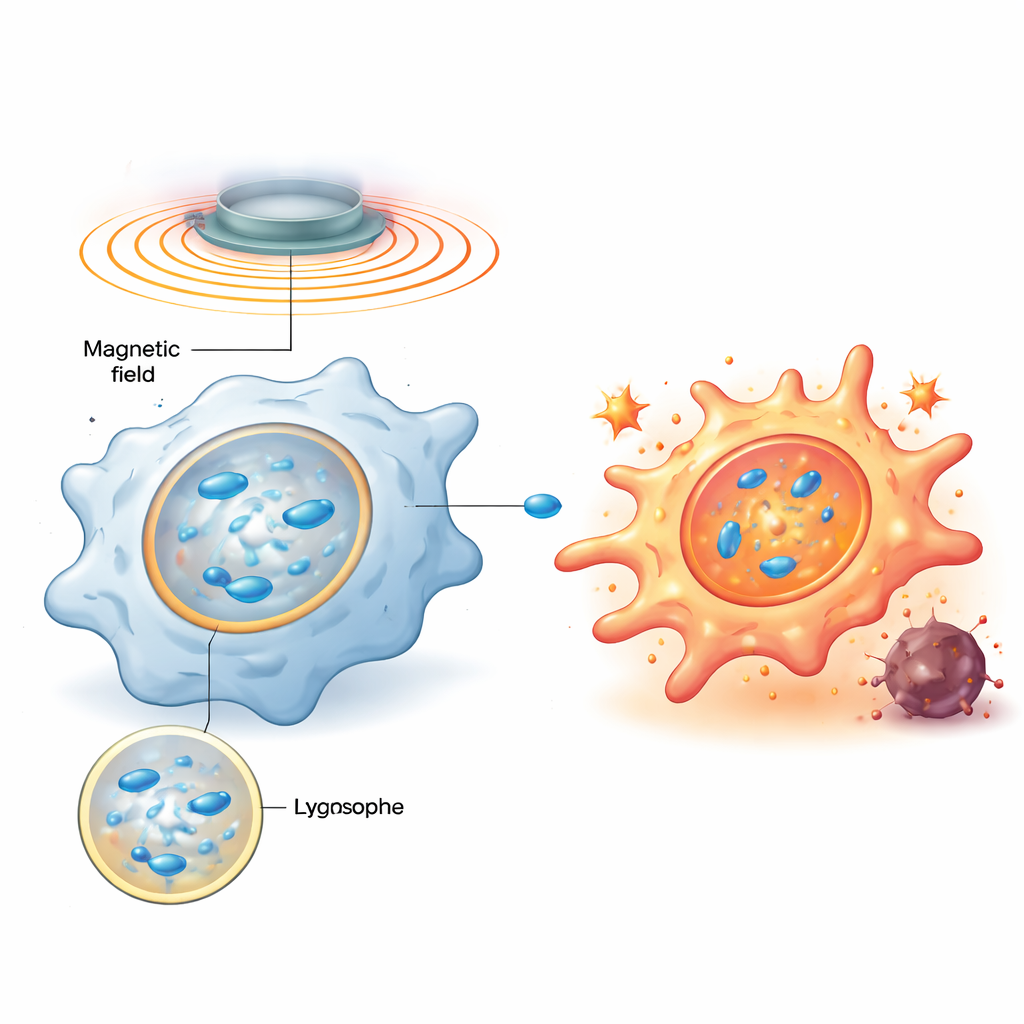
Mekanik Bir Hafif Dokunuş Biyokimyasal Bir Alarmı Tetikliyor
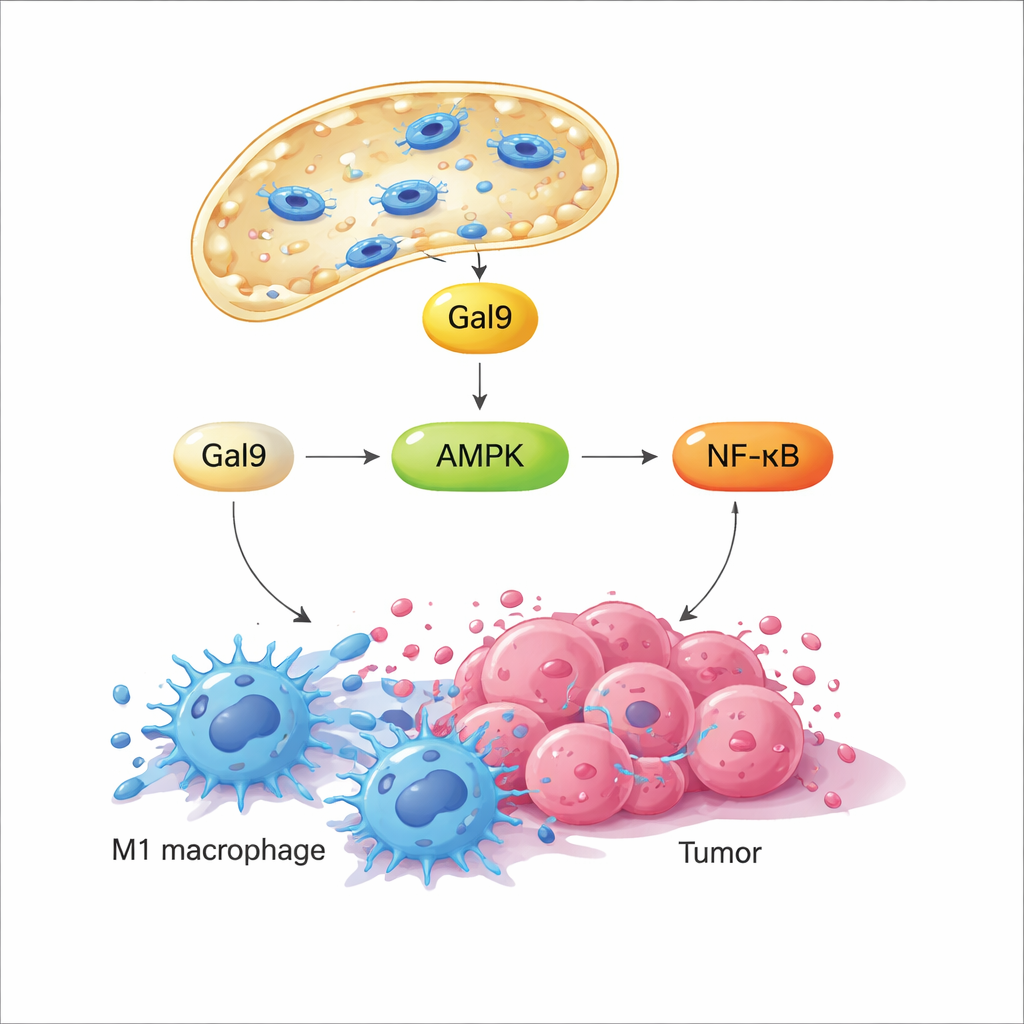
Lizozomal membran kısa süreliğine rahatsız edildiğinde, galektin-9 adlı bir şeker bağlayan protein hasarlı bölgelere hızla gelir ve bu mekanik strese duyarli bir sensör görevi görür. Çalışma, bunun sırasıyla anahtarı konumundaki enerji algılayıcı enzim AMPK’yi aktive ettiğini ve bunun da inflamatuvar ve antimikrobiyal yanıtları tetikleyen NF-κB sinyal yolunu artırdığını gösteriyor. Bu sinyaller birlikte makrofaj metabolizmasını sessiz, yakıt verimli bir durumdan hızlı glikolize doğru yeniden yönlendiriyor; bu desen düşmanca, M1-benzeri davranışla bağlantılı. Önemli olarak, manyetik alan kapatıldığında lizozom kendini onarır ve sinyal söner; alan daha sonra yeniden açıldığında aynı yol tekrar aktive edilir. Bu programlanabilir açma-kapama döngüsü, araştırmacıların hücreleri öldürmeden aynı mekanik anahtara tekrar tekrar “dokunmasına” izin veriyor.
Makrofajları Tümörle Savaşacak Şekilde Yeniden Eğitmek
Hücre kültürlerinde, manyetik olarak indüklenen bu lizozomal geçirgenlik (%MagLMP olarak adlandırılan) tümör destekleyici M2-benzeri duruma itilen makrofajları pro-enflamatuar M1-benzeri duruma çevirdi. Yeniden programlanmış bu hücreler daha fazla inflamatuar sitokin üretti ve normalde onları M2 yönüne iten tümör kaynaklı kültür ortamlarında bile günlerce M1-benzeri profilini korudu. Fare tümör modellerinde, manyetik nanomotorların tümörlere gömülmesi ve dönen alanın günlük döngülerinin uygulanması birkaç kanser türünün büyümesini yavaşlattı. Makrofajlar deneysel olarak azaltıldığında fayda büyük ölçüde ortadan kalktı; bu da bu hücrelerin tedavinin etkisinde merkezi olduğunu gösteriyor. Tümör dokusunun tek hücreli RNA dizilemesi, MagLMP’nin M1-benzeri makrofajların oranını artırdığını, antitümör nötrofilleri ve efektör CD8 T hücrelerini desteklediğini ve makrofajlar içinde NF-κB ile ilişkili ve glikoliz genlerini yukarı düzenlediğini ortaya koydu.
Yerel Kontrolden Sistemik Terapilere
Araştırmacılar daha sonra bu yaklaşımın gerçek dünya tedavisi gibi damar yoluyla verildiğinde işe yarayıp yaramayacağını sordular. Nanomotorları damar içi enjekte edip basit bir dış manyet kullanarak onları tümör içinde yoğunlaştırdılar ve tümör yatağındaki makrofajlar tarafından verimli alımı gösterdiler. Sonraki MagLMP tedavisi yine makrofajları M1-benzeri duruma kaydırdı ve tümör büyümesini baskıladı. Akciğer içinde büyüyen erken evre bir fare akciğer kanseri modelinde, manyetik yönlendirmeyi döngüsel MagLMP ile birleştirmek belirgin şekilde uzamış sağkalım sağladı: tedavi edilen farelerin yaklaşık üçte biri 300 günden fazla yaşarken, kontrol hayvanlarında yalnızca haftalar görüldü. MagLMP’yi bir PD-1 kontrol noktası inhibitörü ile birleştirmek, tedavisi zor modellerde tümör kontrolünü daha da artırdı.
İçten Dışa Bağışıklığı Kontrol Etmenin Yeni Bir Yolu
Bu çalışma, belirli bir organelde iyi kontrol edilen küçük mekanik kuvvetlerin canlı hayvanlarda bağışıklık davranışını yönlendirmek için kullanılabileceğini gösteriyor. Lizozomlara tekrar tekrar ve geri dönüşümlü olarak “dokunarak”, MagLMP galektin-9–AMPK–NF-κB eksenini aktive eder ve makrofajları hücrelere geniş çapta zarar vermeden kalıcı tümör savaşçılarına dönüştürür. Uzman olmayanlar için ana fikir, manyetik olarak sürülen nanomotorlar tarafından iletilen fiziksel ipuçlarının bağışıklık sistemi üzerinde bir düğme gibi davranabileceği; gelecekte ilaçları tamamlayacak yeni bir araç sınıfı sunabileceğidir.
Atıf: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Anahtar kelimeler: kanser immünoterapi, makrofaj yeniden programlama, manyetik nanopartiküller, mekanotransdüksiyon, lizozom sinyalleşmesi