Clear Sky Science · tr
Arşivlenmiş klinik örneklerde CmTSA süperplex teknolojisi kullanarak TME mimarilerini belirlemek için bütünleştirici mekânsal profilleme hattı
Gizli tümör çevresinin neden önemli olduğu
Kanserler izole olarak büyümez. Birbirleriyle etkileşim içinde olan bağışıklık hücreleri, destek hücreleri, kan damarları ve yara-benzeri dokudan oluşan canlı bir mahalle tarafından çevrelenir; bunlar birlikte tümörün "mikroçevresini" oluşturur. Bu makale, standart hastane doku örneklerini kullanarak bu gizli peyzajı ayrıntılı biçimde haritalamaya yönelik pratik bir yaklaşım sunuyor. Hangi hücre türlerinin yan yana bulunduğunu ve bunların yardımcı ya da zararlı mahalleler halinde nasıl organize olduğunu açığa çıkararak, yöntem doktorların bir hastanın kanserinin nasıl davranacağını ve hangi tedavilerin daha olası olarak işe yarayacağını daha iyi tahmin etmelerine yardımcı olabilir.
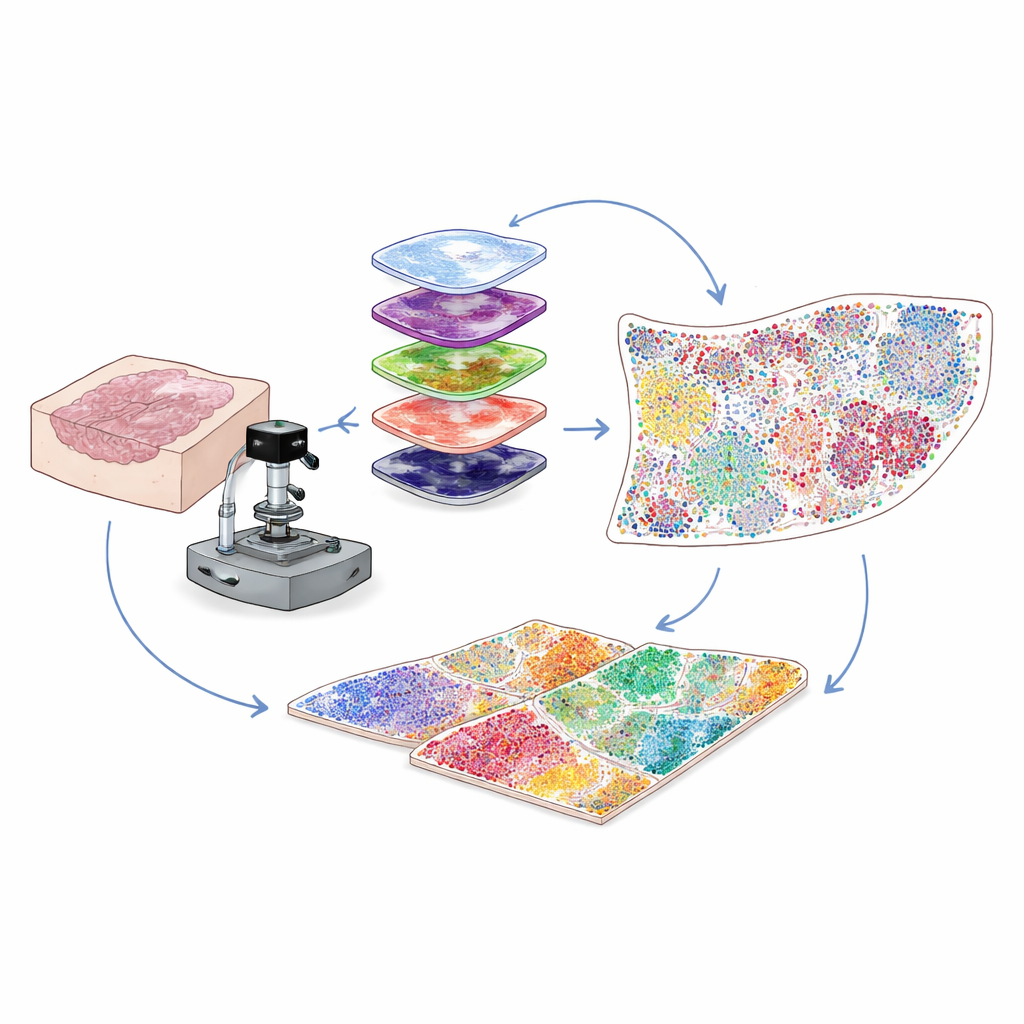
Günlük hastane örneklerinde daha fazlasını görmek
Çoğu klinik kanser örneği, yıllarca saklanabilen mum içine gömülmüş ince dilimler olarak korunur; bunlara FFPE blokları denir. Bunlar araştırma için zengin bir kaynak olsa da bilim insanlarını geri tutan teknik bir sorun vardır: bu örnekler, birçok önemli proteinden gelen zayıf sinyalleri boğan doğal arka plan floresansıyla parlar. Yazarlar bunu, dikkatle ayarlanmış güçlü bir ışığı hafif kimyasal bir işlemle birleştirerek çözdüler; böylece dokuya veya protein hedeflerine zarar vermeden bu arka plan parlamasını seçici olarak yok ettiler. Bu hibrit optik ve kimyasal "solarizasyon" aşaması görüntü netliğini keskin şekilde artırır ve aksi takdirde kaybolacak zayıf protein sinyallerinin tespit edilmesini sağlar.
Aynı dilim üzerinde düzinelerce protein etiketi boyamak
Hangi hücrelerin bulunduğunu ve ne yaptıklarını anlamak için bilim insanları dokuları belirli proteinlere bağlanan antikorlarla boyar. Geleneksel çoklu boyama yöntemleri ya nadir proteinler için zayıf sinyalle mücadele eder ya da aynı anda sınırlı sayıda belirteci izleyebilir. Burada ekip, döngüsel tyramid sinyal amplifikasyonu olarak adlandırılan bir yaklaşım kullanıyor. Her turda küçük bir belirteç seti boyanır ve enzimatik olarak parlak, kalıcı olarak bağlı floresan noktalar halinde "geliştirilir". Antikorlar daha sonra sinyal kalırken nazikçe uzaklaştırılır, arka plan yeniden solarize edilir ve bir sonraki belirteç seti eklenir. Bu döngü birçok kez tekrarlanıp hücre çekirdeklerinden gelen sabit sinalle görüntüler hizalandığında, tek bir doku diliminde tüm lam üzerindeki tek hücre çözünürlüğünde 30 ila 60 farklı proteini güvenilir şekilde görselleştirebilirler.
Renkli görüntüleri hücre hücre atlasına dönüştürmek
Yüksek çoklu görüntüler milyonlarca piksel içerir; bir insanın gözüyle analiz edebileceğinden çok daha fazladır. Bu nedenle yazarlar önce genel hücre segmentasyonu için geliştirilen derin öğrenme araçlarını kullanarak her hücre çekirdeğini bulup çevreleyen bir bilgisayarlı görü hattı kuruyor. Ardından her proteinin floresansının nerede göründüğüne—zarfta, sitoplazmada veya çekirdek içinde—ve mantıksal kurallar kümelerine göre, her hücre tümör hücresi, yardımcı T hücresi, öldürücü T hücresi, B hücresi, fibroblast veya diğerleri gibi bir tipe veya alt tipe atanır. Çıktı, lam üzerindeki her hücre için kimliğini ve kesin koordinatlarını listeleyen dijital bir tabloyu verir. Bu, karmaşık bir görüntüyü tümör mikroçevresinde kimlerin nerede olduğunu nicel bir haritaya dönüştürür.
Sonucu şekillendiren hücresel mahalleleri açığa çıkarmak
Hücreler nadiren tek başına hareket eder; önemli olan hangi komşulara sahip olduklarıdır. Bunu yakalamak için araştırmacılar her hücre etrafındaki yerel mahalleleri tanımlamanın farklı yollarını test eder ve yarıçap tabanlı bir ağ yaklaşımında karar kılarlar. Her hücre etrafına insan saçının kalınlığı kadar küçük bir çember çizdiğinizi ve içinde kimlerin yaşadığını listelediğinizi hayal edin. Çevre çemberleri benzer komşu karışımlarına sahip hücreleri gruplayarak yöntem; immün hücre açısından zengin bölgeler, fibroblast ağırlıklı bariyerler veya tümörün baskın olduğu bölgeler gibi tekrar eden "fonksiyonel nişleri" belirler. Bu stratejiyi kolon dokusunda uygulamak, yarıçap tabanlı mahallelerin alternatif yöntemlerden daha iyi bilinen anatomik yapılarla hizalandığını gösterir. İyi ve kötü sonuçlu hastalardan alınan serviks kanseri örneklerinde ekip, iyi sonuçlu hastalarda immün hücrece zengin nişlerin tümör kenarında kümelendiğini bulurken, kötü sonuçlu hastalarda tümör hücrelerini çevreleyen ve saldıran immün hücreleri dışarıda tutuyor gibi görünen kalın fibroblast yoğun bölgeler tespit eder.
Mekânsal haritalardan kişiselleştirilmiş tedaviye
Çok sayıda proteinin yüksek kaliteli, uygun maliyetli boyanmasını sağlam bir görüntü analiziyle birleştirerek bu çalışma, çok sayıda standart hastane örneğine uygulanabilecek uçtan uca bir hat sunar. Yöntem, korunmuş dokuyu tümör, immün ve stromal hücrelerin nasıl düzenlendiğine ve etkileştiğine dair ayrıntılı haritalara dönüştürür. Genel okuyucu için çıkarım şudur: yalnızca hücre türleri değil, onların kesin mahalle düzenleri de bir kanserin nasıl davrandığı açısından önemlidir. Bu platform, koruyucu immün noktaları belirlemede, baskılayıcı hücresel bariyerleri tanımlamada ve nihayetinde daha doğru prognostik değerlendirmeler ile daha hassas immünoterapi stratejilerinin geliştirilmesini desteklemede araştırmacılara yardımcı olabilir.
Atıf: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Anahtar kelimeler: tümör mikroçevresi, mekânsal proteomik, çoklu görüntüleme, kanser immünolojisi, tek hücre analizi