Clear Sky Science · tr
Nörotropik virüslerin kronobiyolojisi: ritmik viral giriş ve aritmik konak saatleri
Beyin enfeksiyonlarında zamanlamanın önemi
Kuduz ve herpes de dahil olmak üzere birçok tehlikeli virüs, beyni ve sinirleri istila etme yeteneğine sahiptir. Bu çalışma, büyük çıkarımları olan şaşırtıcı derecede basit bir soruyu ele alıyor: günün saati bu “nörotropik” virüslerin sinir sistemimize ne kadar kolay girebildiğini değiştiriyor mu ve virüsler kendi iç saatlerimizi bozabiliyor mu? Vücut saatleri ile virüsler arasındaki bu çift yönlü iletişimi anlamak; aşıların, antiviral ilaçların ve hatta vardiyalı çalışmanın zamanlamasını yeniden düşünerek riski azaltmanın yeni yollarını açabilir.
Günlük vücut saatleri ve viral kapı kolları
Vücuttaki hemen her hücre, genellikle sirkadiyen saat olarak adlandırılan yerleşik 24 saatlik bir zamanlama sistemine sahiptir. Bu sistem, BMAL1 ve REV-ERBα gibi bir dizi çekirdek saat proteini tarafından yönlendirilir ve binlerce geni ritmik dalgalar halinde açıp kapatır. Yazarlar, virüslerin hücrelere girmek için kullandığı “kapı kolları” —hücre yüzeyindeki reseptör proteinleri— üzerinde odaklandılar; bunlar, beyni hedef alan veya beyne giren onlarca virüs için geçerliydi. Kök hücrelerden yetiştirilmiş beyin benzeri organoidler, sinir kaynaklı hücre hatları ve fare dokuları incelendiğinde, bu viral reseptörlerin çoğunun gün boyunca yükselip düştüğü bulundu. Bu ritmler, saat bileşenlerinin aktivitesiyle yakından paralel seyretti; bu da günlük zamanlama sistemimizin, herhangi bir saatte kaç tane viral giriş noktasının mevcut olduğunu sessizce kontrol ettiğini gösteriyor.
Hücre döngüsü faktörü bir saat elçisine dönüşüyor
Daha derine inen araştırmacılar, genellikle hücre bölünmesini kontrol etmesiyle bilinen E2F8 adlı bir proteinin bu zamanlama ağına nasıl uyduğunu sordular. E2F8’in kendisinin sirkadiyen kontrol altında olduğunu ve en az bir kilit kuduz reseptörü olan p75NTR ile saat arasındaki bir röle gibi davrandığını keşfettiler. Saat proteini REV-ERBα aktif olduğunda E2F8’i baskılıyor. Bunun sonucunda düşük E2F8, p75NTR geninin frenini kaldırıyor, daha fazla bu reseptörün üretilmesine izin veriyor ve hücreleri kuduz virüsü için daha konuksever hale getiriyordu. Çarpıcı şekilde, E2F8 aynı zamanda saate geri bildirimde bulunuyor: REV-ERBα ve PER2 gibi çekirdek saat genlerinin kontrol bölgelerine doğrudan bağlanarak onların aktivitesini zayıflatabiliyor. Bu, bir hücre döngüsü düzenleyicisinin günlük ritimleri şekillendirmeye yardımcı olduğu ve bunlar aracılığıyla sinir hücrelerinin enfeksiyona duyarlılığını etkilediği bir geri besleme döngüsü oluşturuyor.
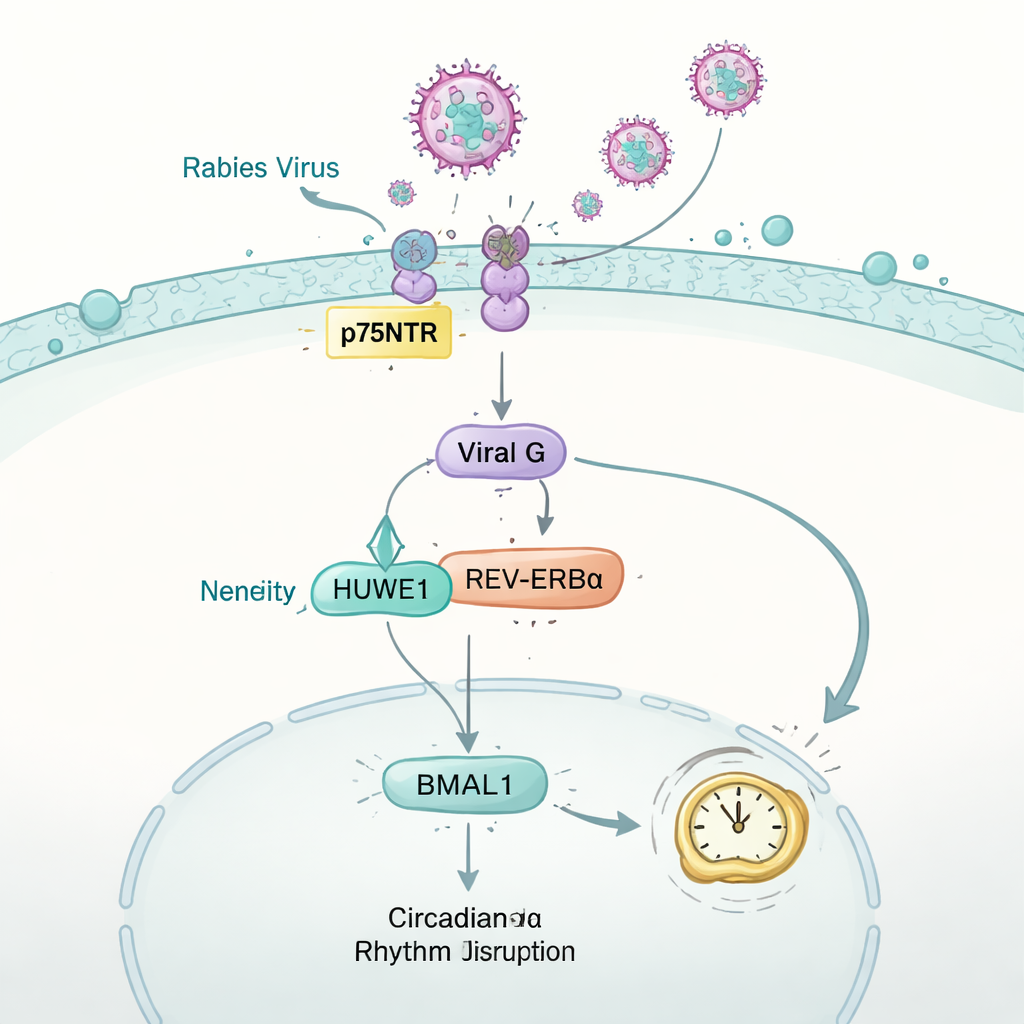
Kuduz virüsü saati nasıl şaşırtıyor
Çalışma daha sonra soruyu tersine çevirdi: bir virüs saate karşılık verebilir mi? Kuduz virüsüyle enfekte edilen fareleri kullanarak ekip, koşu aktivitesini, metabolizmayı ve solunum kimyasını izledi. Enfeksiyonun erken döneminde normal gıda alımına rağmen, hayvanlar sağlıklı farelerin gösterdiği düzenli gündüz-gece desenlerini yavaşça kaybetti. Beyinde ve birkaç organın diğerinde, kritik saat proteini BMAL1’in seviyeleri keskin şekilde düştü. Sinir benzeri hücrelerde bu etki, virüsün hücrelere kaynaşmasına yardımcı olan yüzey proteini olan kuduz glikoproteini “G” ile izlenebildi. G, genellikle diğer bir saat proteini REV-ERBα’yı bertaraf etmek için işaretleyen konak enzimi HUWE1’i ele geçirdi. HUWE1 ile rekabet ederek viral G proteini REV-ERBα’yı stabilize etti; bu da BMAL1’in daha güçlü baskılanmasına ve nihayetinde fizyolojiyi 24 saatlik bir düzende tutan saat mekanizmasının bozulmasına yol açtı.
Zamanlama, jet lag ve enfeksiyon şiddeti
Bu moleküler değişikliklerin tüm organizma açısından önemini test etmek için ekip, fareleri farklı gün saatlerinde kuduzla enfekte etti: normal ışık-karanlık döngüsü altında, kronik “jet lag” koşulları altında ve REV-ERBα eksikliği taşıyan genetik olarak değiştirilmiş hayvanlarda. Aktif (gece) fazlarının başlangıcında, p75NTR reseptörünün en yüksek olduğu dönemde enfekte edilen fareler daha hızlı kilo kaybetti, birden fazla beyin bölgesinde daha yüksek viral yük taşıdı, daha fazla beyin iltihabı gösterdi ve dinlenme fazının başlangıcında enfekte edilen farelere göre daha kısa sürede öldü. Dönen vardiya çalışmasını taklit eden tekrar eden faz kaymaları yaşayan fareler beyindeki normal saat ritimlerini kaybetti, sürekli yüksek p75NTR seviyeleri gösterdi, daha zayıf temel antiviral sinyallere sahip oldu ve daha kötü hastalık geçirdi. Buna karşılık, REV-ERBα’sız fareler daha az p75NTR ifade etti, daha düşük viral yük taşıdı ve enfeksiyon sonrası daha uzun süre hayatta kaldı; bu da bu saat bileşeninin kuduz şiddeti için kritik bir bekçi olduğunu gösteriyor.
İnsanlar için anlamı
Açıkça söylemek gerekirse, çalışma iç saatlerimizin yalnızca uyku zamanlarını ayarlamadığını; aynı zamanda beyni istila eden virüslerin kullandığı moleküler kapıları açıp kapattığını ve aynı virüslerin saati karıştırarak karşılık verebildiğini gösteriyor. Tek bir faktör olan REV-ERBα kilit bir kavşakta duruyor: E2F8 ile birlikte hem reseptör düzeylerini hem de günlük zamanlamayı şekillendiriyor; kuduz virüsü ise bunu kendi lehine kullanıyor. Bu bulgular pratik yollar öneriyor. Aşılar veya antiviral ilaçlar, reseptörlerin düşük veya bağışıklık yanıtlarının güçlü olduğu belirli saatlerde daha etkili olabilir. Sürekli bozulmuş ritimlere sahip insanlar —vardiya çalışanları veya sık seyahat edenler gibi— bazı nörotropik enfeksiyonlar açısından daha yüksek risk altında olabilir. REV-ERBα veya ilgili yolakları hedeflemek, konak lehine dengeyi değiştirmeye, enfeksiyonları daha az şiddetli hale getirmeye ve sonuçları iyileştirmeye yardımcı olabilir.
Atıf: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Anahtar kelimeler: sirkadiyen saat, nörotropik virüsler, kuduz, viral reseptörler, kronoterapi