Clear Sky Science · tr
Meme kanseri tedavisinde piroptozisin kullanımı: immünolojik mekanizmalar ve ortaya çıkan biyomateryal stratejiler
Meme Kanserine Karşı Yeni Bir Silah Olarak Hücre Ölümünü Kullanmak
Meme kanseri, dünya çapında en yaygın ve en inatçı kanserlerden biri olmaya devam ediyor. Birçok tümör sonunda cerrahi, kemoterapi ve hatta modern immünoterapilerden kaçar. Bu derleme, ortaya çıkan bir fikri inceliyor: meme tümörlerinin içinde kontrollü olarak alevli bir hücre ölümü biçimi olan piroptozisi tetiklemek. Kanser hücrelerini kontrollü, inflamatuvar bir şekilde parçalayarak bilim insanları, tümörü doğrudan öldürmeyi ve bağışıklık sistemini saldırıya katılmaya teşvik etmeyi umuyor.
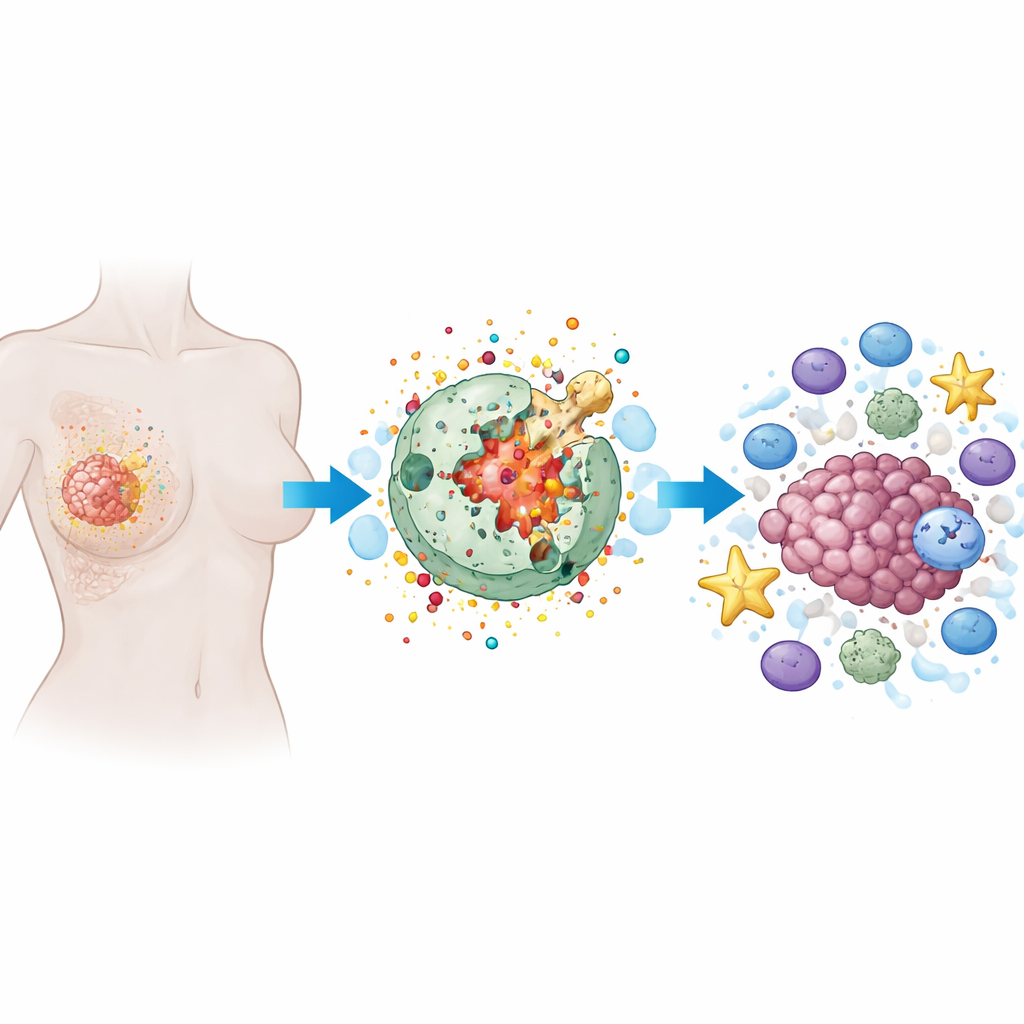
Alevli Bir Hücre Ölümünün Nasıl İşlediği
Piroptozis, hücrenin şiştiği, dış zarının gözeneklerle dolduğu ve sonunda parçalanıp içeriğini dışarı saçtığı programlı bir hücre ölümü biçimidir. Birçok terapide görülen sessiz, düzenli hücre ölümünün aksine piroptozis gürültülü ve inflamatuvardır. Özelleşmiş proteinler, özellikle gasdermin ailesi, küçük yıkım düzenekleri gibi davranır. İç enzimlerce kesildiklerinde gasderminler hücre zarında delikler açar. Bu yalnızca kanser hücresini yok etmekle kalmaz, aynı zamanda alarm sinyalleri ve inflamatuvar moleküller salarak bağışıklık hücrelerini çağırır ve aktive eder.
Meme Tümörlerini Özel Bir Zorluk Yapan Nedir?
Meme kanseri tek bir hastalık değildir; farklı davranışları olan alt tiplerin bir koleksiyonudur. Üçlü negatif meme kanseri gibi bazıları yaygın ilaç hedeflerinden yoksundur ve sıklıkla tedaviye direnç gösterir. Birçok meme tümörü "immünolojik olarak soğuk" olarak kabul edilir; yani içinde az sayıda aktif bağışıklık hücresi bulunur. Derleme, stromal hücreler, immün baskılayıcı hücreler ve yerel oksijen yetersizlikleri dahil olmak üzere meme tümörü ortamının özelliklerinin, hem piroptozis için zemin hazırlayabileceğini hem de kötü kontrol edildiğinde bu iltihabı tümör büyümesi ve yayılımı için yakıta dönüştürebileceğini açıklar. Bu iki uçlu doğa hassasiyeti özellikle önemli kılar.
Tümör Hücrelerindeki Gasdermin Anahtarları
Makalede merkezi tema, farklı gasdermin proteinlerinin meme kanseri hücreleri içinde moleküler anahtarlar olarak nasıl davrandığıdır. GSDMD ve GSDME gibi versiyonlar, kemoterapi, radyasyon veya saldıran bağışıklık hücrelerinden gelen sinyalleri tam ölçekli piroptozise dönüştürebilir. GSDMC ve bazı GSDMB formları gibi diğerleri agresif tümörlerde genellikle daha yüksek olup, nasıl aktive edildiklerine bağlı olarak hem hastalığı teşvik edebilir hem de sınırlayabilir. Birçok meme kanseri GSDME'yi kimyasal olarak susturarak piroptozisi ve bağışıklık aktivasyonunu azaltır. Doğru gasderminleri geri getirmek veya seçici olarak tetiklemek, bir terapinin sadece birkaç hücreyi öldürüp öldürmeyeceğini ya da tüm tümörü bağışıklık sistemini uyaran yerinde bir aşıya dönüştürüp dönüştürmeyeceğini belirleyebilir.
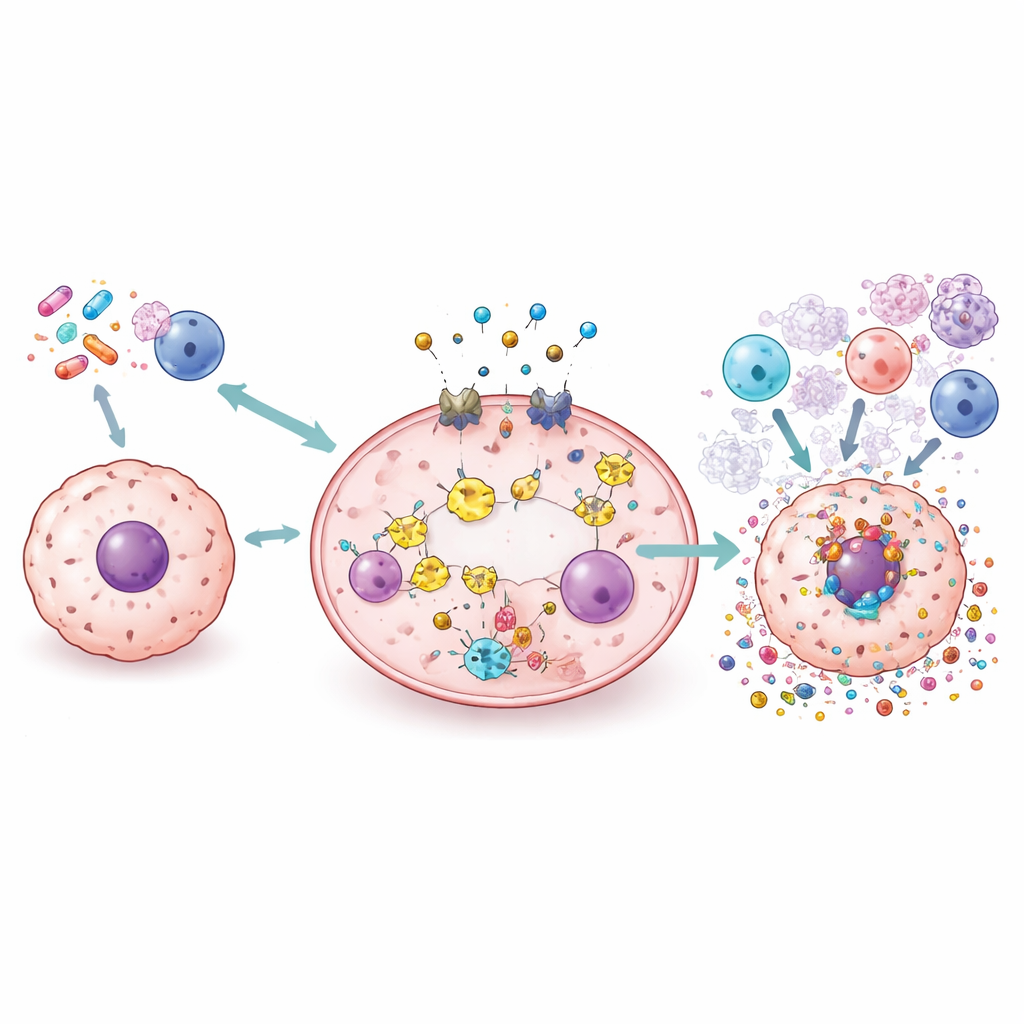
Yeni Araçlar: İlaçlar, Nanopartiküller, Virüsler ve Radyasyon
Derleme, piroptozisi güvenli şekilde kullanmak için çalışılan çok çeşitli stratejileri inceliyor. Sisplatin ve doksorubisin gibi standart ilaçlar, kanser hücrelerini sessiz ölüm yerine gasdermin kaynaklı parçalanmaya itmek için yeniden amaçlanabilir veya yeniden formüle edilebilir. Küçük moleküller, inflamasyonu ince ayarlamak için yolun belli bölümlerini güçlendirebilir veya engelleyebilir. Nanopartiküller ve biyomimetik taşıyıcılar, kemoterapi, bakır iyonları veya ışıkla aktive olan molekülleri doğrudan tümörlere teslim etmek üzere tasarlanıyor; burada sağlıklı dokuları korurken piroptozisi tetikliyorlar. Onkolitik virüsler ve radyoterapi de piroptozisi provoke etmek ve tümörün immün manzarasını yeniden şekillendirmek için mühendislik yapılabilir veya diğer ajanlarla kombine edilebilir; bu, bağışıklık kontrol noktası ilaçlarını daha etkili hale getirebilir.
Güçlü Faydalar ile Gerçek Riskler Arasında Denge Kurmak
Piroptozis çok inflamatuvar olduğu için, bağışıklık sisteminin kansere karşı mücadelede yardımcı olan aynı reaksiyonlar normal dokulara zarar verebilir veya kronik hale gelirse tümör büyümesini teşvik edebilir. Yazarlar, hangi hastaların en çok fayda sağlayacağını ve kimin tehlikeli "sitokin fırtınası" riski altında olduğunu belirlemeye yardımcı olabilecek erken biyobelirteçlere—gen imzaları, metilasyon desenleri, kanda gazdermin protein parçacıkları ve sitokin profilleri gibi—dikkat çekiyor. İleri nanomedisin tasarımları, dikkatle seçilmiş ilaç kombinasyonları ve inflamatuvar belirteçlerin gerçek zamanlı izlenmesi, yanıtı keskin ama kontrollü tutmak için araştırılan yaklaşımlar arasında yer alıyor.
Gelecekteki Hastalar İçin Ne Anlama Gelebilir
Basitçe söylemek gerekirse, bu derleme kanser hücrelerini "yüksek sesle öldürmenin" meme kanseri bakımını dönüştürebileceğini savunuyor. Piroptozisi tümör hücrelerinin hassas bir alt kümesinde tetikleyerek doktorlar hem tümörü küçültebilir hem de soğuk tümörleri ısıtarak modern immünoterapilere daha duyarlı hale getiren güçlü, kalıcı bir bağışıklık yanıtını uyandırabilir. Ancak piroptozis değişken bir müttefiktir: çok geniş veya çok uzun süre serbest bırakılırsa iltihabı kötüleştirebilir veya dirençli hücrelerin gelişmesini teşvik edebilir. Gelecek araştırmalar, kimlerin fayda sağlayacağını haritalamaya, hedefe yönelik teslimat sistemlerini mükemmelleştirmeye ve piroptozis indükleyici yaklaşımları immün ilaçlarla birleştiren klinik deneyler yürütmeye odaklanacak. Bu zorluklar çözülebilirse, piroptozisin kullanımı meme kanseri tedavisine güçlü yeni bir boyut katabilir.
Atıf: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Anahtar kelimeler: piroptozis, meme kanseri, gasdermin, tümör mikroçevresi, nanomedisin