Clear Sky Science · tr
Mutlak dinamik ve göreli statik: kanser gelişiminde glikoliz ve OXPHOS ilişkisi
Kanserin Enerji Tercihleri Neden Önemli?
Kanser hücreleri aşırı dayanıklılık sporcularına benzer: büyümek, yayılmak ve tedaviden kaçınmak için sürekli enerji sağlamak zorundadırlar. Bu derleme, tümör hücrelerinin iki ana enerji sistemine—biri hızlı, diğeri verimli—nasıl başvurduğunu ve daha da önemlisi bunları nasıl karıştırıp aralarında nasıl geçiş yaptığını açıklar. Bu değişen enerji stratejilerini anlamak, hastalığın tüm seyri boyunca tanı ve tedaviye yeni bir bakış açısı sunar.
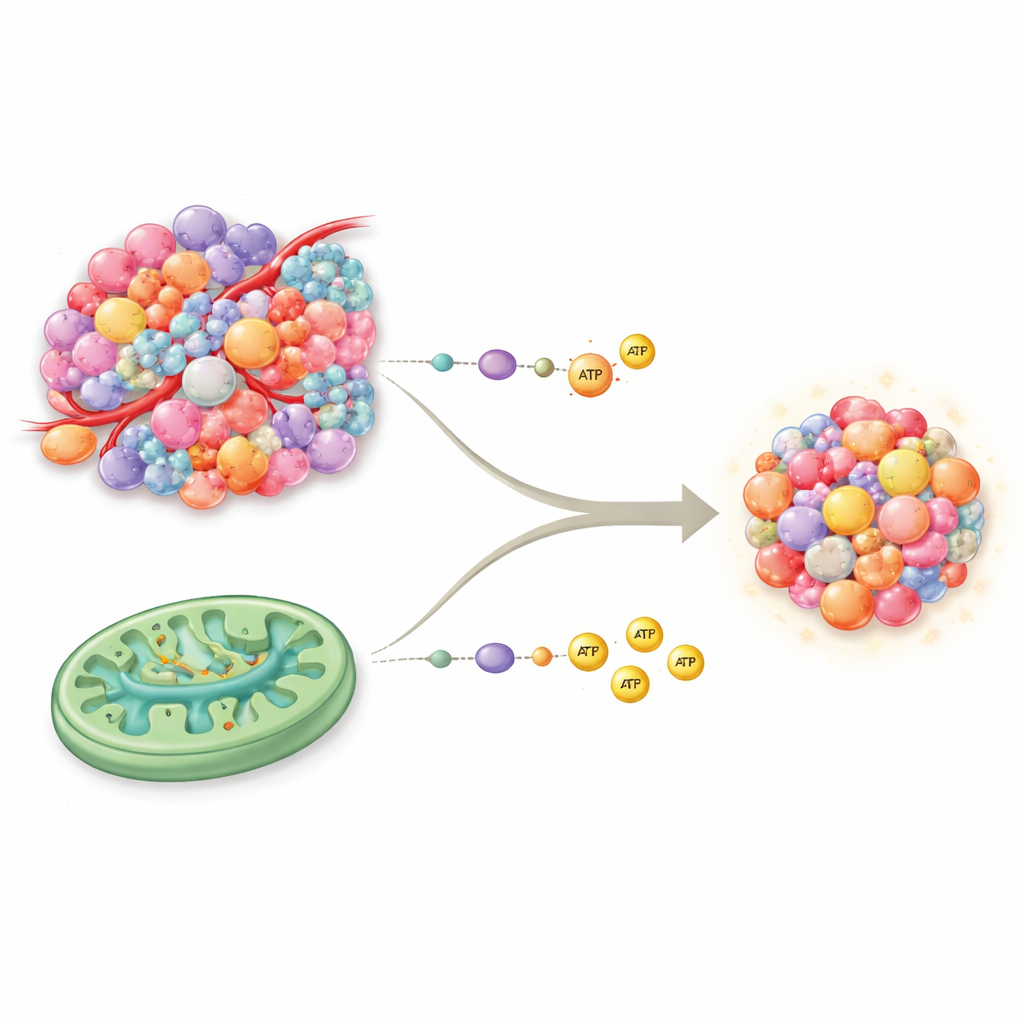
Hücrelerin Enerji Ürettiği İki Ana Yol
Hücrelerimiz tipik olarak enerjiyi iki temel yol üzerinden üretir. Glikoliz hızlı, “anında nakit” sistemi gibidir: şekeri çabucak parçalar ancak birim başına nispeten az enerji sağlar. Oksidatif fosforilasyon (OXPHOS) mitokondri içinde çalışır ve yüksek verimli bir enerji santrali gibi daha fazla enerji üretir; bunun için iyi oksijen ve besin temini gerekir. On yıllar boyunca kanserin, oksijen mevcut olsa bile neredeyse yalnızca glikolize dayandığı—Warburg etkisi olarak bilinen—düşünülmüştür. Yeni bulgular bu basit görüşü bozuyor: birçok tümörde tamamen işleyen mitokondriler bulunur ve OXPHOS ile trikarboksilik asit (TCA) döngüsünü glikolizle birlikte kullanarak önceki düşüncelerden daha zengin ve esnek bir enerji araç setine sahip olurlar.
Çok Çeşitli Hücre Tipleri, Çok Sayıda Enerji Seçeneği
Bir tümör tekdüze bir kütle değildir. Kanser hücreleri, destek hücreleri, kan damarları ve bağışıklık hücrelerini içeren küçük bir ekosistemdir ve her birinin farklı yakıt gereksinimleri vardır. Bazı kanser hücreleri kan damarlarına yakın olup bol oksijen ve besin alırken; bazıları kötü beslenen derin bölgelerde gömülüdür. Sonuç olarak aynı tümör içindeki hücreler glikolizi tercih edebilir, ağırlıklı olarak OXPHOS’a güvenebilir veya her ikisini aynı anda kullanabilir. Bu metabolik çeşitlilik—heterojenite olarak adlandırılır—kan akışı, besin düzeyleri, hücre tipi ve çevresel sinyallerdeki farklılıklardan kaynaklanır. Buna ek olarak, tümörler sıklıkla metabolik simbiyoz gösterir: glikolitik hücreler laktatı atık benzeri bir ürün olarak dışarı verir; komşu OXPHOS’a dayanan hücreler ise bu laktatı değerli bir yakıt olarak içeri alıp yakar. Benzer laktat paylaşımı, fibroblastlar, damar hücreleri ve immün baskılayıcı hücreler gibi destek hücreleriyle de gerçekleşir; bunların tümü tümörün büyümesine ve tedaviye direnmesine kolektif olarak yardımcı olur.
Sürekli Değişim: Tümör Enerjisinin Zaman İçinde Kayması
Tümör metabolizması yalnızca belirli bir anda çeşitli olmakla kalmaz; aynı zamanda son derece dinamiktir. Tümörler büyüdükçe düşük oksijen, asit birikimi, besin eksikliği ve doku sertliğindeki değişimler gibi değişen koşullarla karşılaşırlar. Sert, düşük oksijenli koşullar altında birçok kanser hücresi glikolize kayar. Asit birikimi veya şeker kıtlığı durumunda ise daha fazla OXPHOS’a yönelme görülebilir. Aynı esneklik biyolojik dönüm noktalarında da ortaya çıkar. Hızla bölünen hücreler yeni DNA, yağ ve zarlar için yapı taşları üretmek üzere glikolize dayanma eğilimindedir. Dinlenen veya dolaşımdaki hücreler genellikle daha çok OXPHOS’a bağımlıdır. İnvazyon ve metastaz sırasında kanser hücreleri yakıt tercihlerini sürekli ayarlar: bazı adımlar glikolizi, diğerleri OXPHOS’u destekler ve yeni organları kolonize eden metastatik hücreler varış dokusunun “toprağına” uyacak şekilde metabolizmalarını ayarlar.
Geçişin Arkasındaki Genler, Enzimler ve ‘Enerji Santralleri’
Hücre makinerisinin derinliklerinde genler ve enzimler bu enerji kararlarını yönlendirir. Onkogenler ve tümör baskılayıcılar hücreleri glikolize veya OXPHOS’a itebilir ya da her ikisini birden artırmalarını sağlayabilir. Sitrik asit, sukkinat veya isositrik asit gibi ana TCA enzimlerindeki mutasyonlar veya değişiklikler dengeyi kaydırabilir ve bazen kan damarı büyümesi ve invazyon gibi kanserle ilişkili sinyalleri tetikler. Pirüvat kinaz M2 gibi, şeker kökenli karbonun enerji mi yoksa yapı malzemesi mi olacağına karar veren kritik kavşaklardaki enzimler glikoliz ile mitokondri fonksiyonunu birbirine bağlar. Bu arada tümör bölgeleri arasındaki mitokondri sayısı, yapısı ve performansındaki farklılıklar olası enerji durumları yelpazesini daha da genişletir.
Hareketli Bir Enerji Hedefi Üzerinden Tedaviyi Yeniden Düşünmek
Tümör hücreleri glikoliz ile OXPHOS arasında geçiş yapabildiği için yalnızca bir yolu engellemek genellikle yeterli değildir; kanser yakıt kullanımını yeniden yönlendirip hayatta kalabilir. Yazarlar, kanserin enerji metabolizmasının ancak kısa süreli olarak stabil olduğunu ve temelde sürekli değiştiğini savunur. Tümörleri “enerji metabolizması spektrumu” üzerinden, tek seferlik değil zaman içinde ölçülmesi gereken bir bakışla görmeyi önerirler. Pratikte bu, farklı hastalık evrelerinde bir tümörün yakıt tercihlerini izlemesi ve glikoliz ile OXPHOS inhibitörlerini kişiselleştirilmiş kombinasyonlarda eşleştirmesi anlamına gelebilir. Böyle dinamik, metabolizmaya yön veren tedavi stratejileri tümörün enerji kaynağını daha iyi kesebilir, uyum sağlama kabiliyetini sınırlayabilir ve hastalığın uzun dönem kontrolünü iyileştirebilir.
Atıf: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Anahtar kelimeler: kanser metabolizması, glikoliz, oksidatif fosforilasyon, tümör mikroçevresi, metabolik plastisite