Clear Sky Science · tr
Eksozomal S100A9, adenoid kistik karsinomun akciğer metastazını kanser ilişkili fibroblastları aktive ederek teşvik ediyor
Sessiz bir tükürük bezi kanseri akciğerlere nasıl ulaşır
Adenoid kistik karsinom, genellikle tükürük bezlerinde başlayan, yavaş büyüyen ancak inatçı bir kanserdir ve bazen ilk tümör çıkarıldıktan yıllar sonra akciğerlerde yeniden ortaya çıkar. Hastalar ve yakınları için bu gecikmiş yayılım korkutucu ve öngörülmesi ya da önlenmesi güçtür. Bu çalışma, tümör hücrelerinin uzak akciğer dokusunu gizlice kanser istilasına hazırlama biçimini çözümleyerek tümör hücreleri ile çevresindeki destek hücreleri arasındaki gizli konuşmayı ortaya koyuyor; bu, nihayet tedavi için yeni hedefler sunabilir.
Uzayan ve Tekrarlayan Bir Kanser
Adenoid kistik karsinom (AKK), baş ve boyun bölgesindeki bezlerin, özellikle tükürük bezlerinin kanseridir. Cerrahi ve radyasyon genellikle primer tümörü kontrol altına alabilir, ancak birçok hasta sonunda akciğer metastazı geliştirir; bunlar ölümün başlıca nedenidir. Yaygın AKK için mevcut ilaçlar sınırlıdır; bunun bir nedeni de birincil tümörden gelen hücrelerin akciğerlere yerleşip büyümeyi nasıl başardığını bilim insanlarının tam olarak anlamamış olmasıdır. Bu makalenin yazarları, AKK hücrelerinin çevrelerini yeniden şekillendirip gelecekteki akciğer tümörleri için ‘uygun bir zemin’ oluşturmasına izin veren kilit sinyalleri tanımlamayı amaçladılar.
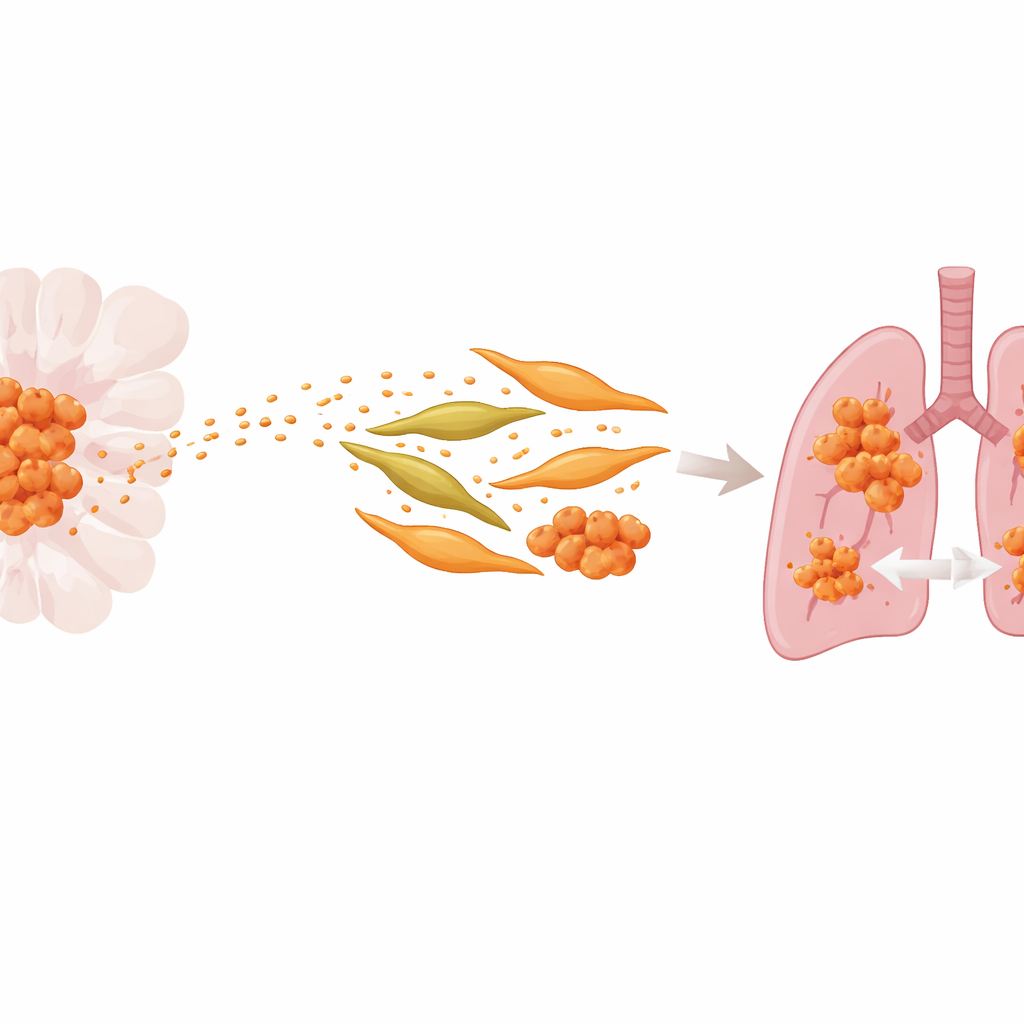
Büyük etkiye sahip küçük paketler
Araştırmacılar, kanser hücrelerinin kana saldığı, zarla çevrili küçük kabarcıklar olan eksozomlara odaklandı. Bu veziküller, diğer hücreleri uzaktan yeniden programlayabilecek proteinler ve genetik materyal taşır. Standart bir AKK hücre hattı ile güçlü akciğer yayılma yeteneği için seçilmiş bir versiyonu karşılaştırarak ekip, agresif hücrelerde ve bunların eksozomlarında iltihapla ilişkili S100A9 adlı proteinin zenginleştiğini buldu. Tümörlerinde ve kan eksozomlarında daha fazla S100A9 bulunan hastalar, akciğer metastazı geliştirme ve hastalıksız kalma sürelerinin daha kısa olması açısından daha yüksek risk taşıyordu; bu da bu proteinin kanser yayılımını desteklemeye yardımcı olduğunu düşündürüyor.
Tümörün destek ekibini yeniden kablolamak
Tek hücre RNA dizi analizi kullanarak yazarlar, AKK tümörleri ve çevresindeki normal bezlerdeki tüm hücre tiplerinin ayrıntılı bir haritasını oluşturdu. Tümörün epitel hücreleri ile çevredeki fibroblastlar—bağ dokusu üreten yapısal hücreler—arasında yoğun bir iletişim keşfettiler. Kanserde bu fibroblastlar “rekrute” edilip kanser ilişkili fibroblastlara (CAF'ler) dönüşebilir; bunlar dokuyu sertleştirir, iltihabı körükler ve kanser hücrelerinin göç etmesine yardımcı olur. Çalışma, agresif AKK hücrelerinden gelen S100A9 açısından zengin eksozomların normal fibroblastları aktive edilmiş CAF'lere dönüştürebileceğini gösterdi: bu hücreler daha kasılgan, daha hareketli hale geldi ve dokuyu yeniden düzenleyen enzimler ile tümör büyümesini destekleyen inflamatuar moleküller üretmeye başladı.
Yerel sinyallerden akciğer kolonilerine
Ardından ekip, eksozomla aktive edilmiş bu fibroblastların gerçekten AKK'nin akciğerleri kolonize etmesini kolaylaştırıp kolaylaştırmadığını sordu. Fare modellerinde, S100A9 yüklü eksozomların kan dolaşımına enjekte edilmesi akciğerleri hazırladı: oradaki fibroblastlar aktivasyon belirteçlerini açtı ve akciğer dokusu yeni damar oluşumu ve matriks parçalanmasıyla ilişkili faktörleri ifade etmeye başladı. Daha sonra AKK hücreleri verildiğinde S100A9 eksozomlarıyla ön işlem uygulanmış fareler daha fazla ve daha büyük akciğer metastazları geliştirdi. Daha ileri analizler, bu sürecin IL-17 öncülüğündeki enflamatuar sinyaller zincirine, ayrıca TNF ve NF-κB'ye dayandığını; bunların birlikte fibroblast aktivasyonunu güçlendirip akciğer mikroçevresini yeniden şekillendirdiğini gösterdi.
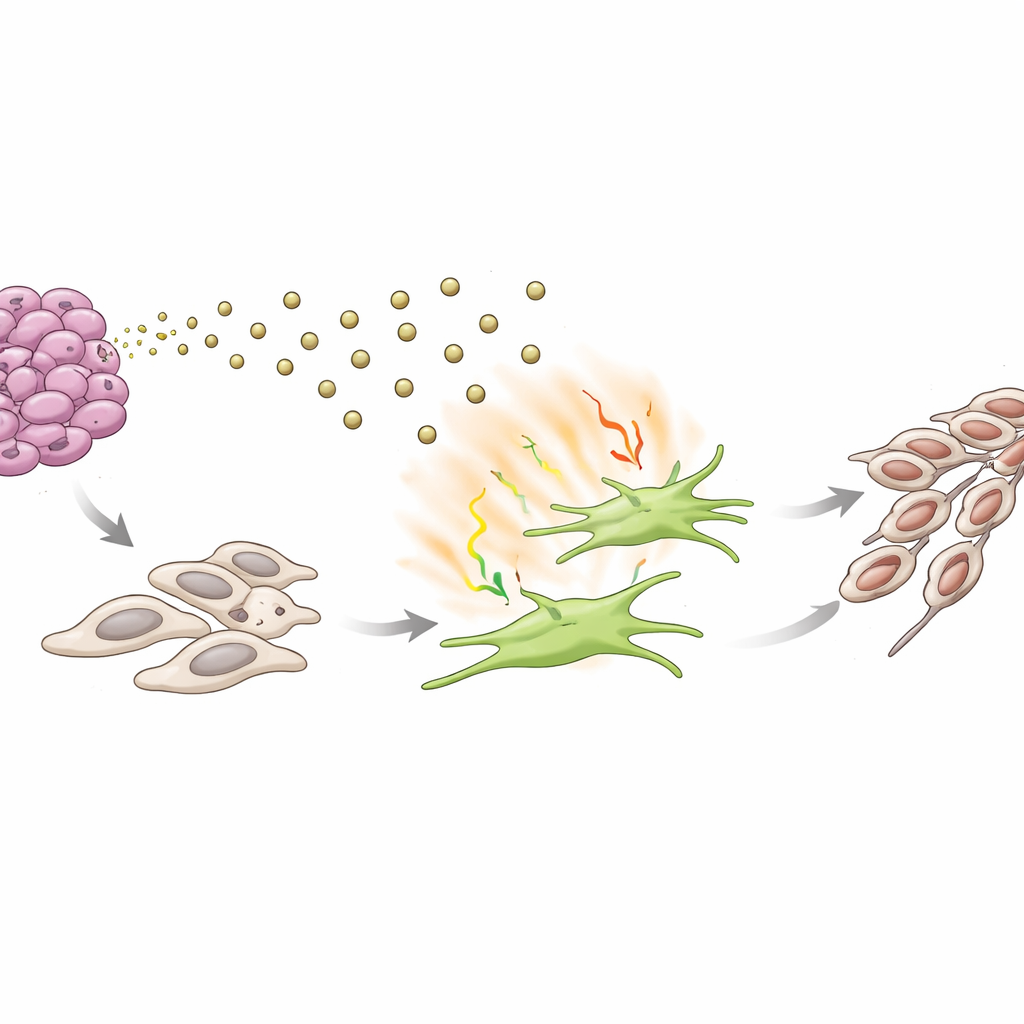
Kanseri şekil değiştirmeye iten kısır döngü
Laboratuvar eş-kültür sistemlerinde, S100A9 açısından zengin eksozomlarla veya IL-17 odaklı bu sinyal yoluyla “eğitilmiş” fibroblastlar, yakınlarındaki AKK hücrelerini daha agresif hale getirdi. Kanser hücreleri daha iyi hareket ediyor, bariyerleri daha kolay aşıyor, koloniler oluşturuyor ve metastaza doğru kilit bir adım olan epitel–mezenkimal dönüşümle ilişkili daha mobil, iğsi bir form alıyordu. IL-17'yi nötralize eden bir antikorun engellenmesi bu değişikliklerin çoğunu tersine çevirdi; yalnızca saflaştırılmış IL-17 eklenmesi ise AKK hücrelerini daha invaziv bir duruma itti. Birlikte, bu bulgular kendini güçlendiren bir döngüyü özetliyor: tümör hücreleri fibroblastları aktive etmek için eksozomlarında S100A9 gönderir; aktive olmuş fibroblastlar IL-17 ve diğer sinyalleri salarak tümör hücrelerini yayılmaya daha yatkın hale getirir.
Gizli iletişim döngüsünü kırmak
Bir uzman olmayan için mesaj şudur: AKK'nin akciğerlere yayılması tesadüfi değildir. Birincil tümör, destek hücrelerini ve uzak dokuları, küçük protein dolu paketler aracılığıyla başka yerde büyümesine yardımcı olacak şekilde gizlice eğitir. Bu çalışma, S100A9 ve aşağı yönlü IL-17 sinyal yolunu bu sürecin merkezi düğümleri olarak tanımlıyor. Bu iletişim eksenini hedefleyerek—S100A9'u bloke etmek, IL-17 sinyalini zayıflatmak veya fibroblast aktivasyonunu bozmak—gelecekteki tedaviler, akciğer metastazının “hazırlık aşamasını” kesintiye uğratabilir ve klinisyenlere bu sessiz ama tehlikeli kanserin başlangıç noktasından uzaklarda yeniden ortaya çıkmasını önlemek için yeni yollar verebilir.
Atıf: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
Anahtar kelimeler: adenoid kistik karsinom, eksozomlar, kanser ilişkili fibroblastlar, akciğer metastazı, S100A9 IL-17 ekseni