Clear Sky Science · tr
APOA2 aracılı endoteliyal mezenkimal geçiş ve kanser lipid metabolizması yeniden programlanması, TGF-β yoluyla antianjiyogenik ilaç direnci kazandırır
Bu keşfin hastalar için önemi
Doktorlar karaciğer tümörlerini kan akışını keserek beslenmelerini engelleyen ilaçları giderek daha sık kullanıyor, ancak birçok hastada başlangıçtaki faydanın ardından kanserler ilaca yanıt vermeyi bırakıyor. Bu çalışma önemli bir soruyu ele alıyor: Neden bazı karaciğer kanserleri bu damarları engelleyen tedavilere dirençli hale geliyor ve onları nasıl yenebiliriz? Araştırmacılar, damarsal yapıları ve tümörlerin enerji kullanımını yeniden programlamasına izin veren, kan yağ proteini ile güçlü bir büyüme sinyali arasındaki gizli iş birliğini ortaya koyuyor; bu da zor tedavi edilen bir kanser için farklı bir tedavi yoluna işaret ediyor.
Alışılmış can suyunu olmadan yaşamayı öğrenen bir tümör
Hepatosellüler karsinom, karaciğer kanserinin en yaygın biçimi, büyümek için yeni kan damarlarına büyük ölçüde bağımlıdır. İleri hastalık için standart ilaçlar VEGF ve reseptörü VEGFR2 etrafında odaklanan önemli bir damar büyüme yolunu bloke edecek şekilde tasarlanır. Ancak birçok hastada tümörler bu ilaçlara rağmen büyümeye devam eder. Apatinib adlı antianjiyogenik ilaca yanıt veren ve yanıt vermeyen hastalardan alınan tümör örneklerini karşılaştırarak, yazarlar APOA2 adlı bir genin öne çıktığını buldular. Dirençli hastaların tümörlerinde, kanda yağ taşımasındaki rolüyle en çok bilinen bir protein olan APOA2 seviyeleri önemli ölçüde yüksekti. Bu, APOA2'nin tümörlerin damar hedefli ilaçlardan kaçmasına yardımcı olabileceği olasılığını gündeme getirdi.
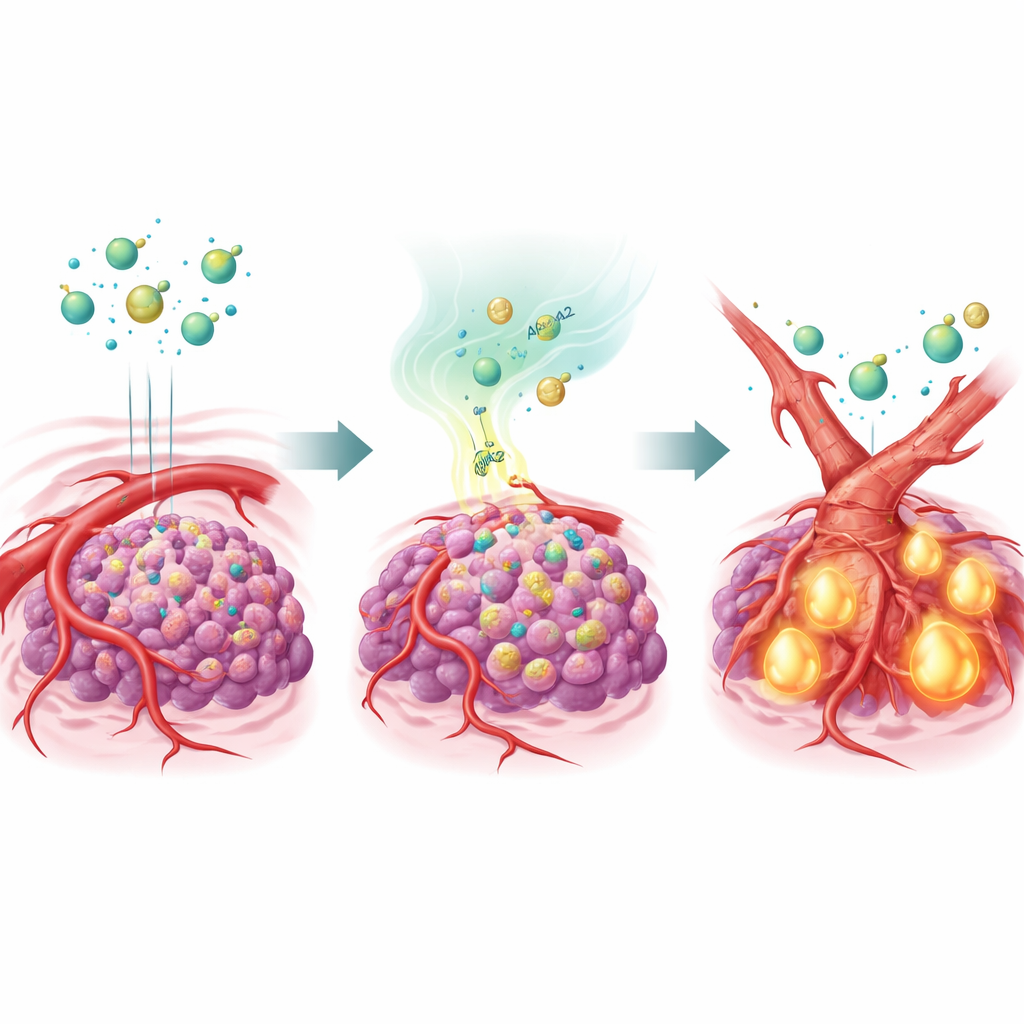
Damarları yeniden şekillendiren bir yağ taşıma proteini
Bu fikri test etmek için ekip, karaciğer kanseri hücrelerini APOA2 fazlaca üretecek şekilde mühendislik yaptı ve bunları farelere nakletti. Birkaç farklı antianjiyogenik ilaçla tedavi edildiğinde, bu APOA2 açısından zengin tümörler büyük ölçüde tedaviyi görmezden geldi: damarları korundu ve kanserler büyümeye devam etti. Ayrıntılı analiz, TGF-β adlı ana sinyalin bu tümörlerde güçlü biçimde etkinleştiğini ve bunun hem tümör mikrosferasındaki hem de hayvanların kanındaki düzeylerinin yükseldiğini gösterdi. TGF-β, damarların iç yüzeyini döşeyen hücrelere etki ederek onların endoteliyalden mezenkimal bir kimliğe geçtiği endoteliyal-mezenkimal geçiş sürecini tetikledi. Bu hücreler daha skar benzeri, mezenkimal bir duruma kayarken VEGFR2'nin çoğunu kaybetti; oysa antianjiyogenik ilaçların hedeflediği tam da bu reseptördü. Sonuç olarak damarlar, ilaçların artık hedefleyemeyeceği bir biçime yeniden yapılandı.
Kanser hücrelerini beslemeye devam ettiren metabolik bir sapma
Hikâye damar duvarında bitmedi. APOA2 tarafından tetiklenen aynı TGF-β sinyali, kanser hücrelerinin enerji sağlama biçimini de yeniden programladı. Şeker parçalanmasına (glikolize) ağırlık vermek yerine, APOA2 yüksek hücreler çevrelerinden daha fazla serbest yağ asidi çekmeye ve bunları mitokondrilerinde yağ asidi oksidasyonu yoluyla yakmaya başladı. Besin kullanımı ve oksijen tüketimini ölçen deneyler, bu hücrelerin enerji kaynağı olarak yağa daha bağımlı hale geldiğini ve daha fazla hücresel yakıt (ATP) ürettiğini gösterdi. Bu değişim, antianjiyogenik tedavinin kan akışını baskılamasına rağmen tümör hücrelerinin hızla bölünmeye devam etmesine ve hücre ölümünden kaçınmasına olanak sağladı.
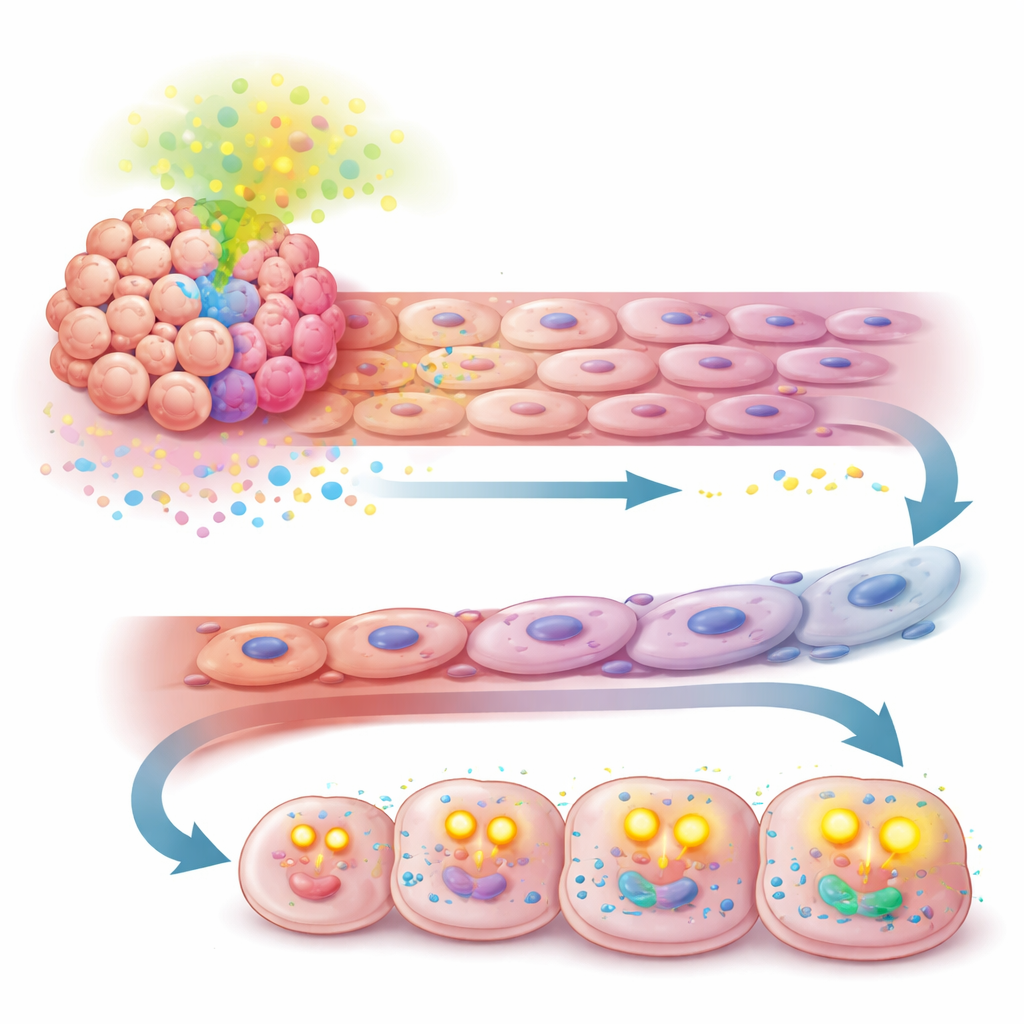
Zayıflığı yeni bir tedavi hedefine dönüştürmek
Önemli olarak, araştırmacılar TGF-β'yi bloke ettiğinde APOA2'nin sağladığı avantajlar çöktü. Fare modellerinde bu sinyalin engellenmesi, anormal damar değişikliklerini azalttı, tedaviye duyarlılığı geri getirdi ve tümör büyümesini yavaşlattı. Daha da ümit verici olarak, TGF-β ile birlikte immün kontrol noktası PD-1'i eşzamanlı olarak bloke eden çift etkili bir antikor, APOA2 yüksek tümörlerde tek başına kullanılan yaklaşımlardan daha iyi sonuç verdi. Bu bulgular, APOA2 yüksek olan bir alt gruptaki karaciğer kanserlerinin sessizce bağımlılığını alışılmış VEGF yolundan, hem damarları hem de tümör metabolizmasını sürdüren TGF-β merkezli bir yola kaydırdığını düşündürüyor.
Gelecekteki karaciğer kanseri bakımına etkisi
Halk açısından ana mesaj şudur: Bazı karaciğer tümörleri, hem boru hattını (damar yapısını) hem de güç kaynağını yeniden düzenleyerek mevcut damar hedefli ilaçlardan kaçıyor. Yağ ilişkili bir protein olan APOA2, TGF-β sinyalini yükseltiyor; bu da damarları mevcut ilaçların görmesini engelleyecek şekilde gizliyor ve kanser hücrelerine şeker yerine yağla yaşamayı öğretiyor. Çalışma, tümörleri APOA2 açısından test etmenin, standart antianjiyogenik ilaçlardan yararlanması olası olmayan ancak özellikle TGF-β'yi bloke eden ilaçlarla, modern immünoterapiyle kombinasyon halinde yanıt verebilecek hastaları belirleyebileceğini öne sürüyor. Kısacası, tümörlerin nasıl uyum sağladığını açığa çıkararak bu çalışma, hem damarları hem de bu dirençli kanserlerin dayandığı enerji kaynağını hedef alan daha kişiselleştirilmiş bir stratejiye işaret ediyor.
Atıf: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Anahtar kelimeler: hepatosellüler karsinom, antianjiyogenik direnç, APOA2, TGF-beta sinyalizasyonu, kanser lipid metabolizması