Clear Sky Science · tr
KCTD1, c-Myc’i stabilize ederek PD-L1’i yukarıya çeker ve hepatosellüler karsinomda antitümör bağışıklığı baskılar
Gelecekteki kanser bakımında bunun önemi
Karaciğer kanseriyle yaşayan birçok hasta, vücudun kendi T hücrelerini tümörlere karşı serbest bırakmak üzere tasarlanmış günümüzün en umut verici immünoterapilerinden fayda görmüyor. Bu çalışma, hepatosellüler karsinom olarak adlandırılan yaygın bir karaciğer kanseri türünün tedavi sırasında bile immün saldırıdan nasıl kaçabildiğini araştırıyor ve mevcut immünoterapi ilaçlarının daha etkili olmasını sağlayabilecek KCTD1 adlı yeni bir moleküler anahtarı tanımlıyor.
Tümör “kapatma anahtarlarının” gizli yardımcısı
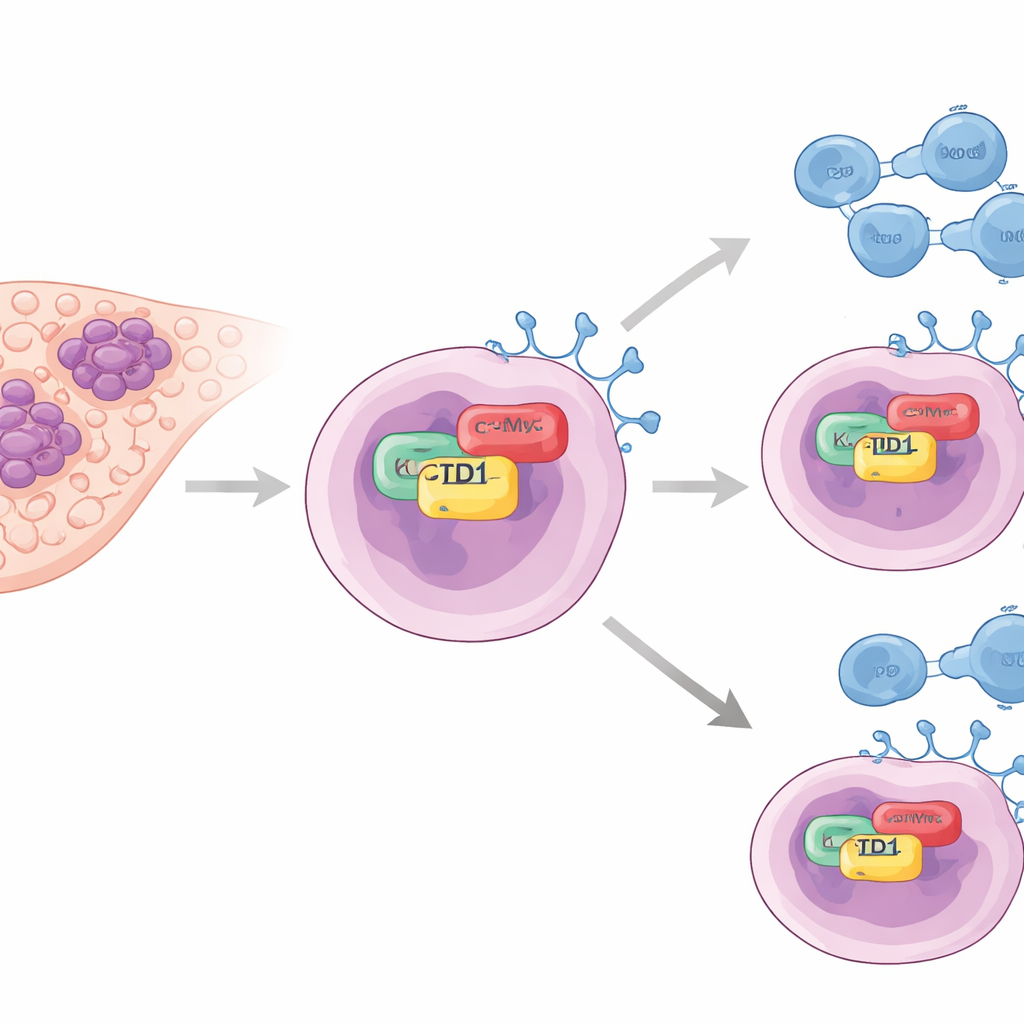
Yazarlar, daha önce karaciğer tümörü büyümesiyle ilişkilendirilmiş ancak immün kaçışta iyi incelenmemiş KCTD1 adlı bir proteine odaklandı. Hastalardan alınan tümör örneklerinde, KCTD1 seviyelerinin normal karaciğer dokusuna göre kanserli dokuda belirgin biçimde daha yüksek olduğunu buldular. Önemli olarak, KCTD1 bakımından zengin tümörler ayrıca T hücrelerindeki PD-1’e bağlanıp immün sistemi susturan yüzey proteini PD-L1’i de yüksek düzeyde taşıyordu. Tümörlerinde daha düşük KCTD1 olan hastalar genellikle daha uzun yaşadı; bu da bu proteinin hem hastalık şiddetiyle hem de tümörün immün kalkanının gücüyle bağlantılı olduğunu düşündürüyor.
Kanser hücreleri içindeki moleküler bağlantıları kurmak
KCTD1’in PD-L1’i nasıl artırdığını anlamak için ekip laboratuvarda büyütülen karaciğer kanseri hücre hatlarına döndü. KCTD1’i azalttıklarında PD-L1 protein düzeyleri düştü ve kalan PD-L1 daha hızlı parçalandı; bu durum KCTD1’in PD-L1’in genini sadece açmaktan ziyade onu stabilize etmeye yardımcı olduğunu gösteriyor. Biyokimyasal çekme (pull-down) deneyleri ve floresan mikroskopi kullanarak, KCTD1’in hücre çekirdeği içinde önemli bir kanser sürücüsü olan onkoprotein c-Myc’e fiziksel olarak bağlandığını gösterdiler. Bu etkileşim her iki proteindeki özgül temas bölgeleri aracılığıyla gerçekleşiyor ve daha stabil bir c-Myc’e yol açıyor; bu da sırasıyla PD-L1 üretimini artırıyor. Sadece c-Myc azaltıldığında, KCTD1 bol olsa bile PD-L1 düştü; bu da c-Myc’i KCTD1–c-Myc–PD-L1 zincirinde kritik bir ara bağlantı olarak konumlandırıyor.
Laboratuvarda T hücrelerini yeniden uyandırmak
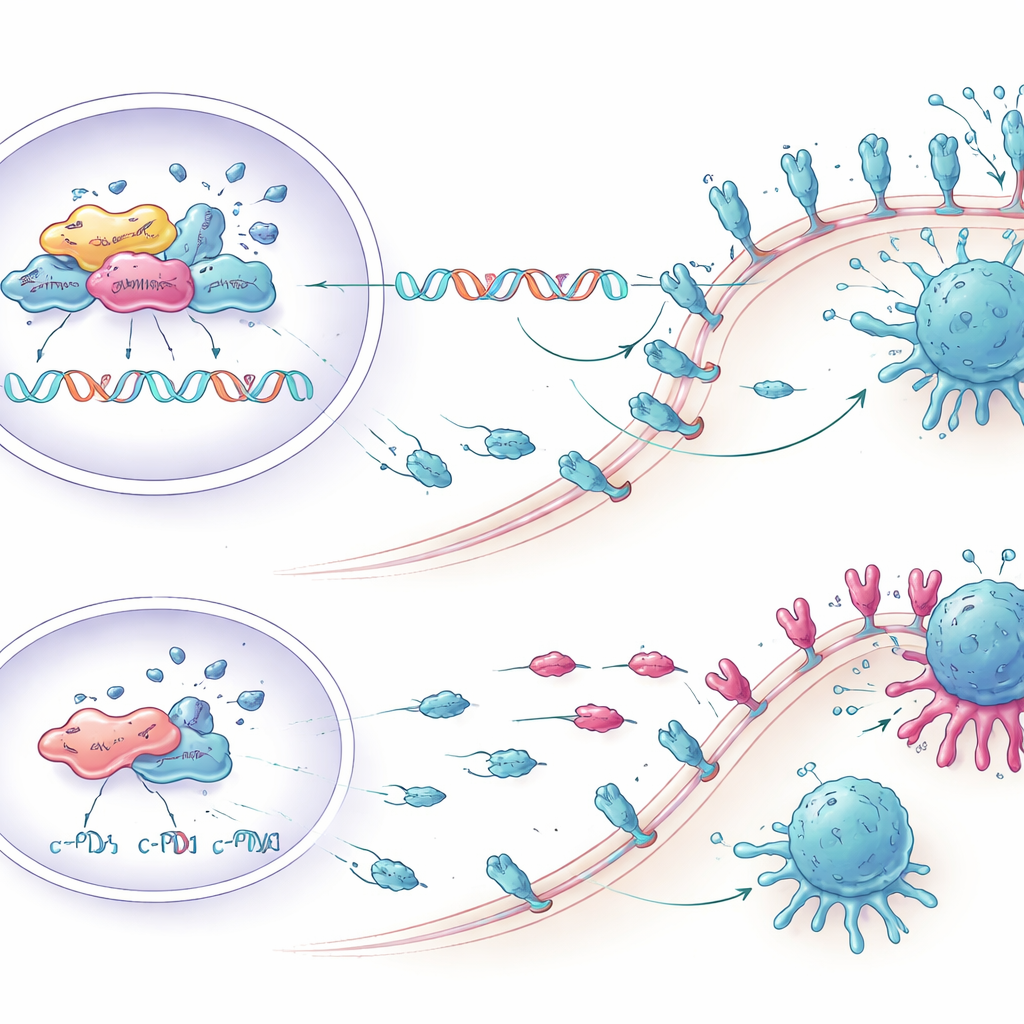
Araştırmacılar sonra KCTD1’in düşürülmesinin gerçekten immün saldırıyı güçlendirip güçlendirmeyeceğini sordular. İnsan karaciğer kanseri hücrelerini kan bağışçılarından alınan bağışıklık hücreleriyle ortak kültürlediler. Daha az KCTD1’e ve dolayısıyla daha az PD-L1’e sahip olacak şekilde tasarlanmış tümör hücreleri, CD8 T hücrelerinden—bağışıklık sisteminin kanser hücrelerini öldürmedeki başlıca efektörleri—daha güçlü yanıtlar tetikledi. Bu T hücrelerinin daha fazlası TNF-α ve interferon-gama gibi enflamatuar moleküller üretti, büyüme ve aktivasyon belirteçlerini daha yüksek gösterdi ve tükenme belirtileri daha azdı. Sonuç olarak, KCTD1 baskılandığında daha fazla tümör hücresi programlanmış hücre ölümü geçirdi; bu da moleküler değişikliklerin gerçek bağışıklık öldürme kazançlarına dönüştüğünü gösteriyor.
Mechanizmayı farelerde test etmek
Aynı örüntünün canlı organizmalarda da geçerli olup olmadığını görmek için ekip KCTD1 eksikliği olan fare karaciğer kanseri hücrelerini doğrudan farelerin karaciğerine implante etti. KCTD1’i azaltılmış tümörler daha az ve daha küçük nodül oluşturdu, hücre bölünmesi daha yavaştı ve daha fazla kanser hücresi hücre ölümü geçiriyordu. Bu tümörler ayrıca daha az c-Myc ve PD-L1 ifade etti. Farelerden CD8 T hücreleri çıkarıldığında bu faydanın büyük kısmı yok oldu; bu da tümör yavaşlamasının büyük ölçüde T hücresi aktivitesine bağlı olduğunu gösteriyor. Son olarak, araştırmacılar KCTD1 baskılanmasını anti–PD-1 antikoru ile birleştirdiklerinde—mevcut bir immün kontrol noktası ilacı—farelerde en küçük tümör yükü ve tümörlerine en yoğun CD4 ile CD8 T hücresi infiltrasyonunu gözlemlediler.
Hastalar için bunun anlamı ne olabilir
Bir arada ele alındığında, çalışma KCTD1’i c-Myc’i stabilize eden, karaciğer kanseri hücrelerinde PD-L1’i yükselten ve CD8 T hücresi saldırısını köreltan merkezi bir düzenleyici olarak ortaya koyuyor. Bu yolun bozulması tümörleri hem bağışıklık sistemi için daha hassas hale getiriyor hem de farelerde PD-1’i engelleyen ilaçlara daha yanıtlı kılıyor. Hastalar açısından bu, KCTD1’e veya KCTD1 ile c-Myc arasındaki temas yüzeyine yönelik ilaçların ileride mevcut immünoterapilerle eşleştirilerek daha fazla karaciğer kanseri hastasının hastalığı üzerinde kalıcı bağışıklık kontrolünden yararlanmasına yardımcı olabileceğini öne sürüyor.
Atıf: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Anahtar kelimeler: hepatosellüler karsinom, tümör immünoterapisi, PD-1 PD-L1 yolu, c-Myc sinyalleşmesi, T hücresi antitümör bağışıklığı