Clear Sky Science · tr
Multi-omik, insan nöral kök hücreleriyle indüklenen oligodendrosit progenitör hücrelerin heterojenliğini ve fonksiyonel popülasyonlarını ortaya koyuyor
Beyin yalıtımını korumanın önemi
Beynimizin bağlantıları, sinir liflerini elektrik kablolarındaki yalıtım gibi saran miyelin adlı yağlı bir kaplama sayesinde işler. Miyelin hasar gördüğünde —örneğin multipl skleroz ve diğer bozukluklarda— iletim yavaşlar veya aksar; bunun sonucu olarak hareket, görme ve düşünmeyle ilgili sorunlar ortaya çıkar. Bu çalışma, miyelini yeniden inşa edebilen özel bir insan hücresi grubunu araştırıyor ve pratik bir soruyu yanıtlamaya çalışıyor: Gelecekteki hücre terapileri için hangi hücreler bu hayati yalıtımı onarmada en uygun?
Başlangıç beyin hücrelerinden miyelin yapıcılara
Araştırmacılar, fetal beyin dokusundan elde edilen ve sinir sistemi hücrelerine dönüşme yönünde belirlenmiş çok yönlü başlangıç hücreleri olan insan nöral kök hücreleriyle başladılar. Bu kök hücreleri laboratuvarda oligodendrosit progenitör hücrelere (hOPC’ler) dönüştürdüler; bunlar miyelin üreten hücrelerin doğrudan öncülleridir. Mikroskop altında hücreler basit yuvarlak biçimlerden çok dallanmış daha karmaşık görünümlere geçti ve olgun miyelin üreten hücrelere giden yolda yer alan karakteristik proteinleri aktif hale getirdiler. Bu, insan miyelin inşa edici öncüllerinin güvenilir ve görece güvenli bir kaynağını sağlayarak ayrıntılı analizlere olanak verdi.
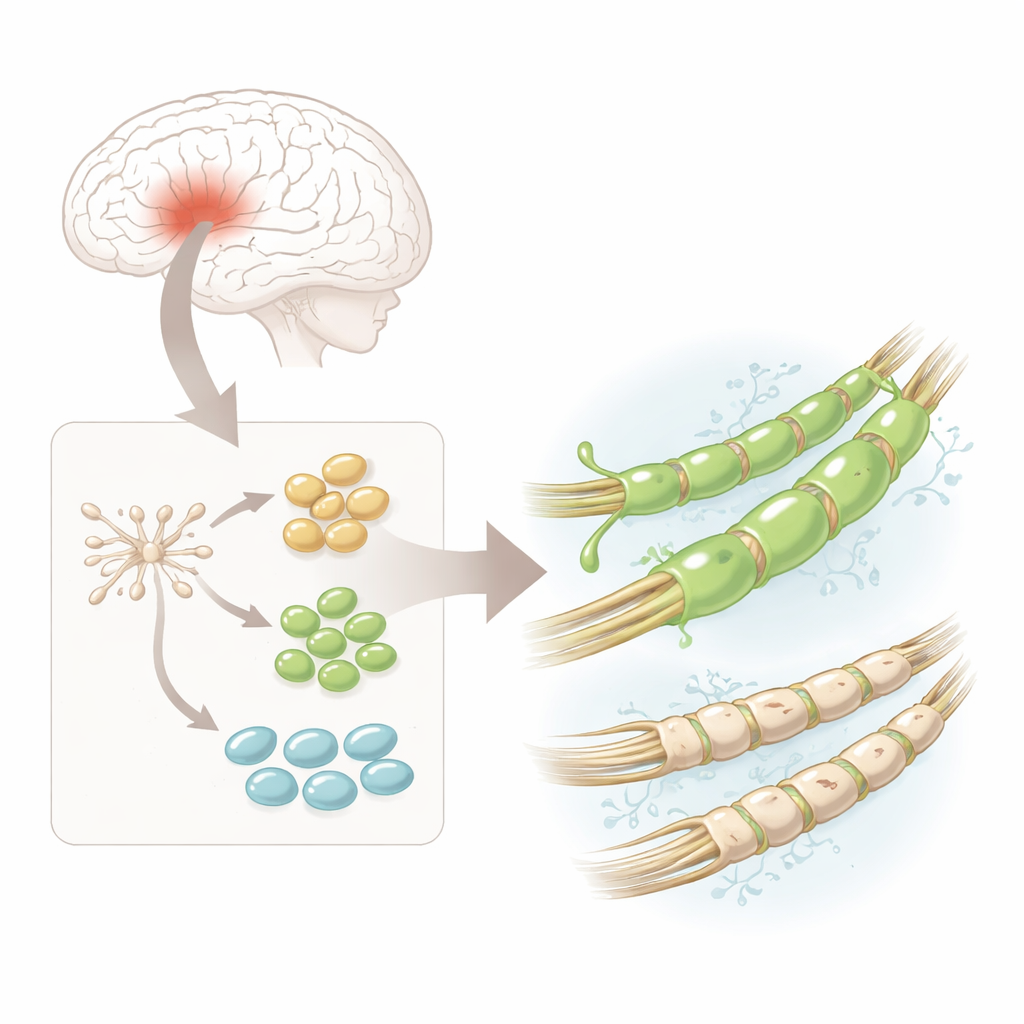
Tek hücre tipi, birçok gizli çeşit
Binlerce bireysel hücrede hangi genlerin aktif olduğunu okuyan tek hücre RNA dizilemesi kullanarak ekip, hOPC’lerin birbirinin aynı olmadığını keşfetti. Bunun yerine, hücreler üç ana aşamada gruplaştı: erken “ön-progenitörler”, daha kararlı progenitörler ve tam oligodendrosit kimliğine yaklaşan hücreler. Tüm bu aşamalar boyunca öne çıkan bir gen vardı: hücre yüzeyi reseptörünü kodlayan PDGFRA. RNA-Scope adı verilen yüksek hassasiyetli görüntüleme yöntemi, PDGFRA’nın mesajının ve proteininin diğer ana belirteçlere göre her aşamada daha bol olduğunu doğruladı; bu da bu reseptörün özellikle yetenekli miyelin inşa eden hücreleri tanımlayabileceğini düşündürdü.
En güçlü onarım hücrelerini ayırmak
Bu fikri test etmek için bilim insanları hOPC’leri yüzeylerinde PDGFR-α reseptörü bulunup bulunmamasına göre iki gruba ayırdı. Ardından PDGFR-α–pozitif hücreleri, PDGFR-α–negatif hücreleri ve sıralanmamış hücreleri bir dizi fonksiyonel testte karşılaştırdılar. Normal miyelin oluşturamayan “shiverer” farelere nakledildiğinde, PDGFR-α–pozitif hücreler sinir lifleri etrafında diğer gruplara göre daha yoğun ve daha kompakt miyelin üretti. Bu hücreler laboratuvar testlerinde ayrıca daha uzaklara göç etti ve daha hızlı çoğaldı. Başka bir deyişle, PDGFR-α–pozitif popülasyon ihtiyaç duyulan yere hareket etme, sayısal olarak genişleme ve yalıtımı yeniden inşa etme konusunda en dinamik olanıydı.
Büyüme ve onarımı yönlendiren iç sinyaller
Daha derine indiklerinde ekip, PDGFR-α–pozitif ve –negatif hücreler arasındaki gen etkinliğini karşılaştırdı. Pozitif hücrelerin, glial hücre büyümesi ve miyelin oluşumunda rol oynayan gen ağlarını ve hücre içindeki birkaç önemli sinyal yolunu aktive ettiklerini buldular. Özellikle iki yol öne çıktı: uzun süredir hücre büyümesi ve miyelin üretimiyle ilişkilendirilen PI3K–AKT–mTOR yolu ve genç beyin hücrelerinin kader seçimlerini etkileyen TGF-β sinyal yolu. Veriler, PDGFR-α aktivasyonunun PI3K–AKT–mTOR’a bağlandığını, bunun da TGF-β ile ilişkili sinyalleri güçlendirdiğini ve birlikte hücreleri etkili miyelin yapıcılar olmaya yönlendirdiğini öne sürdü.
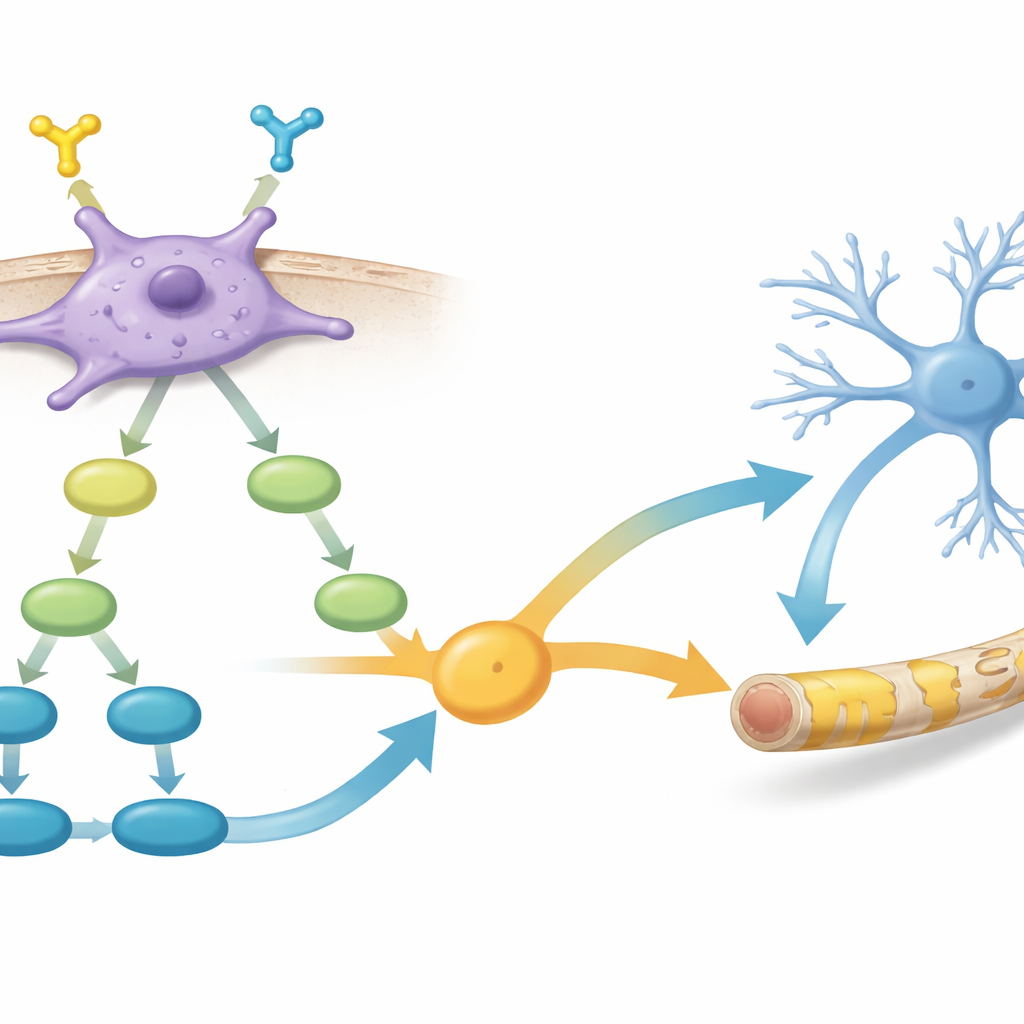
Kimyasal bir yardımcı ile miyelin onarımını güçlendirmek
Araştırmacılar ardından bu umut verici hücreleri daha da güçlendirip güçlendiremeyeceklerini sordular. PDGFR-α–pozitif hOPC’leri TGF-β yolunu aktive eden küçük bir molekül ile tedavi ettiler ve hem gen etkinliğini hem de davranışı incelediler. Tedavi sonrası bu hücreler birden fazla miyelinle ilişkili gen düzeyinde artış gösterdi ve shiverer farelere nakledildiklerinde, tedavi edilmemiş PDGFR-α–pozitif hücrelere kıyasla daha kalın ve daha bütünsel miyelin kılıfları üretti. Bu, iyi seçilmiş progenitor hücrelerde iç sinyallemeyi dikkatli şekilde ayarlamanın, canlı miyelin onarım araçları olarak performanslarını daha da iyileştirebileceği fikrini destekliyor.
Gelecekteki tedaviler için anlamı
Uzman olmayanlar için temel mesaj şudur: Tüm miyelin inşa edici öncü hücreler eşit değildir. Güçlü gen-okuma ve görüntüleme araçlarını birleştirerek bu çalışma göze çarpan bir alt grubu tanımlıyor — PDGFR-α–pozitif hOPC’ler — bunlar daha iyi göç ediyor, daha fazla bölünüyor ve akranlarından daha etkili şekilde miyelin yeniden inşa ediyor. Ayrıca kimyasal olarak yönlendirilebilecek iç sinyal yollarını vurguluyor; bunlar bu hücreleri daha da güçlü kılmak için hedef alınabilir. Birlikte, bu bulgular miyelin kaybının olduğu hastalıklarda beynin yalıtımını eski haline getirmek için daha güvenli ve daha etkili hücre tedavileri tasarlamak adına bir yol haritası sunuyor.
Atıf: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Anahtar kelimeler: miyelin onarımı, oligodendrosit progenitör hücreler, nöral kök hücreler, hücre terapisi, tek hücre RNA dizileme