Clear Sky Science · tr
Mitokondriyal biyoenerjetik–SASP etkileşimi, tedavi kaynaklı senesansda senolitik etkinliği belirler
“Zombi” kanser hücrelerini yok etmek neden bu kadar zor?
Birçok modern kanser ilacı tüm tümör hücrelerini doğrudan öldürmez. Bunun yerine bazı hücreler bölünmeyi bırakıp canlı kalan, adeta “zombi” hücrelere benzeyen bir ara durum olan senesans haline girer. Tedaviyle oluşan bu senesans hücreleri başlangıçta yararlı olabilir, ancak uzun süre kalırlarsa nüks, direnç ve yan etkilere yol açabilirler. Bu yüzden bilim insanları, senesanslı hücreleri seçici olarak öldürmeyi amaçlayan senolitik ilaçları test ediyor. Bu makale, aldatıcı derecede basit bir soruyu soruyor: bazı senesanslı kanser hücreleri senolitiklere maruz kaldığında neden ölürken, diğerleri inatla hayatta kalıyor?
Geçmişini hatırlayan enerji santralleri
Çalışmanın merkezinde hücre içindeki küçük enerji santralleri olan mitokondriler var. Yazarlar, mitokondrilerin şekerler, yağlar ve aminoasitler gibi farklı yakıtları yakma biçiminin, BCL‑xL adlı bir hayatta kalma proteininin hedeflendiği senolitik ilaçlara karşı senesanslı kanser hücrelerinin duyarlılığını etkileyip etkilemediğini incelediler. Yüksek verimli bir test (MitoPlate S‑1) kullanarak, farklı tedavilerle (DNA hasarı yapan ilaçlar, mitotik bloke ediciler, oksidatif stres veya hücre döngüsü inhibitörleri) senesans tetiklenmeden önce ve sonra birkaç kanser hücre hattında mitokondriyal aktivitenin fonksiyonel “parmak izini” çıkardılar. Tedaviyle oluşan senesansın tek, birleşik bir mitokondriyal durum üretmediğini buldular. Bunun yerine her ilaç, mitokondrilerin çeşitli enerji kaynaklarına ne kadar yaygın ve yoğun erişebildiğini değiştiren belirgin bir “biyoenerjetik iz” bıraktı. Kritik olarak, bu esneklik önceden var olan bir temelin üzerine örüldü: ebeveyn kanser hücrelerinin özgün mitokondriyal konfigürasyonu, sonraki herhangi bir senolitik yanıtın ne kadar güçlü olabileceğine dair üst sınırı —“tavanı”— belirliyordu.
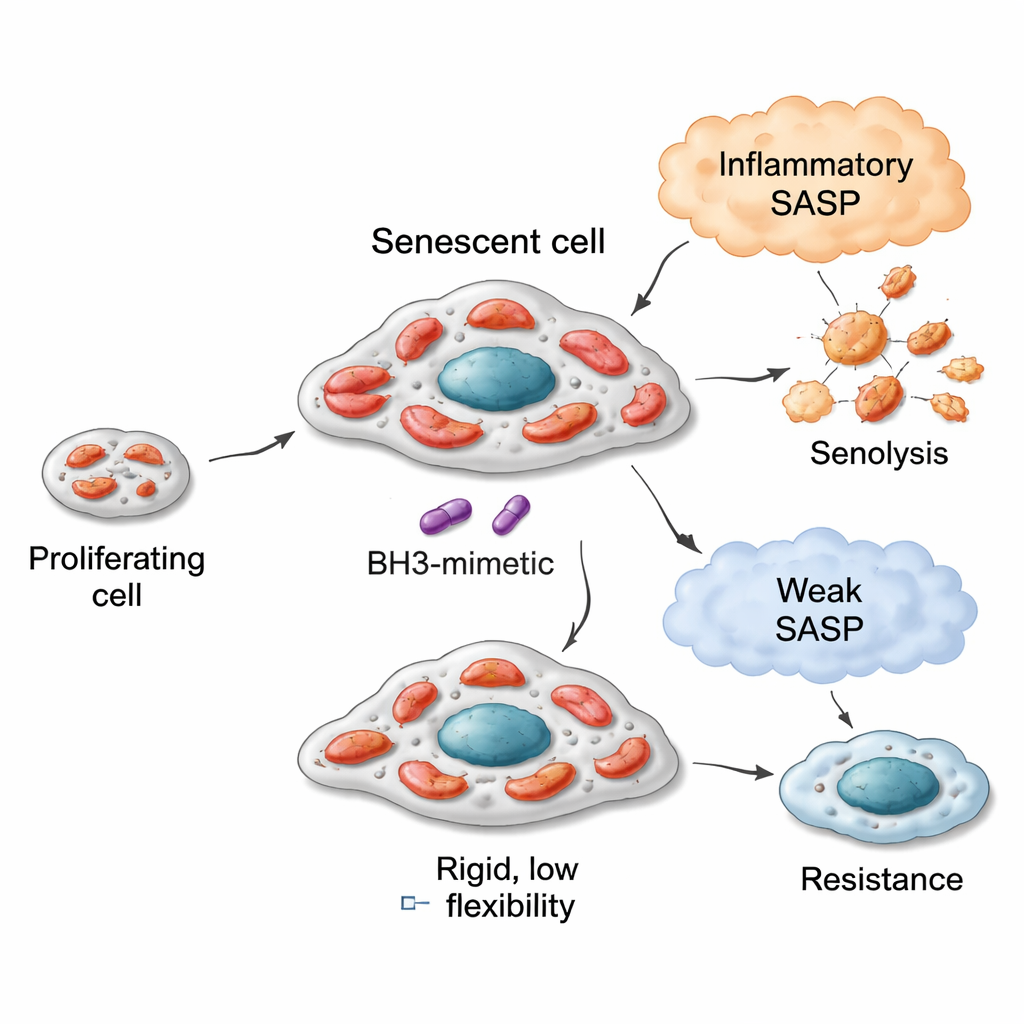
Esnek motorlar, farklı yakıtlar ve senolitik hassasiyet
Akciğer, meme ve kolon kanseri modellerinde, daha esnek mitokondrilere sahip —daha geniş bir yakıt yelpazesini oksitleyebilen— senesanslı hücreler, navitoklaks (ABT‑263) ve A1331852 gibi BCL‑xL’i hedef alan senolitiklere karşı daha hassas olma eğilimindeydi. Örneğin, bleomisin ile senesansa sürülen akciğer kanseri hücreleri, özellikle yağ asidi ayrışımı ve belirli aminoasit yollarıyla bağlantılı birçok substratı canlı biçimde kullanan mitokondriler geliştirdi. Bu hücreler senolitiklere karşı oldukça duyarlıydı. Buna karşılık, bir CDK4/6 inhibitörü (palbociklib) ile senesansa itilen hücreler daha dar bir metabolik repertuvara sahipti ve aynı senolitik ilaçlara zayıf yanıt verdi. Yine de bu ilişkinin sınırları vardı: meme kanseri hücreleri de senesans sonrası metabolik esneklik kazanabilirdi, ancak başlangıçtaki mitokondrilerinin apoptoza daha az “hazır” olması nedeniyle maksimum senolitik yanıtları mütevazi kaldı. Apoptotik mekanizması bozuk kolon kanseri hücreleri, metabolizmaları nasıl değişirse değişsin dirençli kaldı. Tek bir ölçüm —hücrelerin temel düzeyde sukkinatı ne kadar iyi okside ettiğini gösteren değer— bu miras alınmış mitokondriyal kapasitenin basit bir göstergesi olarak hizmet etti.
Metabolizma ile iltihap konuştuğunda
Senesanslı hücreler, çevreleyen dokuları etkileyebilen salgılanan inflamatuvar ve büyüme faktörleri karışımı olan SASP ile kötü şöhretlidir. Ekip, mitokondriyal metabolizmanın bu salgılama davranışıyla nasıl bağlandığını, ana inflamatuvar düzenleyici NF‑κB tarafından aktif hale getirilen bir mikroRNA olan miR‑146a için raporör taşıyan hücreler kullanarak araştırdı. Genel SASP profillerinin büyük ölçüde hücre tipine bağlı olduğunu, yalnızca belirli senesans durumlarının bu NF‑κB/miR‑146a eksenini aktive ettiğini buldular. Bu durumlar, BCL‑xL senolitiklerine iyi yanıt veren aynı durumlarla örtüşüyordu. Önemli olarak, bu “inflamatuvar SASP‑pozitif” senesanslı hücreler aynı zamanda yağ asidi oksidasyonunun artmış kullanımını ve uzun zincirli yağları mitokondriye taşıyan genlerin transkripsiyonel yükselmesini gösterdi. Etomoksir ile yağ asidinin girişinin engellenmesi, senesansı tamamen tersine çevirmeden miR‑146a aktivasyonunu azalttı; bu, mitokondriyal yakıt seçiminin inflamatuvar, senolitik‑izin veren bir SASP’i yetkilendirmeye yardımcı olduğunu düşündürüyordu.
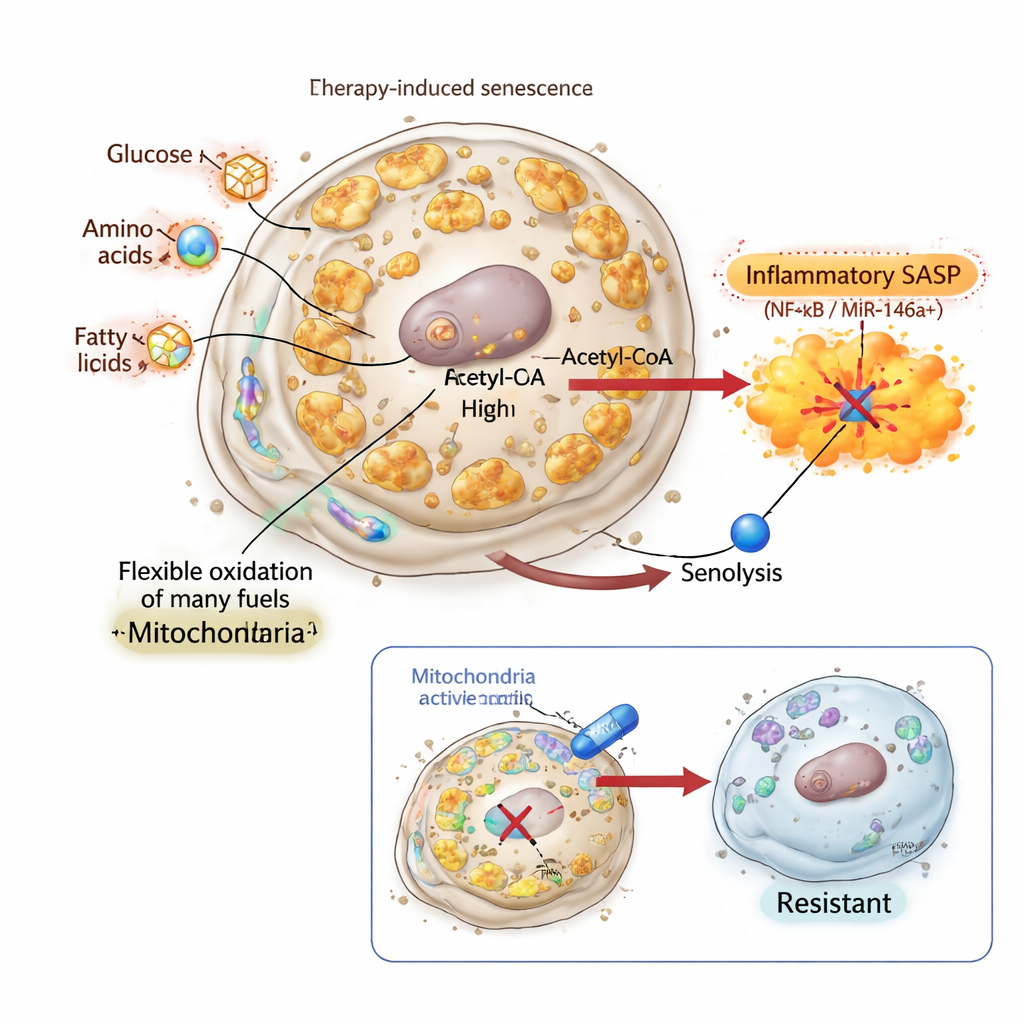
Sinyali susturmak ve öldürülemez senesanslı hücreler yaratmak
Araştırmacılar, inflamatuvar SASP’in gerçekten senolitik öldürme için gerekli olup olmadığını test etmek amacıyla, kromatin proteinleri HMGB1 ve HMGB2’ye bağlanan ve SASP genlerinin aktivasyon rolünü engelleyen bir bileşik olan inflazromen’e (inflachromene) döndüler. Akciğer ve meme kanseri hücrelerinde inflachromene, ders kitabı senesans fenotipi indükledi: hücreler büyüdü, bölünmeyi bıraktı ve senesans belirteçleri birikti. Mitokondriyal kütleleri ve biyoenerjetik aktiviteleri önemli ölçüde arttı ve yakıt kullanımları belirgin biçimde yeniden düzenlendi. Ancak SASP’leri zayıfladı ve miR‑146a raporörü büyük ölçüde sessiz kaldı. Çarpıcı şekilde, bu SASP‑yok senesanslı hücreler, biyoenerjetik olarak aktif, yeniden programlanmış mitokondrilere ve klasik anti‑apoptotik gen BCL2’nin azalmış ifadesine rağmen, BCL‑xL’i hedef alan senolitiklere tamamen dirençliydi. Bu, mitokondriyal değişikliklerin tek başına yeterli olmadığını; mitokondri kaynaklı bir inflamatuvar çıktı olmadan senolitik “ikinci darbe”nin başarısız olduğunu gösterdi.
Gelecekteki kanser tedavileri için anlamı
Bilim dışı bir okuyucu için çalışmanın sonucu şudur: tedavi kaynaklı “zombi” kanser hücrelerini öldürmek katmanlı bir devre tarafından yönetiliyor. Birincisi, bir tümör hücresinin mitokondrilerinin özgün sağlığı ve bağlantılanması, senolitik ilaçların ulaşabileceği sınırı belirler. İkincisi, senesansı tetikleyen özel tedavi, mitokondriyal metabolizmayı daha fazla veya daha az esnekliğe iterek hücreleri apoptoz kenarına daha yakın veya daha uzak hale getirebilir. Üçüncüsü —ve en belirleyici olanı— metabolik yeniden programlama, inflamatuvar bir SASP programını etkinleştirmeyi başarıyla başarmadıkça senolitikler iyi iş görmez. Bu inflamatuvar çapraz iletişim yoksa, senesanslı hücreler ilaçlara dirençli, çıkmaz bir duruma dönüşebilir. Pratikte bu, gelecekteki terapilerin tümörlerde hem mitokondriyal esnekliği hem de SASP inflamasyonunu fonksiyonel olarak test ederek optimize edilebileceğini; ardından senesans-indükleyen ilaçlar ile senolitiklerin kombinasyonlarının, “zombi” hücrelerin yalnızca donup kalmamasını, aynı zamanda uzaklaştırılmaya hazır hale getirilmesini sağlayacak biçimde seçilebileceğini öne sürer.
Atıf: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Anahtar kelimeler: hücresel senesens, mitokondriler, senolitikler, kanser metabolizması, inflamatuvar SASP