Clear Sky Science · tr
PDHA1, anoikis’e dirençli prostat kanserinde AIFM2’yi yukarı düzenleyerek ferroptozise karşı direnci artırıyor
Neden bazı prostat kanseri hücreleri ölmekten kaçınıyor
Tümörden kopup kan dolaşımına giren kanser hücrelerinin çoğunun yeni bir organa ulaşmadan önce ölmesi beklenir. Buna rağmen tehlikeli bir azınlık hayatta kalır, yolculuk yapar ve genellikle ölümcül olan metastazları tohumlar. Bu çalışma temel bir soruyu soruyor: belirli prostat kanseri hücrelerinin, normalde dokularıyla temasını kaybettiklerinde ortaya çıkan bir hücre ölümü biçimine karşı koymasını ne sağlıyor? Bu hücrelerin içinde gizli bir hayatta kalma devresini ortaya çıkararak araştırma, metastazı kaynağında engellemek için yeni yollar önermektedir.
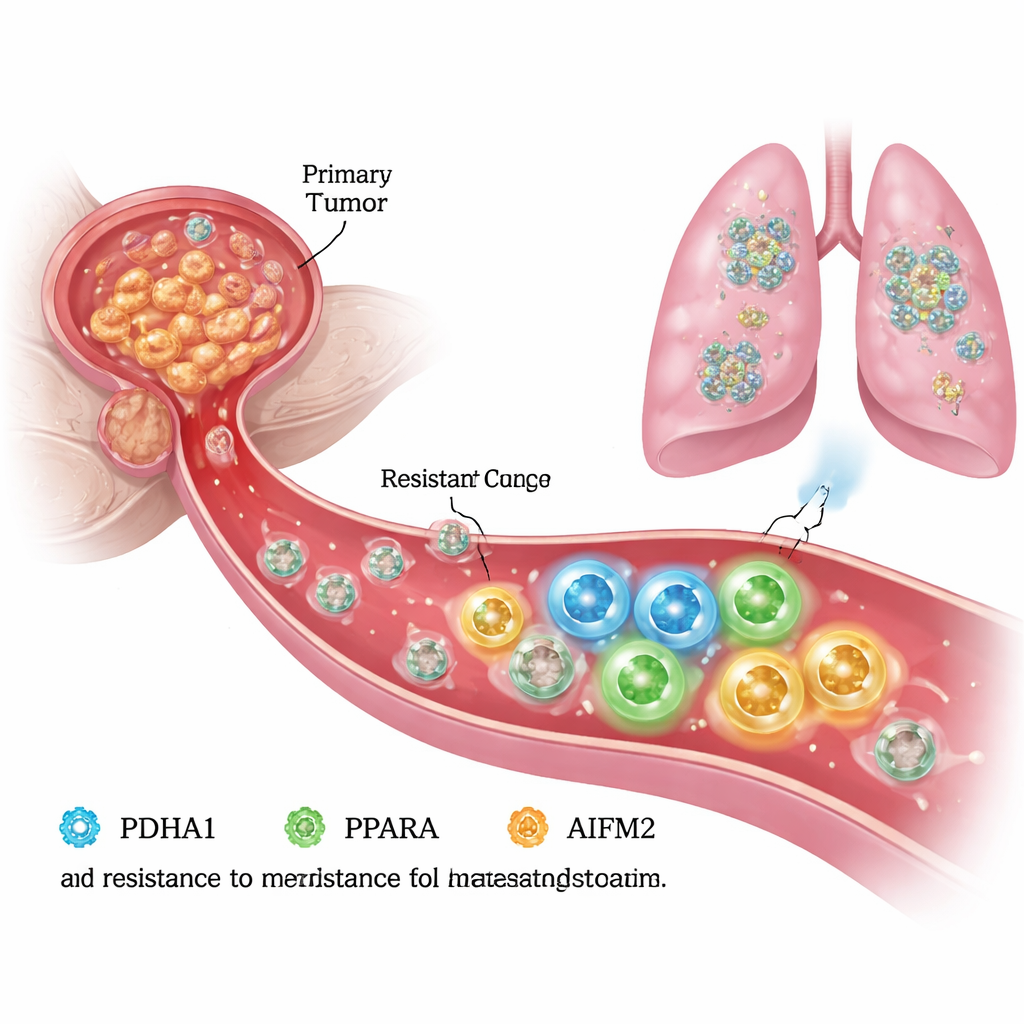
Kan dolaşımında ölümden kaçış
Yayılmak için prostat kanseri hücreleri, çevreleyici doku desteği olan hücre dışı matriks olmadan yaşamaya dayanmak zorundadır. Bu “ayrılmış” koşullar altında sağlıklı hücreler anoikis adı verilen programlı bir ölümü yaşar ve pek çok kanser hücresi de ilişkili demir kaynaklı bir ölüm süreci olan ferroptozise duyarlıdır. Yazarlar laboratuvarda anoikis’e dirençli prostat kanseri hücreleri oluşturdular ve bunları orijinal “ebeveyn” hücreleriyle karşılaştırdılar. Rezistan hücrelerin sadece daha agresif göç ve invazyon göstermediğini, aynı zamanda ayrılma koşullarında daha iyi hayatta kaldıklarını buldular; bu da ferroptozisten kaçınmak ve büyümeye devam etmek için iç mekanizmalarını yeniden yapılandırdıklarını düşündürüyor.
İkinci bir işleve sahip metabolik bir anahtar
Daha derine indiklerinde ekip, şeker kaynaklı pirüvattan mitokondride asetil-CoA üretilmesine yardımcı olmasıyla bilinen PDHA1 adlı bir metabolik enzim üzerinde yoğunlaştı. Anoikis’e dirençli hücrelerde PDHA1 seviyeleri ve aktivitesi belirgin şekilde daha yüksekti ve hasta örnekleri, prostat kanseri lenf düğümlerine veya uzak bölgelere yayılmış erkeklerin primer tümörlerinde daha fazla PDHA1 gösterdi. Araştırmacılar PDHA1’i azalttığında, dirençli hücreler göç, invazyon ve hayatta kalma yeteneklerinin büyük bir kısmını kaybetti. Sürpriz bir şekilde, bu hücrelerdeki PDHA1’in önemli bir bölümü artık yalnızca mitokondride değildi; nükleusa taşınmıştı; burada DNA histonlarla paketlenir ve bu histonlar genleri açıp kapatmaya yarayan kimyasal değişikliklere uğrayabilir.
Ferroptozisi engellemek için gen aktivitesini yeniden yazmak
Nükleusta PDHA1, histon asetilasyonu için kritik bir yapı taşı olan asetil-CoA’nın yerel üretimini destekliyor gibi görünüyordu. Yazarlar, nükleer PDHA1’in bir gen olan PPARA’nın kontrol bölgesinde H3K9 asetilasyonu adlı spesifik bir işareti artırdığını gösterdiler. Bu değişiklik kromatin “makaralarını” gevşetmek gibi davranarak PPARA’yı açmayı kolaylaştırdı. PPARA da kendi başına, bir anahtar anahtar rolü görerek başka bir proteinin, AIFM2’nin üretimini artırdı; PPARA, AIFM2’nin promotörüne bağlanıp transkripsiyonunu yükseltti. PDHA1 doğrudan AIFM2 genini ayarlamak yerine böylece PPARA yoluyla çalışmış, metabolik değişimden gen düzenlemesine uzanan çok adımlı bir yol oluşturmuştu.
Demir kaynaklı hasara karşı bir kalkan inşa etmek
AIFM2, ferroptozise karşı içsel bir fren olarak bilinir: hücre zarlarındaki yağları yıkıcı oksidasyondan korumaya yardımcı olur. Rezistan prostat kanseri hücrelerinde PDHA1 artışı AIFM2 düzeylerini yükseltirken, PDHA1 bastırılması bunları düşürdü. Fonksiyonel testler PDHA1’in azaltılmasının ferroptozis belirtilerini yoğunlaştırdığını gösterdi—daha fazla reaktif oksijen türü, daha fazla lipid hasarı, daha düşük mitokondri membran potansiyeli ve tipik mitokondri büzüşmesi—özellikle hücreler ferroptozis indükleyici ilaç erastine maruz kaldığında. AIFM2’nin aşırı eksprese edilmesi bu etkileri tersine çevirdi, kültürde hücre hayatta kalmasını kurtardı ve PDHA1 baskılanmış olsa bile farelerde akciğer metastazını geri getirdi. Bu, AIFM2’nin PDHA1 kaynaklı ferroptozis direncinin kritik bir aşağı akış etkileyicisi olduğunu doğruladı.
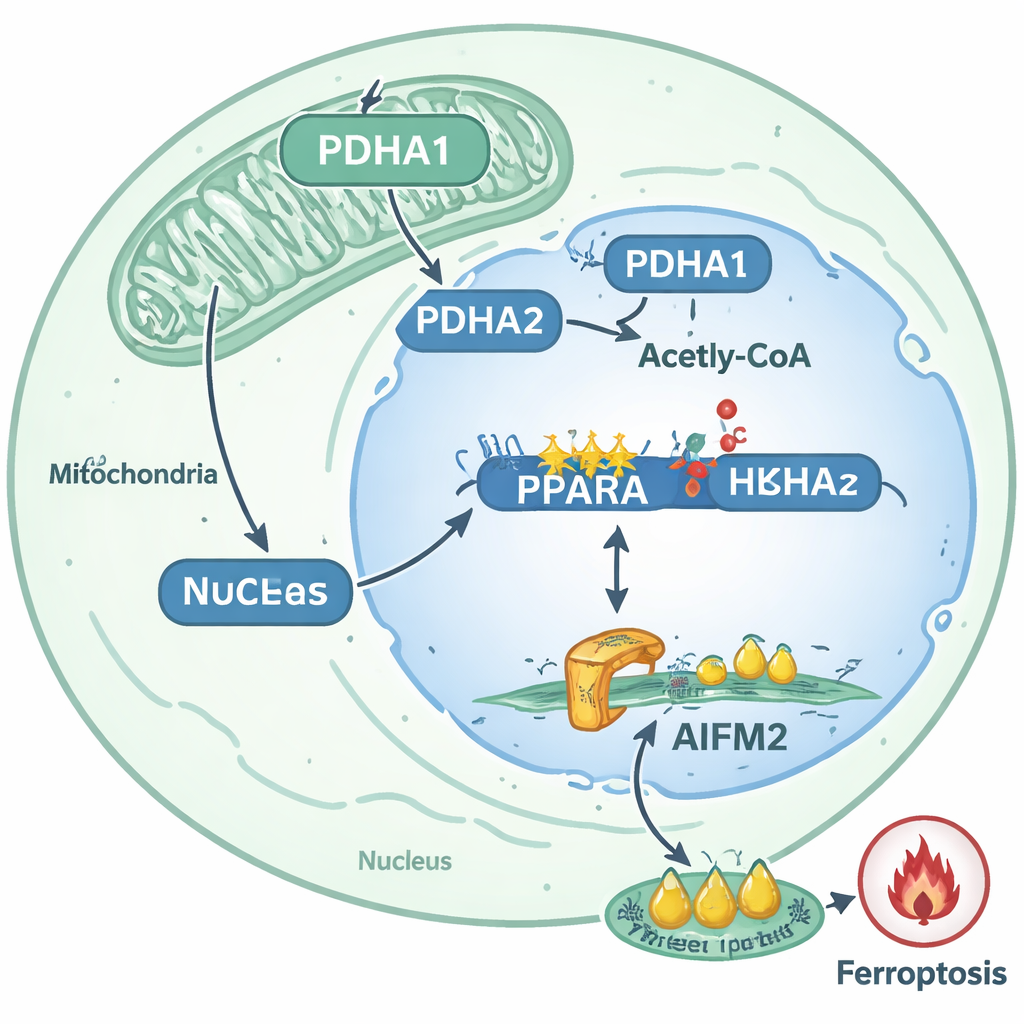
Moleküler devreden tedavi fikirlerine
Bu olayları haritalandırarak çalışma, ayrılmış prostat kanseri hücrelerinin neden öldürülmesinin daha zor hale geldiğine dair net bir yol sunuyor: PDHA1 nükleusa taşınıyor, PPARA geninde histon asetilasyonunu artırıyor, PPARA aktivitesini yükseltiyor ve böylece AIFM2 düzeylerini artırarak ferroptozisi engelliyor. Bu yol hasta tümörlerinde ve hayvan modellerinde metastatik davranışla güçlü şekilde ilişkilendiriliyor. Uzman olmayanlar için çıkarım şu: belirli kanser hücreleri, klasik bir metabolik enzimi epigenetik bir araca dönüştürerek gen aktivitesini yeniden kablolar ve güçlü bir hücre ölümü biçimine karşı biyokimyasal bir kalkan inşa eder. Yazarlar, PDHA1, PPARA veya AIFM2’yi hedefleyen ilaçların—ya da kasıtlı olarak ferroptozisi tetikleyen tedavilerin—bir gün kombinasyon halinde kullanılarak metastatik prostat kanseri hücrelerinin bu hayatta kalma avantajından mahrum bırakılabileceğini ve organlar arası en savunmasız yolculuklarında onları çok daha hassas hale getirebileceğini öne sürüyorlar.
Atıf: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Anahtar kelimeler: prostat kanseri metastazı, ferroptozis, anoikis direnci, PDHA1, AIFM2