Clear Sky Science · tr
Glioma zayıflıklarını açığa çıkarmak: yenilikçi tedaviler için düzenlenmiş hücre ölümü yollarını hedeflemek
Beyin Tümörü Hücre Ölümünün Neden Önemi Var
Gliomlar, yetişkinlerde en yaygın ve ölümcül beyin tümörlerinden bazılarıdır. Cerrahi, radyasyon ve kemoterapiye rağmen sıklıkla tekrarlama eğilimindedirler ve kontrol altına alınmaları zordur. Bu derleme makalesi yeni bir saldırı açısını inceliyor: hücrelerin programa bağlanmış farklı ölüm yollarını kullanmak. Bu “kendi kendini yok etme” yollarını anlamak ve yönlendirmek suretiyle araştırmacılar, glioma hücrelerindeki zayıf noktaları açığa çıkarmayı ve gelecekteki tedavileri daha etkili ve kişiselleştirilmiş hale getirmeyi umuyorlar.
Gliomlar Standart Tedavileri Nasıl Alt Eder
Gliomlar, beynin destek hücrelerinden kaynaklanır ve yavaş büyüyenden glioblastoma gibi son derece agresif formlara kadar değişir. Kötü sonuçlarının arkasında birbiriyle bağlantılı birkaç sorun vardır: genetik mutasyonlar, epigenetik değişiklikler, öldürülmesi zor kök hücreye benzer hücreler, anormal kan arzusu ve yüksek derecede baskılayıcı bir bağışıklık ortamı. Buna ek olarak kan–beyin bariyeri ilaçların tümöre ulaşmasını sınırlar. Bu faktörler birlikte tümör hücrelerinin cerrahi ve standart ilaçlardan kurtulmasına, strese uyum sağlamasına ve sonunda yeniden büyümesine olanak tanır. 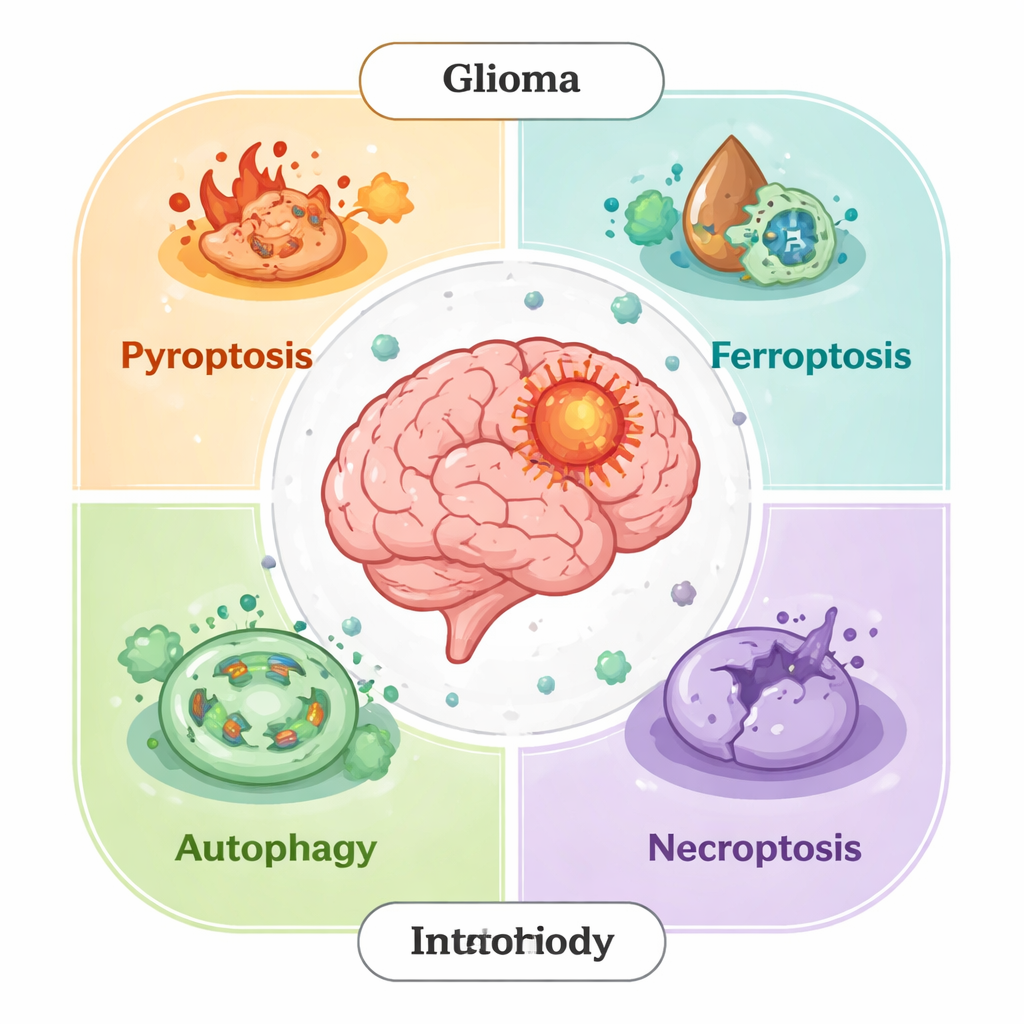
Hücrelerin Kendi Kendini Yok Etmesinin Birçok Yüzü
On yıllar boyunca bilim insanları, apoptoz adı verilen ana programlanmış hücre ölümü biçimine odaklandı. Şimdi bunun hikâyenin yalnızca bir parçası olduğunu biliyoruz. Glioma hücreleri ayrıca başka düzenlenmiş yollardan da ölebilir: piyroptoz (alevli, iltihaplı bir patlama), ferroptoz (demir kaynaklı membran hasarı), nekroptoz (kontrollü hücre yırtılması) ve otofaji-bağımlı ölüm (fazla giden oto-yeme). Sağlıklı dokularda bu süreçler hasarlı hücreleri ortadan kaldırır ve kanseri önler. Ancak tümörlerde glioma hücreleri bu yolları sıklıkla yeniden düzenler—ölüm sinyallerini engelleyerek, antioksidan savunmaları artırarak veya otofajiyi bir hayatta kalma aracına çevirerek—tedaviye direnmek ve büyümeyi destekleyen bir mikroçevre oluşturmak için.
Ölüm Yollarını Tedaviye Dönüştürmek
Araştırmacılar bu ölüm yollarını bir sorun olarak görmek yerine silahlandırmayı öğreniyor. Piyroptozu indükleyen stratejiler, glioma hücrelerinin şişip parçalanmasını ve bağışıklık sistemini uyaran tehlike sinyalleri salmasını sağlamak için akıllı nanoparçacıklar, ışıkla ısıtma, mühendislik virüsleri veya ilaç yüklü hidrojel kullanan yaklaşımlar içerir. Ferroptoz tabanlı yaklaşımlar ise tümör hücrelerini GPX4 gibi koruyucu enzimleri engelleyerek, glutatyon üretimini bozarak veya tümör hücrelerinin yağ işleme yollarını değiştirerek demir destekli çöküşe iter. Bu taktiklerin birçoğu, ilaçların kan–beyin bariyerini geçmesine yardımcı olmak ve sağlıklı beyin dokusunu korurken tümör içinde yoğunlaşmasını sağlamak için graphdiyne ve diğer nanoparçacıklar dahil gelişmiş taşıyıcılarla verilmektedir. 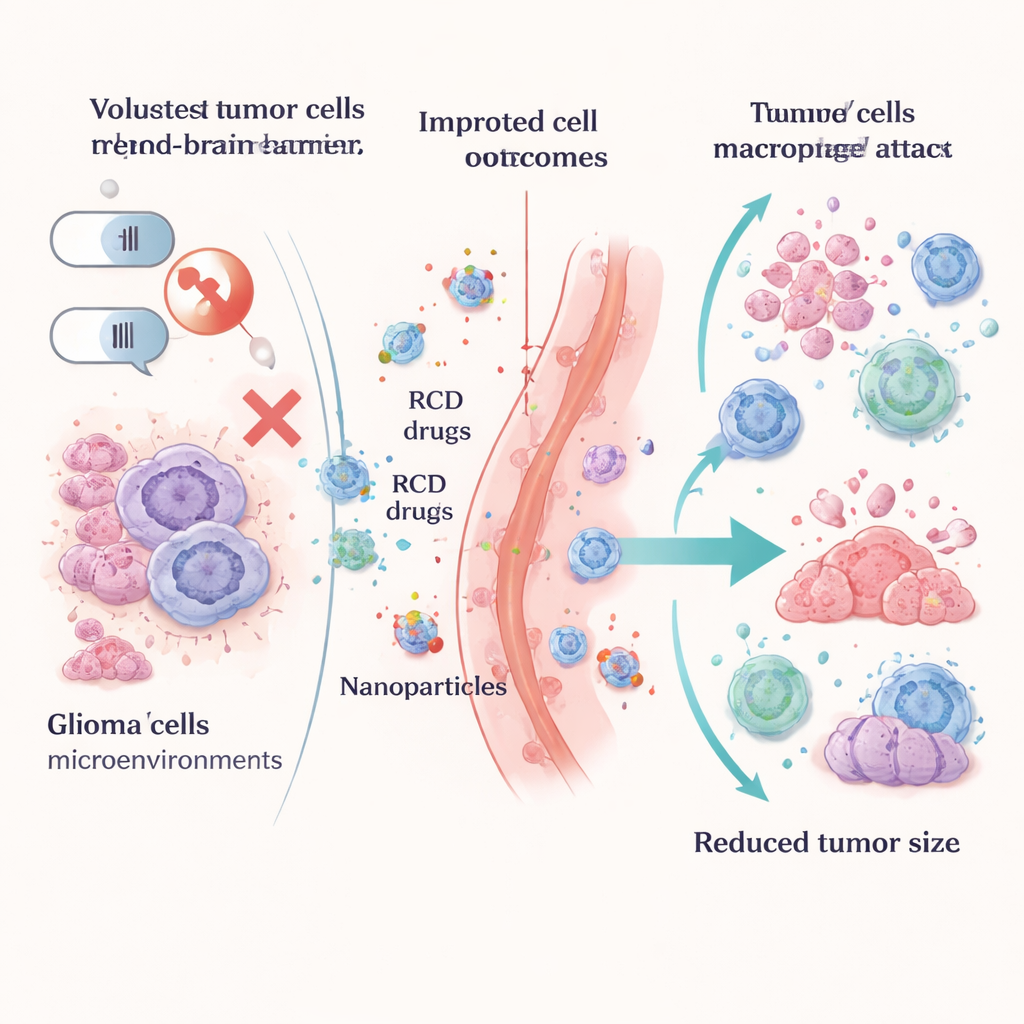
Tümörün Bağışıklık Ortamını Yeniden Başlatmak
Nekroptoz odaklı tedaviler, artık standart ölüm sinyallerine yanıt vermeyen hücrelerdeki direnci aşmayı hedefler. Şikonin, emodin ve celastrol türevleri gibi doğal ürünler glioma hücrelerini nekroptoza itebilir; bu sadece hücreleri öldürmekle kalmaz, aynı zamanda bağışıklık hücrelerini tümöre çeken moleküller salar. Aynı zamanda bilim insanları otofajiyi de araştırıyor; bazen tümör hücrelerinin radyasyon ve kemoterapi sırasında “kendini temizleme” ile dayanmasına engel olmak için bloke ediliyor, bazen ise otofajiyi sınırlarının ötesine iterek hücre ölümünü tetiklemek için kullanılıyor. Klorokin ve hidroksiklorokin gibi ilaçlarla yürütülen erken klinik denemeler, otofajinin hastalarda güvenle modüle edilebileceğini gösterse de net sağkalım faydaları henüz kanıtlanmamıştır.
Laboratuvardaki Keşiflerden Kişiselleştirilmiş Bakıma
Bu kavramları gerçek dünyadaki tedavilere dönüştürmek zorlu olmaya devam ediyor. Gliomlar hastadan hastaya ve tek bir tümör içinde büyük çeşitlilik gösterir, bu nedenle tek bir ölüm yolu stratejisi herkes için uygun olmayacaktır. Kan–beyin bariyeri hâlâ ilaç dağıtımını engelliyor ve bağışıklık mikroçevresi en akıllıca kombinasyonları bile etkisiz hale getirebilir. Yazarlar umut verici yönleri vurguluyor: ferroptoz indükleyicilerini bağışıklık kontrol noktası inhibitörleriyle eşleştirmek, onkolitik virüsleri kanser hücrelerinin “beni ye” sinyallerini artıran ilaçlarla birleştirmek veya seçilmiş kemoradyasyon rejimlerine otofaji düzenleyiciler eklemek. Çoklu-omik profil çıkarma ve daha iyi biyobelirteçler, hangi hastaların belirli strateji karışımlarından en çok yararlanacağını belirlemede yardımcı olmalıdır.
İleriye Bakış: Tümörleri Kendi Kendini Yok Etmeyi Seçmeye Zorlamak
Basitçe ifade etmek gerekirse, bu makale glioma tedavisinin geleceğinin tümör hücrelerini dikkatle kontrol edilen biçimlerde kendi kendini yok etme düğmesine basmaya zorlamaktan geçebileceği sonucuna varıyor. Piyroptozu, ferroptozi, nekroptozi ve otofaji-bağımlı ölümü nasıl tetikleyeceğimizi ve koordine edeceğimizi öğrenerek—ve bunları modern immünoterapiler ve hassas ilaç teslimatıyla birleştirerek—araştırmacılar şu anki karanlık bir tanıyı daha yönetilebilir ve nihayetinde daha tedavi edilebilir hale getirmeyi umuyorlar.
Atıf: Guo, J., Zong, L., Huang, Y. et al. Unlocking glioma vulnerabilities: targeting regulated cell death pathways for innovative therapies. Cell Death Discov. 12, 95 (2026). https://doi.org/10.1038/s41420-026-02949-8
Anahtar kelimeler: glioma, düzenlenmiş hücre ölümü, piyroptoz, ferroptoz, glioblastoma tedavisi