Clear Sky Science · tr
Pankreas kanserinde mitofaji: mekanistik içgörüler ve yeni terapötik stratejiler için çıkarımlar
Neden hücrelerimizin enerji santralleri pankreas kanserinde önemli?
Pankreas duktal adenokarsinomu en ölümcül kanserlerden biridir; kısmen tümörlerin doktorların uyguladığı hemen her tedaviye hızla direnç kazanması nedeniyle. Bu derleme makalesi, direnç hikâyesinde beklenmedik bir oyuncuyu inceliyor: mitofaji, hücrenin eskimiş mitokondrileri tanıma ve geri dönüştürme sistemi—enerji üreten küçük “enerji santralleri”. Pankreas kanserinin bu temizlik sürecini nasıl ele geçirdiğini anlamak, daha etkili ve daha kalıcı tedavilere giden yeni yollar açabilir.
Hücresel temizlik ekipleri ve kanserin hayatta kalma hileleri
Mitokondriler sadece enerji üretmez; metabolizmayı, hücre ölümünü ve reaktif oksijen türleri olarak adlandırılan zararlı moleküllerin yönetimini de kontrol ederler. Mitokondriler hasar gördüğünde veya fazla olduğunda hücreler bunları etiketleyip ortadan kaldırmak için mitofajiyi kullanır. Bu iki ana yol aracılığıyla olabilir. PINK1/Parkin yolu olarak bilinen birinci yol, hatalı mitokondrileri yıkım için işaretlemek üzere bir hasar sensörü (PINK1) ve bir etiketleme enzimi (Parkin) kullanır. Diğer yol ise BNIP3, NIX ve FUNDC1 gibi mitokondri yüzeylerinde yer alan reseptör proteinlerini kullanarak aynı etiketleme adımı olmadan doğrudan onları otofagosom adı verilen hücresel atık torbalarına bağlar. Bu yollar sıklıkla birlikte çalışarak hücrelere düşük oksijen ya da ilaç maruziyeti gibi strese karşı mitokondri stoklarını esnek biçimde ayarlama imkanı verir. 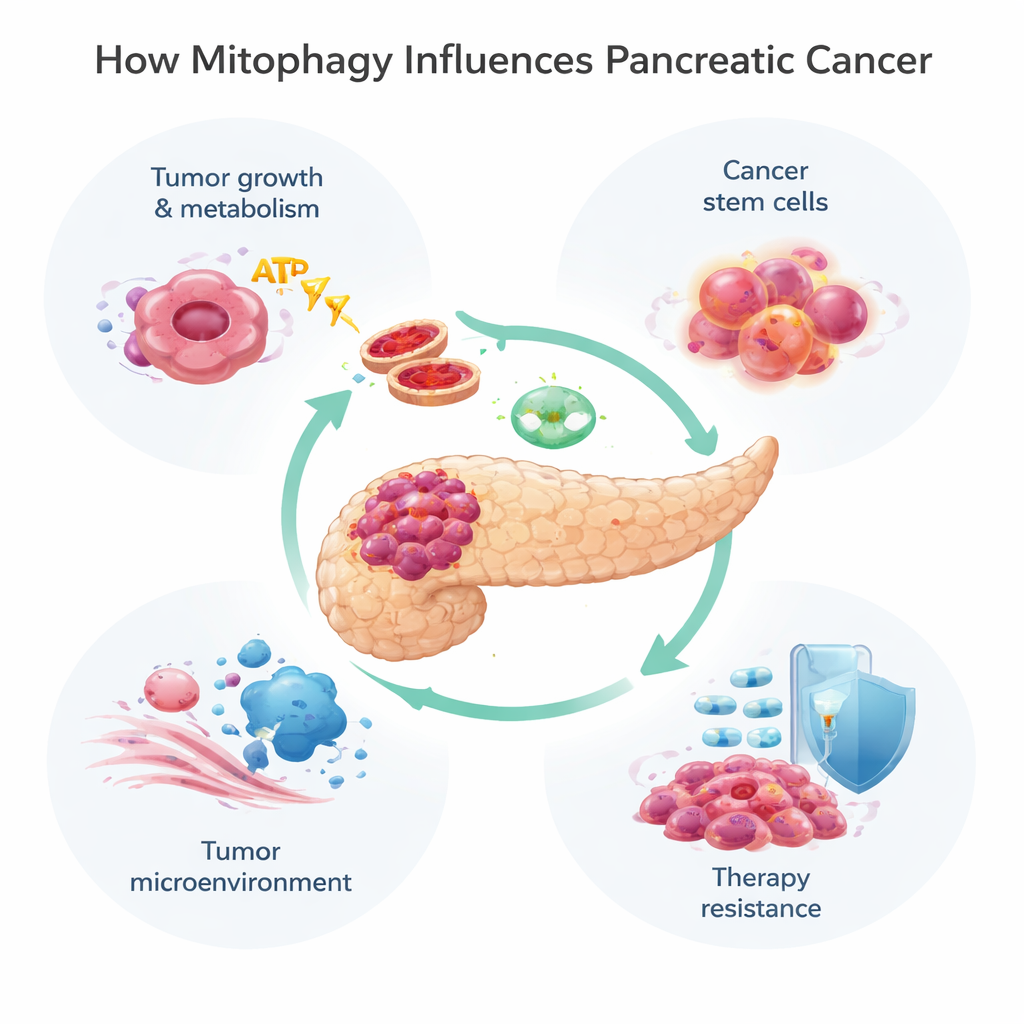
Pankreas tümörleri enerji kullanımını nasıl yeniden şekillendirir?
Pankreas tümörleri zorlu bir ortamda yaşar: kan ve oksijen arzı zayıftır ve yoğun yara benzeri doku ile çevrilidir. Hayatta kalmak için kanser hücreleri enerji sistemlerini yeniden kablolayarak sıklıkla mitokondride oksijene dayalı solunumdan daha ilkel bir şeker yakma süreci olan glikolize yönelir. Mitofaji bu geçişi ince ayarlar. Tümör gelişiminin erken dönemlerinde PINK1 veya Parkin kaybı demir birikimine, artmış reaktif oksijen türlerine ve glikolize doğru bir itmeye izin vererek kanser oluşumunu hızlandırır. Aynı zamanda başka bir mitofaji proteini olan NIX hâlâ işlevsel mitokondrileri kaldırarak hücreleri daha da glikolitik bir metabolizmaya itebilir ve büyümeyi hızlandırabilir. Buna karşılık BNIP3 daha karmaşık bir desen gösterir: erken dönemde görülür, birçok ilerlemiş tümörde daha sonra susturulur ve geri getirildiğinde kanser hücresi büyümesini yavaşlatabilir; bu da bazı mitofaji yollarının kanseri sınırlarken bazılarının onu beslediğini düşündürür.
Kanser kök hücreleri ve tümörün çevresi
Tüm kanser hücreleri eşit değildir. Küçük bir alt grup, sıklıkla kanser kök hücreleri olarak adlandırılanlar, kendini yenileyebilir, yeni tümörler tohumlayabilir ve özellikle kemoterapiye karşı dayanma yeteneğine sahiptir. Pankreas kanserinde bu hücreler metabolik esnekliğini korumak için mitofajiye bağımlıdır. ISG15 adındaki bir düzenleyici protein bu süreci destekler ve onların kök-hücre benzeri özelliklerini sürdürmesine yardım ederek mitofajiyi doğrudan nüks ve tedavi başarısızlığıyla ilişkilendirir. Kanser hücrelerinin ötesinde, mitofaji tümör mikroçevresini—tümörün etrafındaki destek hücreleri, bağışıklık hücreleri ve bağ dokusu karışımını—şekillendirir. Örneğin kanserle ilişkili fibroblastlar, kendi mitofajilerini ve glikolizlerini artırdıkları, sonra tümörü enerji açısından zengin yan ürünlerle besledikleri bir “ters Warburg etkisi”ne sürüklenebilir. Mitofaji ayrıca bağışıklık hücrelerinin kanseri tanıma ve saldırma biçimini değiştirerek MHC‑I gibi bağışıklık işaretlerinin ve tümörlerin saklanmak için kullandığı PD‑L1 gibi frenlerin gösterimini etkiler.
Temizlemeyi engellemek veya artırmak ilaç yanıtını neden değiştirebilir
Gemcitabin gibi kemoterapi ilaçları ve yaygın KRAS‑G12D mutasyonuna yönelik yeni hedefe yönelik ilaç da dahil olmak üzere birçok standart ve deneysel pankreas kanseri tedavisi mitokondrilere zarar verir. Tümör hücreleri genellikle mitofajiyi açarak yanıt verir, hasarı temizler ve ölümden kaçınır. Çalışmalar, PINK1 kaynaklı mitofajinin kemoterapinin ve bazı doğal bileşiklerin öldürücü etkilerini azaltabileceğini ve kanser hücrelerinin hayatta kalmasına yardımcı olduğunu gösteriyor. Öte yandan, belirli koşullar altında mitofajiyi—özellikle BNIP3 ve NIX yoluyla—aşırı tetiklemek, hücreleri çok fazla işlevsel mitokondriden yoksun bırakıp enerji krizine sokarak hücre ölümünü teşvik edebilir. Bu ikili doğa, mitofajinin tümörleri ya tedaviden koruyabileceği ya da doğru şekilde zorlandığında onları daha hassas hale getirebileceği anlamına gelir. 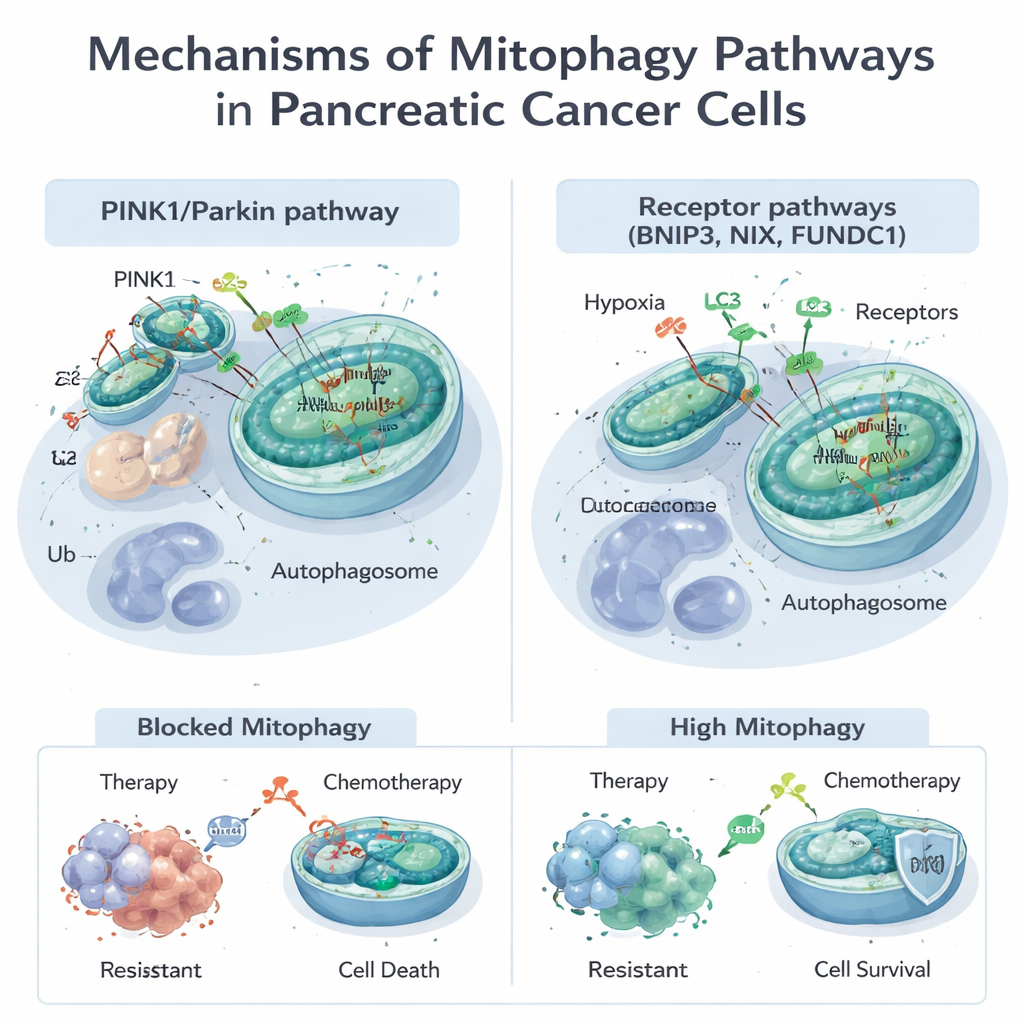
Yeni tedavi fikirleri ve doğru hasta eşleştirmeye duyulan ihtiyaç
Mitofaji metabolizma, stres yanıtları ve hücre ölümü kavşağında yer aldığı için kombinasyon terapileri açısından cazip bir hedeftir. Mevcut ilaç stratejileri çoğunlukla dolaylı etki gösterir: bazı bileşikler mitokondri bölünmesi ve kaynaşması ile etkileşir; diğerleri, kininolinin türevleri olan klorokin ve hidroksiklorokin gibi ilaçlar, atık torbalarının asidik sindirim keseleriyle kaynaşmasını engelleyerek geri dönüşüm sürecinin son aşamalarını bloke eder. Birkaç klinik çalışma bu ilaçları pankreas kanserinde standart kemoterapiyle birlikte test ediyor. Ancak şimdiye kadar sonuçlar karışık—bazı hastalar fayda görüyor, bazıları görmüyor. Sorunun bir kısmı tümörlerin temel mitofaji ve metabolik profiller bakımından büyük farklılık göstermesidir: bazıları mitokondriyal solunuma, bazıları glikolize büyük ölçüde dayanır. Yazarlar, gelecekteki başarının mitofaji aktivitesine ve enerji kullanımına göre hastaları gruplamak için daha iyi biyobelirteçler ve gen imzalarına; ayrıca otofajiyi kaba bir şekilde açıp kapatmak yerine belirli mitofaji yollarını seçici olarak ayarlayan daha hassas ilaçların geliştirilmesine bağlı olduğunu savunuyorlar. Halk için çıkarılacak ana mesaj, bu mitokondri temizlik sistemini okumayı ve dikkatli biçimde ayarlamayı öğrenmenin pankreas kanserini inatçı bir düşmandan daha yönetilebilir bir hastalığa dönüştürmeye yardımcı olabileceğidir.
Atıf: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Anahtar kelimeler: pankreas kanseri, mitofaji, mitokondri, kemoterapi direnci, tümör metabolizması