Clear Sky Science · tr
DIAPH3 kaybı farelerde glioma oluşumunu hızlandırıyor
Bu beyin çalışması neden önemli
Glioblastom en ölümcül beyin kanserlerinden biridir ve cerrahi, radyasyon ve kemoterapiye rağmen çoğu hasta bir yılı biraz aşan bir süre hayatta kalır. Bu çalışma temel ama kritik bir soruyu ele alıyor: Beyin hücreleri içinde hangi erken değişiklikler onları bu kadar agresif tümörlere doğru itiyor ve neden bu tümörleri radyasyonla yok etmek bu kadar zor? Araştırmacılar fare beyin hücrelerindeki tek bir yapısal proteini izleyerek, bu proteinin kaybının kromozomları nasıl istikrarsızlaştırdığını, tümör ortaya çıkışını nasıl hızlandırdığını ve kanser benzeri kök hücrelerin onları yok etmesi gereken radyasyona nasıl dayanmasını sağladığını ortaya koyuyor.
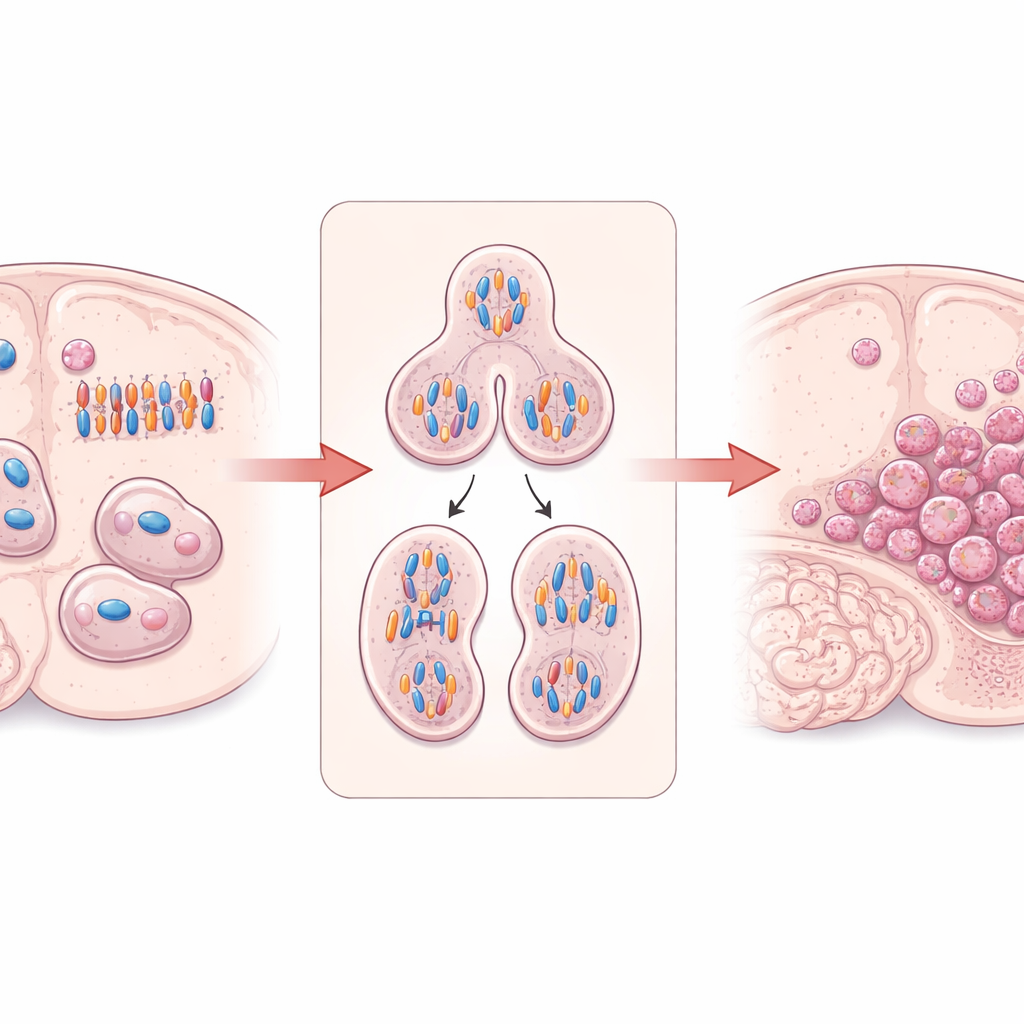
Bölünmeyi düzenleyen bir hücre “inşaatçısı”
Çalışma, hücrenin iç iskeleti olan aktin filamentleri ve mikrotübülleri kurup düzenlemeye yardımcı olan DIAPH3 proteinine odaklanıyor. Bölünen beyin kök hücrelerinde DIAPH3, çoğaltılmış kromozomları ayıran ve bir hücreyi ikiye bölen iğ biçimli yapının (spindle) doğru oluşumu için hayati önemdedir. Daha önceki araştırmalar, gelişen fare beyinlerinde DIAPH3 eksik olduğunda bölünen hücrelerin sık sık kromozomları yanlış yönettiğini, anöploidiye (anormal kromozom sayıları), duraklamış hücre döngülerine ve hücre ölümüne yol açtığını göstermişti. İlginç şekilde, insan kromozomu 13’te DIAPH3 genini içeren küçük bir bölge glioblastomlarda sıkça siliniyor ve bazı hastalarda daha yüksek DIAPH3 düzeyleri daha iyi sağkalımla ilişkilendirilmiş; bu da bu proteinin beyinde tümör baskılayıcı rolü olabileceğini düşündürüyor.
Tümör büyütmek için fare beyinlerini genetik olarak değiştirmek
DIAPH3 kaybının gerçekten beyin kanserini teşvik edip etmediğini test etmek için ekip, korteks oluşturan kök hücrelerde seçici olarak silinebilen iki gene sahip fareler yarattı: Diaph3 ve genomun bekçisi olarak bilinen p53’ü kodlayan Trp53. Yalnızca Diaph3’ü bu bölgede kaybeden fareler iki yıl bile geçse tümör geliştirmedi; bu da p53’ün hâlâ son derece anormal hücreleri ortadan kaldırabildiğini gösteriyor. Buna karşın yalnızca Trp53 eksikliği olan veya hem Trp53 hem Diaph3 eksik olan fareler, mikroskop altında insan hastalığına çok benzeyen yüksek dereceli difüz gliomlar geliştirdiler. Tekrarlanan ultra‑yüksek alanlı MRG taramaları kullanılarak, her iki geni de kaybeden hayvanların daha erken zamanda saptanabilir tümörler geliştirdiği ve orta yaşa gelindiğinde özellikle koku soğanlarında, yalnızca Trp53 eksik olan farelere göre daha sık büyük gliomlara sahip olduğu gösterildi. Tümör büyüme hızı başladıktan sonra gruplar arasında benzerdi—değişen şey tümörlerin ne kadar erken ortaya çıktığıydı.
Kromozom kaosu ve yeniden yapılandırılmış gen etkinliği
DIAPH3 kaybının tümör başlangıcını neden hızlandırdığını anlamak için ekip, henüz görünür tümör yokken genç farelerin koku soğanlarındaki gen etkinliğini inceledi. Hem Diaph3 hem Trp53 eksik olan hayvanlarda, yalnızca Trp53 mutantlarına kıyasla 126 gen farklı düzeylerde ifade ediliyordu ve bunların neredeyse yarısı daha önce kanserle ilişkilendirilmişti. Birçok değişiklik, VEGF, MAPK, RAS, Rap1 ve cAMP sinyal yolları ile G‑protein’e bağlı reseptör ağları dahil olmak üzere hücre büyümesini, göçünü ve damar oluşumunu yönlendiren yolların kümelendiğini gösteriyordu. Bu değişmiş moleküler manzara, hücrelerin daha erken bir kanser benzeri duruma doğru itildiğini düşündürdü. Tam genom kopya‑numarası analizi, tam gelişmiş tümörlerde DIAPH3 eksikliğinin küçük, odaklanmış DNA değişikliklerini büyük ölçüde artırmak yerine, hatalı kromozom segregasyonundan beklenen anöploidiye karşılık gelen büyük, tüm kromozom kazanımları ve kayıplarını artırdığını ortaya koydu.
İçten gelen DNA hasarı ve daha dayanıklı tümör kök hücreleri
Anöploid tümör hücreleri, hücre çekirdekleri genelinde yayılan yükselmiş DNA kırık belirteci γ‑H2AX düzeyleriyle tespit edilen daha fazla iç DNA hasarı taşıyordu. Yine de bu tümörler büyümeye devam etti; bu da onların bu tür stresi tolere etmenin yollarını edindiğini ima ediyor. Oturmuş tümörlerde gen ekspresyonunu karşılaştıran araştırmacılar, DIAPH3 kaybıyla yüzlerce genin değiştiğini ve birçok çift mutant tümörde büyüme faktörü reseptörü FGFR2’nin çarpıcı amplifikasyonu ve aşırı üretiminin olduğunu buldu. FGFR2, glioblastom hücrelerinde DNA tamir mekanizmalarını güçlendirmesiyle biliniyor ve aktivasyonu radyasyona dirençle ilişkilendirilmiş. Ekip fare tümörlerinden glioma kök‑benzeri hücreleri izole etti ve klinik açıdan anlamlı bir iyonize radyasyon dozu ile yanıtlarını test etti. Tedavi öncesinde kök‑benzeri hücre sıklığı her iki genotipte de benzerdi; ancak ışınlamadan sonra DIAPH3‑eksik tümörlerden elde edilen kültürlerde, yalnızca Trp53 eksiklerine ait kültürlere göre yaklaşık iki kat daha fazla aktif kök‑benzeri hücre kaldı; bu da daha yüksek radyodirenç gösteriyordu.
Beyin kanseri açısından ne anlama geliyor
Bir arada ele alındığında, çalışma DIAPH3’ü beyin kök hücrelerinin doğru kromozom sayısıyla bölünmesine yardımcı olan bir koruyucu olarak resmediyor. Hem DIAPH3 hem p53 eksik olduğunda, hücre bölünmesi hataya açık hale geliyor, tüm kromozomlar kaybediliyor veya kazanılıyor ve DNA hasarı birikiyor. Bazı hücreler ölmek yerine FGFR2 gibi tamirle ilişkili faktörleri amplifiye ederek uyum sağlıyor ve anöploid, yüksek dereceli gliomlara dönüşüyor; bu tümörlerin kök‑benzeri hücreleri radyasyona karşı alışılmadık derecede dirençli oluyor. Fare modelleri insan glioblastomunun her özelliğini yakalamasa da, bu bulgular DIAPH3’ü prognostik bir biyobelirteç potansiyeli ve tümör başlatma, genom kararlılığı ve tedavi yanıtını kontrol eden süreçler ağında bir düğüm olarak destekliyor—bu yıkıcı beyin kanserini mevcut tedavilere karşı daha savunmasız kılabilecek yeni tedavi yollarını açıyor.
Atıf: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Anahtar kelimeler: glioblastom, kromozomal kararsızlık, beyin tümör kök hücreleri, radyasyon direnci, tümör baskılayıcı genler