Clear Sky Science · tr
Kemoradyoterapi kaynaklı hücre ölümünden kaçınan glioblastoma hücreleri iki kollu bir glikolitik program sergiliyor
Bu beyin kanseri çalışması neden önemli
Glioblastoma, erişkinlerdeki en ölümcül beyin kanserlerinden biridir ve cerrahi, kemoterapi ve radyasyon sonrası neredeyse her zaman yeniden büyür. Bu çalışma hayati bir soruyu gündeme getiriyor: tedaviden kurtulan ve daha sonra hastalığı yeniden alevlendiren küçük tümör hücresi grubunda ne özel? Araştırmacılar bu hücrelerin zaman içinde şekeri nasıl işlediğini izleyerek, mevcut tedavilerin neden bu kadar sık başarısız olduğunu açıklayabilecek gizli bir hayatta kalma stratejisi ortaya çıkarıyor ve tümörün yaşam hattını kesmeye yönelik yeni yollar öneriyor.
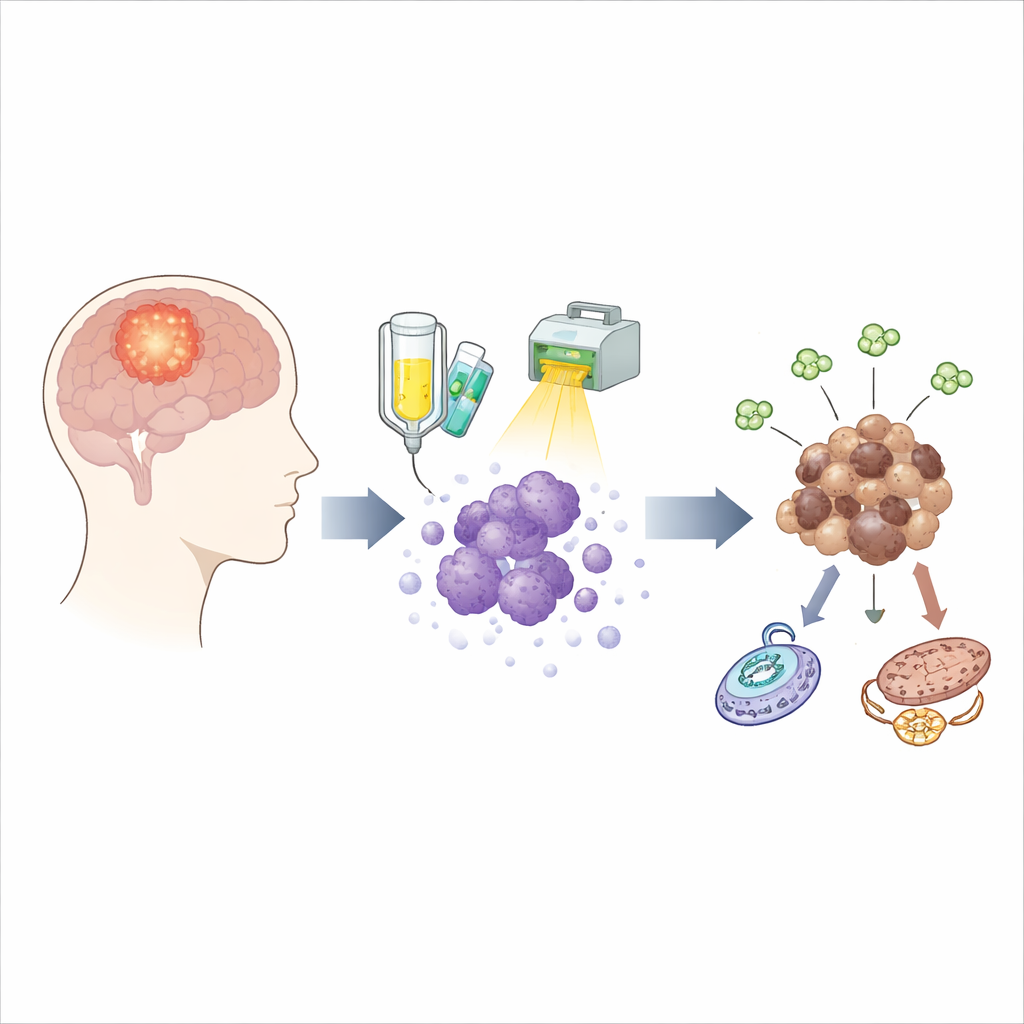
Tedavi sonrası gizlenen hayatta kalanlar
Glioblastoma için standart bakım, temozolomid adlı bir ilaç ile radyasyonun kombinasyonunu içerir. Bu kombinasyon çoğu tümör hücresini öldürse de, inatçı bir azınlık hayatta kalır ve aylar sonra yeni bir tümör tohumlayabilir. Bu sağ kalanları eylem halinde yakalamak için ekip, doğrudan on farklı hastadan alınan tümör hücrelerini kullanarak klinikte uygulananlara yakın olacak şekilde tasarlanmış bir tedavi rejimine maruz bıraktı. Tedavi sırasında ve sonrasında birkaç noktada yaşayan hücreleri örneklediler ve ayrıca eşleşen tümörleri farelerde yetiştirerek, nüks öncesi ve sonrası karşılaştırmanın ötesinde hayatta kalanların zaman içinde nasıl değiştiğini izleyebildiler.
Tümör hücreleri şeker kullanımını nasıl değiştiriyor
Beyin dokusu vücudun şekerinin dikkate değer bir kısmını tüketir ve glioblastoma hücreleri özellikle bunun için açtır. Araştırmacılar, tedavi ilerledikçe hayatta kalan hücrelerin çevrelerinden daha fazla glikoz çektiğini buldular. Ancak şaşırtıcı şekilde bu ekstra yakıtı daha hızlı yakmadılar. Bunun yerine bu hücreler tipik olarak hızlı şeker parçalanmasının atık ürünü olan laktat üretimini azalttı. Anahtar proteinlerin ölçümleri belirgin bir bölünmüş desen gösterdi: şekeri hücre içine getiren ve parçalanmayı başlatan bileşenler artarken, daha sonraki adımları ve laktat üretimini yönetenler azaldı. Bu “iki kollu” program, şekerin hücreye girip işlemeye başlandığı, ancak laktata giden olağan çıkış yolunun kısmen kapalı olduğu anlamına geliyor.
Yakıtı yapı taşlarına ve enerji santrallerine yönlendirmek
Yönlendirilen şeker nereye gidiyor? Özel işaretli glikoz ve ileri metabolit ölçümleri kullanarak ekip, hayatta kalan hücrelerin bu karbonun büyük kısmını iki ana hedefe yönlendirdiğini gösterdi. Birincisi, DNA ve RNA yapı taşlarını üretmek için gerekli hammaddeleri oluşturan pentoz fosfat yolu adlı yan rotadır. Bu hücrelerde birçok nükleotid bileşeni ve ilgili genler artmıştı; bu da onarım ve yeniden büyümeye hazırlık yönünde güçlü bir itki olduğunu gösteriyor. İkinci hedef hücrenin enerji santralleri olan mitokondriler. Mitokondriyal enerji döngüsünün enzimleri arttı ve aynı grubun önceki çalışmaları şeker kaynaklı yakıtın bu yapılara daha fazla ithal edildiğini göstermişti. Birlikte bu, laktata giden israfcı fermantasyonun azaltıldığı, onarım, büyüme malzemeleri ve esnek enerji üretimine daha fazla yatırım yapılan koordine bir yeniden kablolamayı ortaya koyuyor.
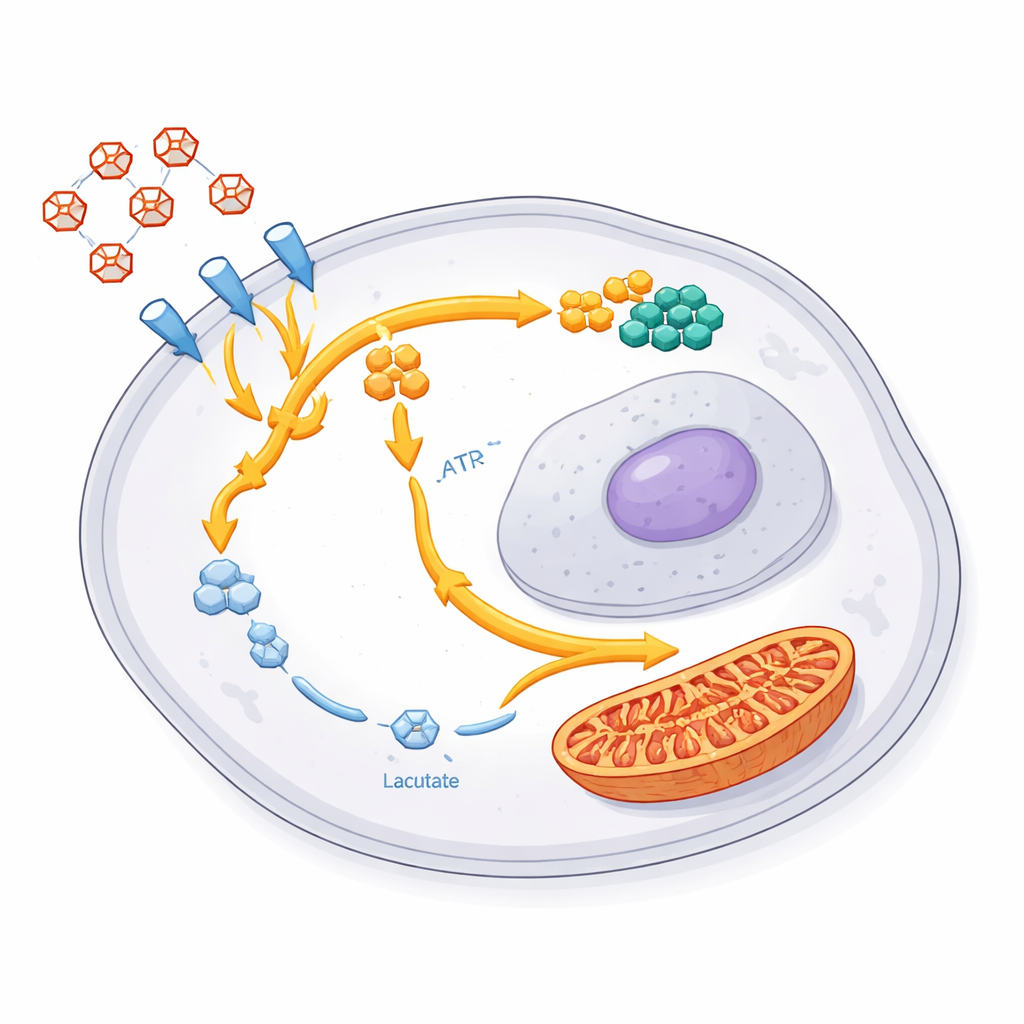
Tümörlerde ve hayvanlarda ortak bir hayatta kalma oyun kitabı
Glioblastoma tümörleri hasta bazında büyük farklılıklar gösterir ve bu durum çoğu zaman tek tip tedavileri boşa çıkarır. Bu çeşitliliğe rağmen, on hasta kaynaklı modelin her biri kemoradyoterapiden sonra aynı temel kaymayı gösterdi: artmış erken şeker işleme adımları, azalmış geç adımlar ve laktat çıkışı ile artmış mitokondriyal aktivite. Önemli olarak, aynı imza hastadan elde edilen hücrelerden büyütülen ve uyarlanmış standart tedavi uygulanan fare beyin tümörlerinde de ortaya çıktı. Bu hayvanlardaki rekürren tümörler hâlâ değişmiş şeker programını taşıyordu; bu da bunun geçici bir etki değil, tedaviyi atlatıp kanseri yeniden kurmayı başaran hücrelerin kalıcı bir özelliği olduğunu gösteriyor.
Gelecek tedaviler için ne anlama geliyor
Halkın anlayacağı şekilde ana mesaj şudur: hayatta kalan glioblastoma hücreleri sadece tedaviden “saklanmıyor”; hayatta kalmak için şekeri nasıl kullandıklarını aktif olarak yeniden yapılandırıyorlar. Daha fazla glikoz çekiyor, onu atığa dönüştürmekten kaçınıyor ve bunun yerine DNA yapı taşlarını üretmeye ve mitokondrileri güçlendirmeye yönlendiriyorlar—bu da onların hasarı onarmasına, esnek, kök hücre benzeri bir durumu sürdürmesine ve sonunda tümörü yeniden büyütmesine yardımcı oluyor. Bu ortak metabolik hayatta kalma durumunu ortaya koyarak çalışma, erken şeker işleme adımlarını, DNA üretimine giden yan rotayı veya bu hücrelerin mitokondriyal bağımlılığını hedeflemenin standart kemoradyoterapinin daha tam olmasını sağlayabileceğini ve hastalığı yeniden başlatacak daha az kaçak bırakacağını öne sürüyor.
Atıf: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Anahtar kelimeler: glioblastoma, kanser metabolizması, glikoz kullanımı, tedavi direnci, pentoz fosfat yolak