Clear Sky Science · tr
HNF4α-HKDC1 ekseni, ileri evre mide kanserinde göç ve metastazı teşvik etmek için metabolik bir yeniden programlama düzenliyor
Hastalar için neden önemli
Mide kanserinden kaynaklanan ölümlerin çoğu, birincil tümör yüzünden değil; kanser hücrelerinin vücudun uzak bölgelerine göç edip orada kök salması nedeniyle gerçekleşir. Bu çalışma, mide (gastrik) kanseri hücrelerinin yakıt kullanımlarını değiştirmelerine ve daha hareketli hale gelmelerine yardımcı olan gizli bir moleküler "açma düğmesini" ortaya koyuyor. Daha da önemlisi, bu düğmeyi kapatmak ve yayılmayı yavaşlatmak veya önlemek amacıyla yeniden kullanılabilecek mevcut, FDA onaylı bir ilaca işaret ediyor.
Mide kanserinde tehlikeli bir dönüşüm
Mide kanseri dünya genelinde en sık görülen beşinci kanserdir ve genellikle yayıldıktan sonra geç evrede tespit edilir. Yazarlar, tümör hücrelerinin ayrılıp karın boşluğu veya kan damarları yoluyla hareket ettiği ve yeni bölgeleri kolonize ettiği adım olan metastaza odaklandı. Geniş halka açık kanser veritabanlarını tarayarak ve hasta doku örneklerini inceleyerek, P2 promotörü tarafından yönlendirilen HNF4α'nın özel bir versiyonunun (P2‑HNF4α) birincil tümörlere ve yakınındaki sağlıklı dokulara kıyasla uzak metastatik lezyonlarda özellikle bol olduğunu buldular. Bu versiyonun çevreleyen normal hücrelerde değil şiddetle tümör hücreleri içinde bulunduğu tespit edildi; bu da onun kanserin invaziv davranışıyla sıkı bir bağlantısı olduğunu gösteriyor.
Hücre hareketini artıran bir ana anahtar
Neden‑sonuç ilişkisini test etmek için araştırmacılar, hastalığın başlıca moleküler alt tiplerini temsil eden bir dizi insan mide kanseri hücre hattında P2‑HNF4α düzeylerini değiştirdiler. Normalde HNF4α ifade eden hücrelerde HNF4α'yı azalttıklarında, hücrelerin yapay membranlar boyunca göç etme ve invaze olma ya da kültür kabında yara kapatma yeteneği belirgin şekilde düştü. Düşük HNF4α'ya sahip hücrelerde temsili bir P2‑HNF4α izoformunu zorlayarak fazla ürettiklerinde, bu hücreler üç boyutlu tümörü taklit eden sferoid testleri dahil olmak üzere belirgin şekilde daha hareketli ve invaziv hale geldi. Farelerde P2‑HNF4α'yı fazla üreten hücreler, karın boşluğu boyunca çok daha fazla metastatik nodül oluşturdu; bu da bu faktörün canlı organizmalarda yayılmayı aktif olarak sürdürdüğünü gösteriyor.
Enerji kullanımını yeniden programlayarak yayılmayı beslemek
Kanser hücreleri genellikle büyümeyi ve hareketi desteklemek için besin işleme yollarını yeniden şekillendirir. Eşzamanlı RNA dizileme ve metabolit profillemesi kullanarak ekip, HNF4α'nın azaltılmasının glikoliz adı verilen önemli bir enerji üreten yolu zayıflattığını keşfetti. Bir dizi glikolitik enzimin ve ara ürünün düzeyleri düştü; oksijen tüketimi, asit üretimi ve ATP üretimi gibi enerji çıktısı ölçümleri de azaldı. Daha ileri analizler, HNF4α ile en güçlü ve tutarlı bağlantılı olan enzim olarak HKDC1'i öne çıkardı. HKDC1, glukoz işleme sürecinin en ilk adımında yer alır ve şekeri hem laktat üretimine hem de mitokondriyal solunuma yönlendirmeye yardımcı olur — bu iki yol birlikte enerji sağlar ve hücre hareketini kolaylaştıran bir kimyasal ortam yaratır.
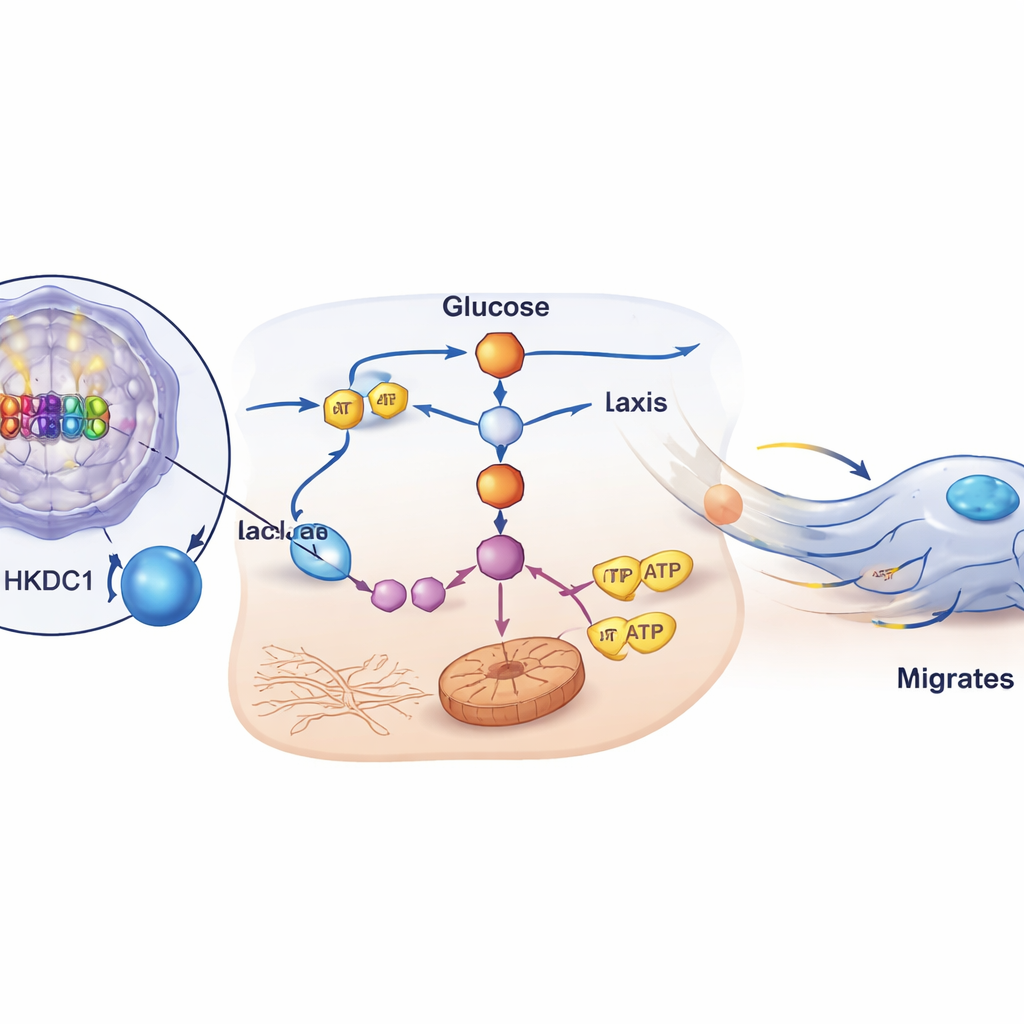
Doğrudan moleküler bağlantı ve kilit bir suç ortağı
Bilim insanları P2‑HNF4α'nın sadece HKDC1 ile korele olmadığını; bu geni doğrudan aktive ettiğini gösterdi. Genom çapında bağlanma verileri, DNA raporlayıcı testleri ve protein–DNA bağlanma deneyleri kullanarak HNF4α'nın oturup transkripsiyonu aktive ettiği HKDC1 geninin bir güçlendirici bölgesindeki spesifik bölgeleri haritaladılar. HKDC1 hücrelerde azaltıldığında, kısa dönem hayatta kalma etkilenmese bile bu hücrelerin göç etme ve farelerde peritoneal metastazlar oluşturma yeteneği çarpıcı şekilde düştü. Kritik olarak, HNF4α baskılandığı hücrelerde HKDC1’in yeniden sağlanması glikolitik aktiviteyi, enerji üretimini ve göç davranışını kurtardı; laktat veya α‑ketoglutarat gibi metabolik son ürünlerin eklenmesi de hareketi geri getirdi. Bu bulgular birlikte, HKDC1'in P2‑HNF4α'nın metabolizmayı yeniden programlayarak metastaza güç veren merkezi bir aşağı akış etkinleştiricisi olduğunu savunuyor.
Mevcut bir ilaçla düğmeyi kapatmak
HNF4α genellikle ilaç hedefi olabilecek protein ailesine ait olduğundan ekip, onaylı bir ilacın bu pro‑metastatik ekseni engelleyip engelleyemeyeceğini test etti. Araştırmacılar daha önce nakil ilacı miykofenolat mofetilin (MMF) aktif formu miykofenolik asidi akciğer kanserinde HNF4α antagonisti olarak tanımlamışlardı. Burada MMF tedavisi, yüksek HNF4α ifade eden mide kanseri hatlarında HKDC1 düzeylerini ve hücre göçünü azalttı; düşük HNF4α'ya sahip hücrelerde ise çok az etkisi oldu. Fare modellerinde MMF, karın metastazlarını anlamlı biçimde azalttı ve HKDC1 ekspresyonunu düşürdü — ancak yalnızca tümörler yüksek P2‑HNF4α taşıdığında. Bu, HNF4α'nın hem terapötik bir hedef hem de MMF bazlı stratejilerden fayda görmesi muhtemel hastaları seçmek için bir biyobelirteç olarak hizmet edebileceğini öne sürüyor.
Gelecek bakım için anlamı
Düz bir dille ifade etmek gerekirse, bu çalışma P2‑HNF4α'nın HKDC1 aracılığıyla çalıştığı moleküler bir yakıt‑kontrol sistemini tanımlıyor; bu sistem mide kanseri hücrelerinin enerji makinesini hızlandırmasına ve yayılmada daha başarılı olmasına yardımcı oluyor. Mevcut bir ilacın bu sistemi bozabildiğini ve preklinik modellerde metastazı azaltabildiğini göstererek ileri evre mide kanseri için yeni tedavilere ulaşma yolunu gerçekçi kılıyor. Gelecekteki klinik çalışmalar bu bulguları doğrularsa, tümörlerde HNF4α aktivitesinin test edilmesi MMF veya ilgili ajanların kullanımıyla bu hastalığın ölümcül yayılmasını yavaşlatma veya önleme konusunda yol gösterici olabilir.
Atıf: Xu, X., Wu, H., Shang, J. et al. HNF4α-HKDC1 axis orchestrates a metabolic rewiring to promote migration and metastasis in advanced gastric cancer. Cell Death Dis 17, 347 (2026). https://doi.org/10.1038/s41419-026-08627-y
Anahtar kelimeler: mide kanseri metastazı, HNF4A, HKDC1, kanser metabolizması, miykofenolat mofetil