Clear Sky Science · tr
GGCT tarafından yönlendirilen metabolik düzen: tümör proliferasyonu için glutaminin glutatiyon biyosentezine yönlendirilmesi ve glikoz anaplerozisinin artırılması
Kanser tedavisi açısından neden önemli
Kanser hücreleri hızlı büyür; bunun için büyük miktarda yakıt tüketirler ve kendi metabolizmalarının toksik yan ürünlerine karşı sürekli korunmak zorundadırlar. Bu çalışma, az bilinen bir enzim olan GGCT’nin, karaciğer ve prostat tümörlerinin iki yaygın besini—glutamin ve glikoz—ü akıllıca nasıl yeniden yönlendirerek hem büyümeyi desteklediğini hem de reaktif oksijen türleri adı verilen zararlı molekülleri kontrol altında tuttuğunu ortaya koyuyor. Bu metabolik ustalık anlaşılırsa, tümörleri aç bırakmanın veya savunmalarını bozmaya yönelik yeni stratejilerin geliştirilmesine kapı açabilir.
Tümör hücreleri yakıt ve korumayı nasıl dengeliyor
Tümör hücreleri glutamine büyük ölçüde bağımlıdır; bu amino asit iki yönlü bir rol oynar: hücrenin ana enerji üreten döngüsünü beslemek üzere parçalanabilir ve aynı zamanda güçlü bir antioksidan olan glutatiyon için yapı taşları sağlar; glutatiyon reaktif oksijen türlerini etkisizleştirir. Yazarlar önce karaciğer tümörlerinde glutamin düzeylerinin çevre sağlıklı dokuya göre daha yüksek olduğunu doğruladı ve daha fazla glutaminle yetiştirilen kanser hücrelerinin hem kültürde hem de fare modellerinde daha hızlı bölündüğünü gösterdi. Glutamin kıt olduğunda hücreler yavaşlıyor, önemli hücre döngüsü proteinleri azalıyor ve hayvanlardaki tümörler küçülüyor—kısmen antioksidan savunmalar zayıfladığı ve reaktif oksijen türleri biriktiği için.
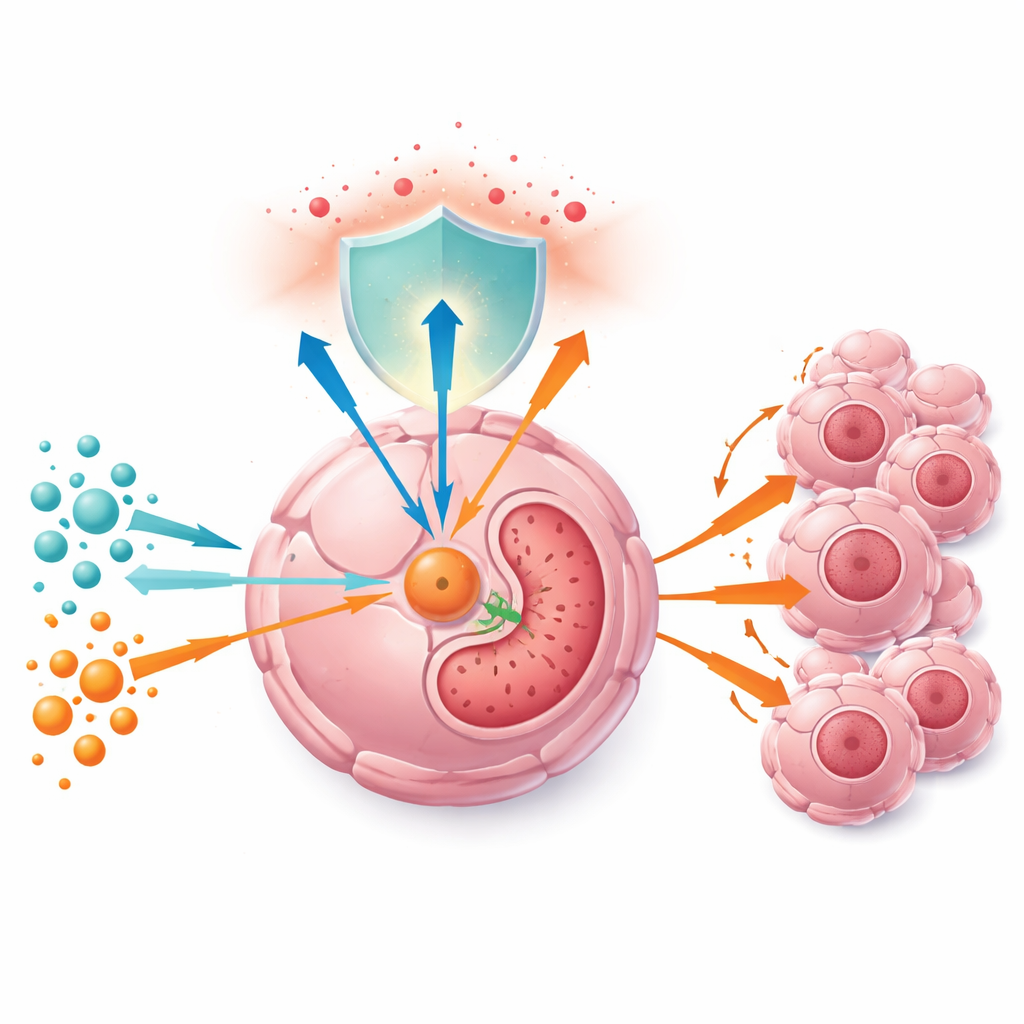
Açıkta gizlenen bir metabolik anahtar
Hasta örnekleri ve büyük kanser veri tabanlarına bakıldığında, ekip GGCT enziminin karaciğer ve prostat tümörlerinde normal dokulara göre tutarlı şekilde daha bol bulunduğunu ve daha yüksek GGCT düzeylerinin daha kötü sonuçları öngördüğünü tespit etti. Hem tümör örneklerinde hem de kültürdeki hücrelerde GGCT düzeyleri glutamin konsantrasyonu ile paralel arttı; bu, tümörlerin glutamin mevcudiyetini bu protein aracılığıyla “okuduğuna” işaret ediyor. Araştırmacılar bir kontrol zincirini çözdü: glutamin büyümeyi destekleyen faktör c‑Myc’i aktif tutuyor, bu da miR‑29b‑3p adındaki küçük düzenleyici RNA’yı baskılıyor; miR‑29b‑3p düşük olduğunda GGCT üzerindeki kısıtlama kalkıyor ve enzim birikiyor. Glutamin azaldığında bu zincir tersine dönüyor, miR‑29b‑3p yükseliyor, GGCT mesajları daha hızlı parçalanıyor ve enzim düzeyi düşüyor.
Glutamini yeniden yönlendirmek ve daha fazla glikoz çekmek
GGCT’nin hücre içinde gerçekte ne yaptığını görmek için yazarlar enzim düzeylerini azalttı veya artırdı ve hem hücre davranışını hem de yüzlerce metaboliti ölçtü. GGCT susturulduğunda hücreler bölünme döngüsünde durdu, kolonileri küçüldü ve glutatiyon belirgin şekilde azalıp reaktif oksijen türleri arttı; kimyasal bir antioksidanın eklenmesi büyümeyi kısmen kurtardı. Mikroskop altında mitokondriler anormal şekilde uzamış ve oksijen tüketiminde daha az verimli hale gelmişti; buna karşın hücreler glikolizi, yani şeker yıkımının ilk adımını artırarak telafi etmeye çalıştı. Ayrıntılı metabolik profilleme, GGCT kaybolduğunda merkezi enerji döngüsünün ara ürünlerinin düştüğünü, aşırı üretildiğinde ise yükseldiğini gösterdi.
Karbon atomlarının izini sürmek
Ekip daha sonra işaretlenmiş glutamin ve glikoz atomlarının tümör metabolizmasında nasıl aktığını izledi. GGCT aşırı eksprese edildiğinde, işaretli glutaminin enerji döngüsüne daha az ulaştığı ve daha fazlasının yeni yapılan glutatiyona yönlendirildiği; bu da antioksidan savunmayı destekledi. Aynı zamanda işaretli glikoz enerji döngüsüne daha güçlü katkıda bulunarak yönlendirilen glutamini telafi etti. Normal enzim aktivitesinden yoksun bir GGCT mutantı bu değişimleri tetikleyemedi veya çoğalmayı destekleyemedi; bu GGCT’nin katalitik işlevinin kritik olduğunu gösterdi. Önemli olarak, ekstra piruvat sağlanması veya enerji döngüsüne girişin ayarlanması hücresel enerji düzeylerini geri getirse de reaktif oksijen türlerini azaltmadı; bu, GGCT’nin esas olarak redoks dengesini basit enerji arzı değişiklikleriyle değil, glutatiyon aracılığıyla kontrol ettiğini gösteriyor.
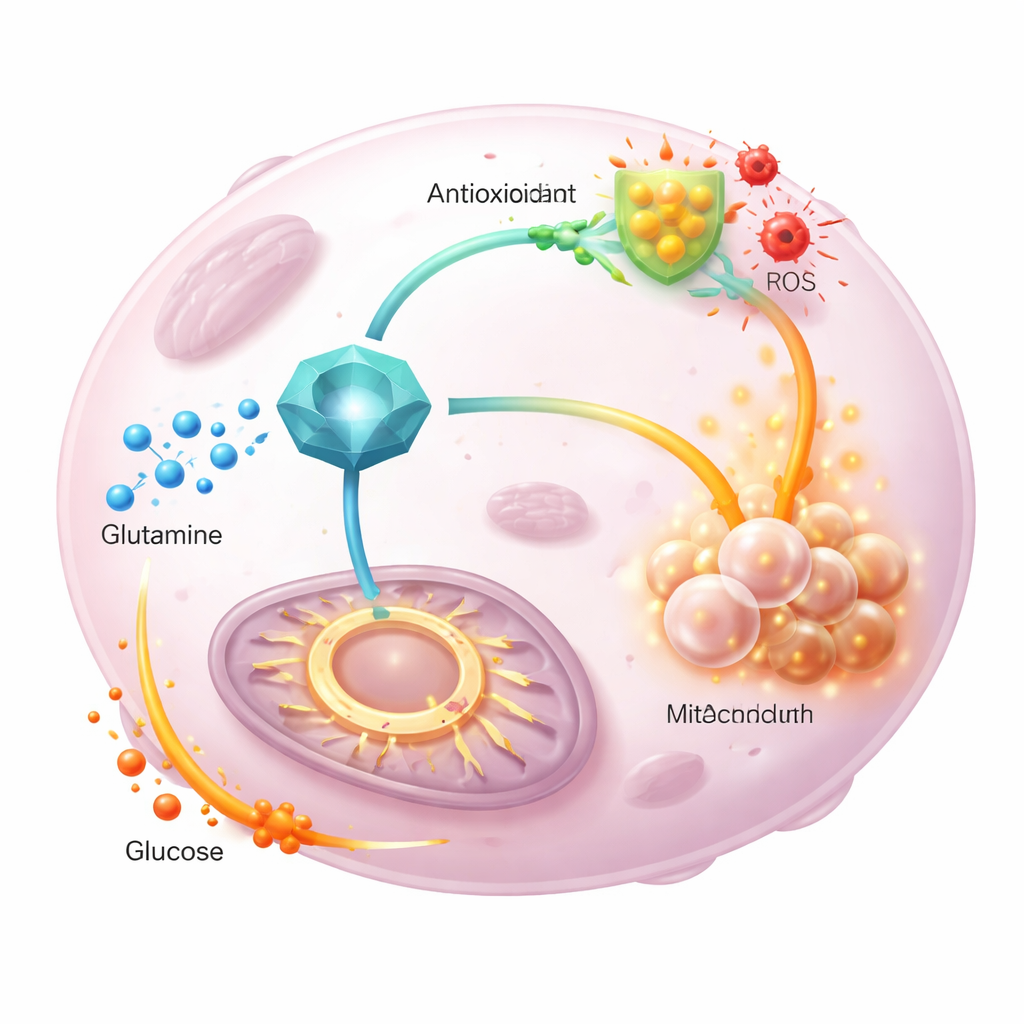
Gelecek terapiler için ne anlama geliyor
Genel olarak bulgular, GGCT’yi tümörlerin glutaminin görevlerini ayırmasına izin veren merkezi bir koordinatör olarak konumlandırıyor: bu besinin daha fazlasını antioksidan üretimine yönlendirirken glikozu enerji döngüsüne çekerek hücre bölünmesinin sürmesini sağlıyor. Hayvan modellerinde GGCT’nin susturulması tümör büyümesini yavaşlattı, glutatyonu azalttı ve oksidatif stresi artırdı; bu etkiler bir antioksidan ilaçla kısmen geri döndürülebildi. Genel okuyucu için çıkarılacak mesaj şudur: bazı kanserler GGCT’yi bir metabolik bağlantı anahtarı olarak kullanarak hayatta kalıyor; bu anahtarı devre dışı bırakan ilaçlar aynı anda tümörün oksidatif hasara karşı savunmasını zayıflatabilir ve besinlerin esnek kullanımını bozarak standart tedavilerin etkinliğini artırabilir.
Atıf: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Anahtar kelimeler: kanser metabolizması, glutamin, glutatiyon, oksidatif stres, GGCT enzimi