Clear Sky Science · tr
CBX2 faz-ayrışması, over kanserinde homolog rekombinasyon onarımına ve ilaç direncine katkıda bulunuyor
Bu araştırma neden önemli
Over kanseri, birçok tümörün kemoterapiye yanıt vermeyi bırakması nedeniyle kadınlarda en ölümcül kanserlerden biridir. Bu çalışma, yüksek dereceli seröz over kanserlerinin kullandığı gizli bir hayatta kalma hilesini ortaya koyuyor: hücre çekirdeği içinde, DNA onarımını aşırı hızlandıran küçük sıvı-benzeri damlacıklar oluşturuyorlar; bu da tümör hücrelerinin standart ilaçlarla verilen hasara karşı direnç kazanmasına yardımcı oluyor. Çalışma ayrıca, tümörleri bu damlacık tabanlı onarım sistemine dayanmış olan hastalarda bu zayıflıktan yararlanmak için mevcut bir ilaç olan Ibrutinib’i potansiyel bir seçenek olarak işaret ediyor.
DNA’sını çok iyi onaran tümör hücreleri
En güçlü kanser ilaçlarının çoğu, DNA’yı o kadar çok hasara uğratarak çalışır ki tümör hücreleri artık bölünemez hale gelir. Ancak yüksek dereceli seröz over kanserinde birçok tümör bu hasarı tamir etmede uzmanlaşır ve bu da platin kemoterapisi ve PARP inhibitörlerine karşı dirençle sonuçlanır. Yazarlar, DNA paketlemesindeki kimyasal işaretleri okuyan ve over tümörlerinde normal dokuya göre daha yüksek düzeyde bulunan CBX2 adlı proteine odaklandı. Hasta veri setleri ve doku örnekleri boyunca daha fazla CBX2 içeren tümörlerin platin tedavisine dirençli olma ve özellikle bu agresif over kanseri alt tipinde daha erken nüks etme olasılığı daha yüksekti.
Çekirdekteki damlacıklar: onarımı hızlandıran bir "çalışma tezgâhı"
CBX2, faz ayrışması olarak bilinen bir süreçle hücre çekirdeği içinde yoğun, damla benzeri kümeler oluşturma konusunda alışılmadık bir yeteneğe sahip. Bu damlacıklar, belirli proteinleri yoğunlaştırabilen küçük sıvı çalışma tezgâhları gibi davranır. Araştırmacılar, normal CBX2, CBX2 yokluğu veya damlacık oluşturamayan bir mutant formu olan kanser hücrelerini karşılaştırarak CBX2 damlacıklarının tümör hücrelerinin kırık DNA’yı nasıl onardıklarında merkezi bir rol oynadığını gösterdi. CBX2 çıkarıldığında kromozomlar daha sık kırıldı, DNA hasar sinyalleri birikti ve iki ana DNA çift zincir kırığı onarım yolu zayıfladı. Normal CBX2 geri getirildiğinde bu onarım yetenekleri geri geldi, ancak damlacık oluşturmaya yetmeyen bir versiyon, DNA’ya bağlanabiliyor olmasına rağmen işe yaramadı. 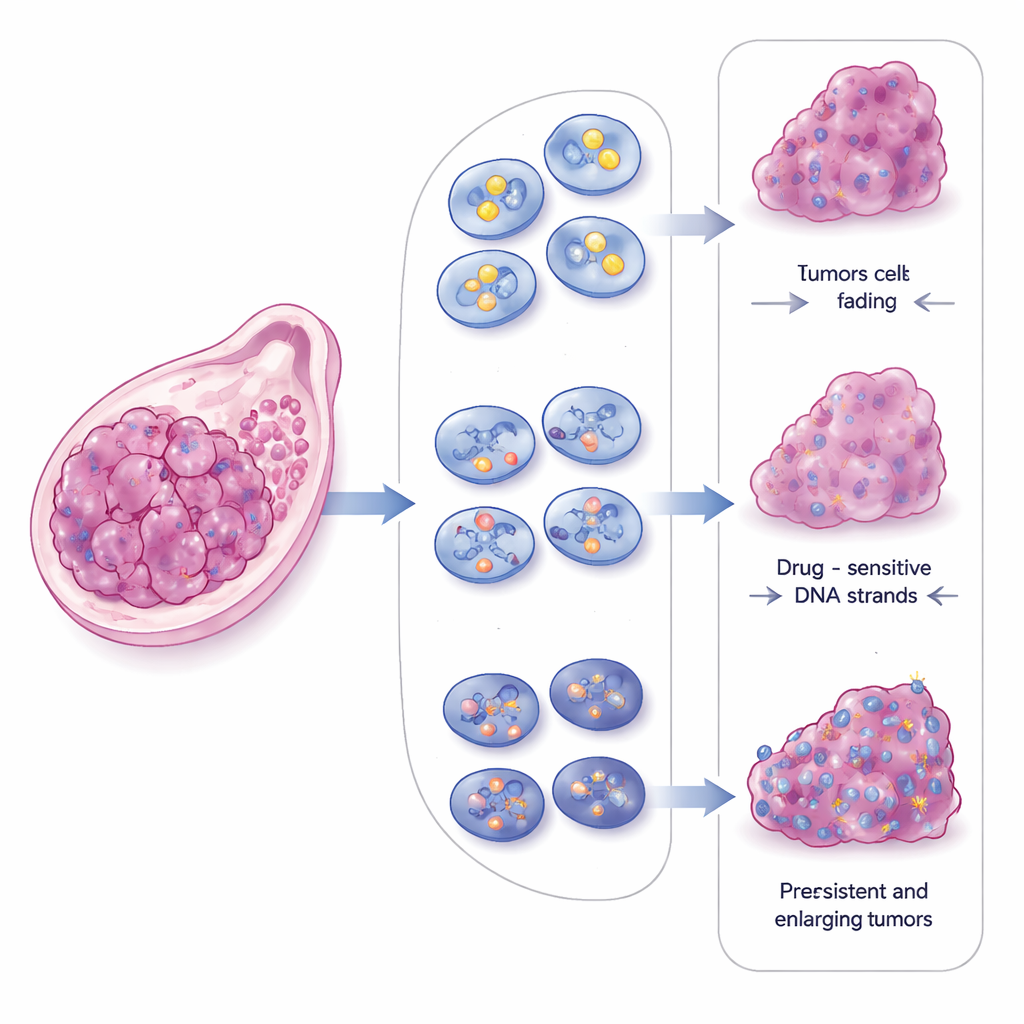
CBX2 damlacıkları onarım ekibini nasıl düzenliyor
Daha derine inen ekip, CBX2 damlacıklarının varlığında veya yokluğunda hangi onarım proteinlerinin gerçekten DNA’ya bağlandığını inceledi. CBX2 damlacıklarının PARP1, 53BP1, BRCA1 ve RAD51 dahil olmak üzere hasar yanıtında kilit rol oynayan oyuncuları DNA’ya çekmeye yardımcı olduğunu buldular—bu proteinler bir kırığın nasıl onarılacağına karar verir ve onarımı gerçekleştirir. Canlı hücre görüntülemesi, iki tip CBX2 damlacığı gösterdi: hasarlı kromatinle dinamik olarak karışan hareketli, sıvı bir form ve karışmayan yoğun, katı‑benzeri bir form. Sadece hareketli damlacıklar DNA hasar odakları ve ana onarım proteinleri ile örtüşüyordu; bu da bu akışkan fazın onarım makinesini gerektiği yerde toplayan ve organize eden işlevsel iskelet gibi davrandığını düşündürüyor.
Mevcut bir ilaçla gücü zayıflığa çevirme
CBX2 damlacıkları tümör hücrelerini DNA onarımında özellikle iyi hale getirdiğinden, yazarlar bu artmış onarım kapasitesinin aleyhlerine kullanılabileceğini sordular. İşlevsel CBX2 damlacıklarına sahip veya olmayan hücrelerde bir bileşik kütüphanesi taradılar ve ağızdan alınan, belirli kan kanserleri için onaylı bir ilaç olan Ibrutinib’in, CBX2 kondensatlarına dayanan hücrelere karşı özellikle toksik olduğunu keşfettiler. Ibrutinib damlacıkların oluşmasını engellemedi, fakat bu hücrelerin dayandığı yüksek doğruluklu onarım yolunu selektif olarak zayıflattı. Hayvan modellerinde, CBX2 damlacıkları içeren tümörler Ibrutinib tedavisinde küçüldü ve hastalardan alınan yüksek CBX2 düzeyli tümörlerden yetiştirilen üç boyutlu organoidler ilaca düşük düzeyli olanlara göre daha duyarlıydı. 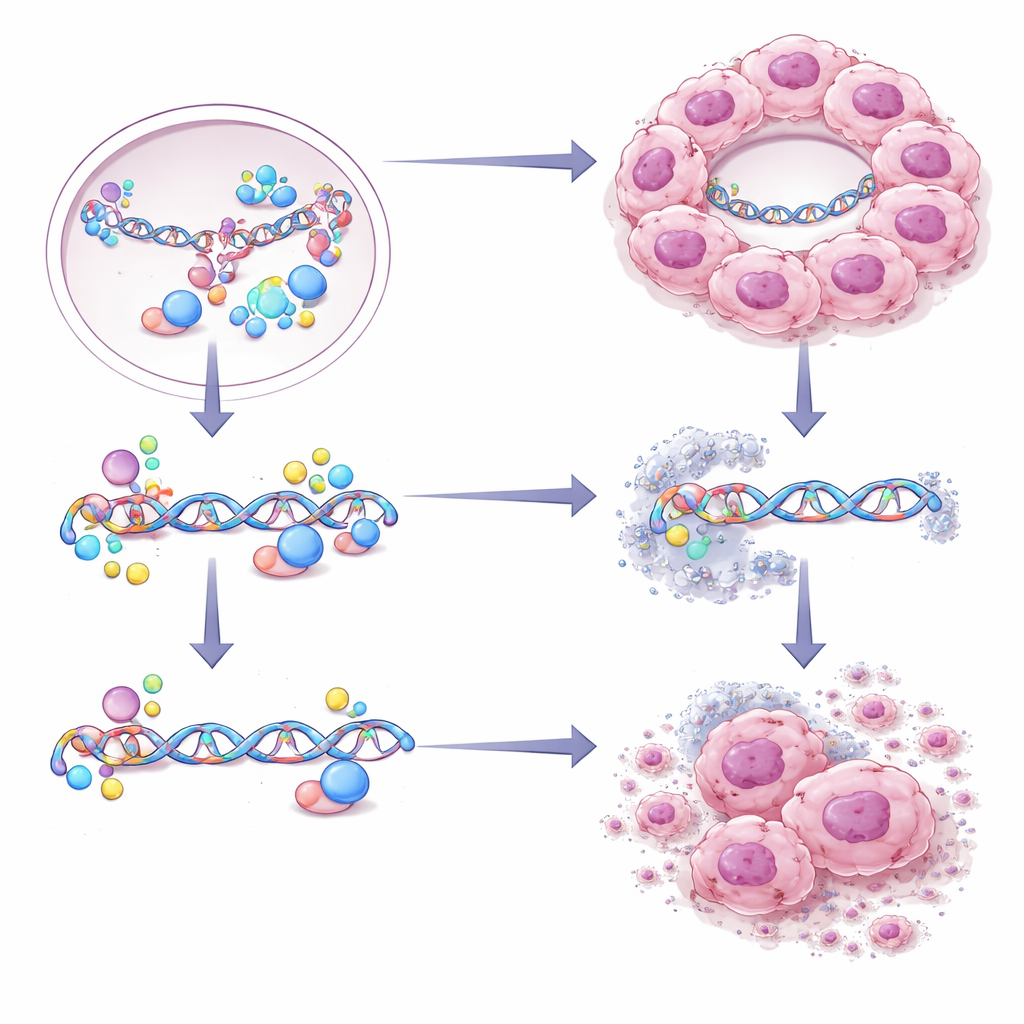
Bu hastalar için ne anlama gelebilir
Hastalar için çalışma iki önemli fikri öne sürüyor. Birincisi, tümör dokusundaki CBX2 damlacıklarının varlığı ve desenleri birinin platin kemoterapisi ve PARP inhibitörlerine nasıl yanıt vereceğini tahmin etmeye yardımcı olabilir: CBX2 içermeyen tümörlere sahip hastalar en iyi sonucu alırken, yaygın CBX2’ye sahip olanlar ortada, belirgin CBX2 kondensatlarına sahip olanlar ise en kötü sonuçları alıyor. İkincisi, aynı damlacık deseni Ibrutinib’ten fayda görebilecek hastaları işaretleyebilir; böylece bir kanser ilacının zor tedavi edilen bir over kanseri alt tipine yeniden yönlendirilmesi mümkündür. Özetle, çalışma tümör DNA’sını koruyan yapıların aynı zamanda yeni bir Aşil topuğunu açığa çıkarabileceğini gösteriyor—bu da daha kişiselleştirilmiş ve etkili tedavilere giden potansiyel bir yol sunuyor.
Atıf: Sun, S., Huang, L., Ma, Y. et al. CBX2 phase-separation contributes to homologous recombination repair and drug resistance in ovarian cancer. Cell Death Dis 17, 366 (2026). https://doi.org/10.1038/s41419-026-08605-4
Anahtar kelimeler: over kanseri, ilaç direnci, DNA onarımı, faz ayrışması, Ibrutinib