Clear Sky Science · tr
Prostat kanseri hücrelerinden makrofajlara STAT1 ile güçlendirilen bir geri bildirim mekanizması, tümör ilerlemesini ve radyoterapiye direnci düzenler
Bu araştırma neden önemli
Radyoterapi prostat kanserinin temel tedavilerinden biridir, ancak birçok tümör zamanla yanıt vermeyi keser ve hastalıkın nüks etmesine veya yayılmasına izin verir. Bu çalışma, tümörlerin radyasyondan korunmasına yardımcı olan, prostat kanseri hücreleri ile yakındaki bağışıklık hücreleri olan makrofajlar arasında gizli bir kimyasal “konuşmayı” ortaya koyuyor. Araştırmacılar bu döngüyü çözümlerek, ileri düzey prostat kanseri olan erkeklerde radyoterapinin etkinliğini artırabilecek yeni ilaç hedeflerini vurguluyor.
Şekeri farklı yakıp kullanan kanser hücreleri
Prostat kanseri hücreleri, birçok tümörde olduğu gibi, aerobin glikoliz olarak bilinen değiştirilmiş bir şeker yakımına dayanır. Şekeri oksijenle tamamen parçalamak yerine, daha hızlı ama daha az verimli bir yolu seçer ve büyük miktarda laktik asit üretirler. Araştırma ekibi tümör hücreleri içindeki STAT1 adlı bir proteini, bu şeker aç gözlü durumunu açan anahtar bir anahtar olarak tanımladı. STAT1, glikolizi yönlendiren üç ana enzimin aktivitesini artırarak hem şeker alımını hem de laktik asit üretimini yükseltiyor. Hücre kültürlerinde ve fare modellerinde STAT1 düzeyi yüksek olan tümörler daha hızlı büyüdü ve radyasyona daha dirençliydi; oysa glikolizin engellenmesi bu saldırgan özellikleri azaltıyordu. 
Tümör atıklarının bağışıklık hücrelerini nasıl yeniden şekillendirdiği
Laktik asit genellikle metabolik “atık” olarak düşünülür, ancak tümör çevresinde bir sinyal görevi görür. Araştırmacılar, prostat kanseri hücreleri tarafından salınan laktik asidin MCT1 adlı bir membran taşıyıcısı aracılığıyla makrofajlar tarafından alındığını gösterdi. Hücre içine girdikten sonra bu asit NFκB olarak bilinen içsel bir alarm sistemini aktive ediyor ve makrofajları M2 adı verilen yardımcı bir duruma itiyor. M2 makrofajlar kansere saldırmak yerine bağışıklık yanıtlarını yatıştırma ve örneğin damar oluşumunu teşvik etme gibi tümörü destekleyici işlevler sergileme eğilimindedir. Bilim insanları kanser hücrelerinde glikolizi engellediklerinde, laktik asit üretimini baskıladıklarında ya da laktik asidin makrofajlara girişini durdurduklarında bu bağışıklık hücreleri tümörü destekleyen M2 durumundan uzaklaşıp daha savunmacı bir profile kaydı.
Makrofajlar tümörlere geri büyüme sinyalleri gönderir
Hikâye makrofajların sadece karakter değiştirmesiyle bitmiyor. Laktik asit NFκB’yi aktive ettikten sonra makrofajlar güçlü bir haberci molekül olan MCP-1’i üretip salgılamaya başlıyor. Bu molekül prostat kanseri hücrelerine geri difüze oluyor ve yüzeydeki CCR2 adlı bir reseptöre bağlanıyor. Bu bağlanma kanser hücrelerinde JAK proteinlerini ve STAT1’i içeren başka bir içsel yolun devreye girmesine neden oluyor. Başka bir deyişle, fazladan şeker yakımını ilk başlatan aynı STAT1, sonunda kendi üretilmesine yol açan laktik aside izlenen bir sinyal tarafından yeniden etkinleştiriliyor. Araştırmacılar MCP-1’i prostat kanseri hücrelerine eklediklerinde glikoliz arttı, hücreler daha hızlı büyüdü ve hareket etti, ayrıca radyasyon kaynaklı DNA hasarını daha etkin onardılar. CCR2 veya JAK’in engellenmesi bu etkileri önledi.
Kendi kendini güçlendiren bir hayatta kalma döngüsü
Bir araya getirildiğinde sonuçlar, kanser hücreleri ile makrofajlar arasında kendi kendini güçlendiren bir döngüyü ortaya koyuyor. Prostat kanseri hücreleri içindeki STAT1 şeker parçalanmasını ve laktik asit salımını artırıyor. Bu laktik asit makrofajlara alınıyor, burada NFκB’yi aktive edip onları tümörü destekleyen M2 durumuna itiyor ve MCP-1 üretimini tetikliyor. MCP-1 sonra kanser hücrelerine geri gidip CCR2 ve JAK/STAT1 yolunu aktifleştiriyor, böylece glikolizi ve radyoterapi direncini daha da güçlendiriyor. Hayvan deneyleri, özellikle radyasyonla birlikte kullanıldığında CCR2 veya JAK’i engelleyen ilaçların tümör büyümesini yavaşlattığını ve M2 makrofajlarının varlığını azalttığını göstererek bu devreyi hedeflemenin klinik vaatini destekliyor. 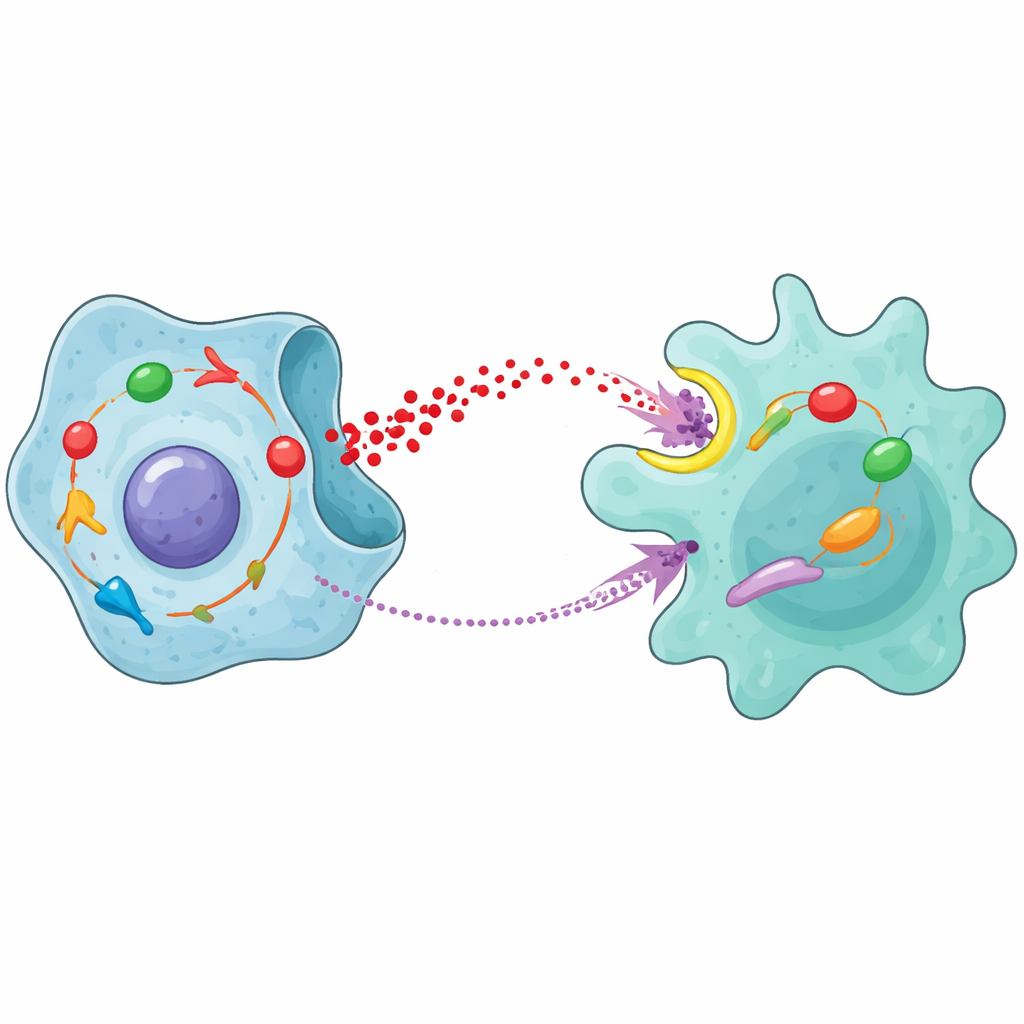
Bu hastalar için ne anlama geliyor
Hastalar için temel fikir, prostat tümörleri ile belirli bağışıklık hücrelerinin kemoterapötik bir ortaklık kurarak kanserin radyasyon tedavisine dayanmasına yardımcı olduğudur. Tümör hücreleri şekeri kullanma biçimlerini değiştirir, çevredeki makrofajları düşman yerine müttefik haline getiren laktik asit üretir. Bu yeniden programlanmış hücreler de tümörleri daha sağlam ve öldürülmesi zor hale getiren sinyaller gönderir. Bu döngüyü—laktik asit işlenmesi, MCP-1 sinyali veya JAK/STAT1 yolunun düzeyinde—keserek gelecekteki tedaviler tümörün savunmasını zayıflatabilir ve radyoterapinin daha iyi çalışmasına izin verebilir; bu da zor tedavi edilen prostat kanseri olan erkekler için yeni umutlar sunar.
Atıf: Chen, JY., Xue, YT., Lin, B. et al. A feedback mechanism from prostate cancer cells to macrophages, reinforced by STAT1, regulates tumor progression and resistance to radiotherapy. Cell Death Dis 17, 282 (2026). https://doi.org/10.1038/s41419-026-08577-5
Anahtar kelimeler: prostat kanseri, radyoterapi direnci, tümör mikroçevresi, makrofajlar, laktat metabolizması