Clear Sky Science · tr
Yeni biguanid 4C tarafından EGFR’nin baskılanması, BRCA2 ve Rad51’in aşağı düzenlenmesi yoluyla over kanserini PARP inhibitörlerine duyarlı hâle getirdi
Bu araştırma neden önemli
Yumurtalık kanseri teşhisi konan birçok kişi için, günümüzdeki hedefe yönelik ilaçlar yalnızca tümörlerinde belirli genetik kusurlar bulunan küçük bir azınlıkta etkili oluyor. Bu çalışma, PARP inhibitörleri olarak bilinen önemli bir ilaç sınıfının yararlarını, bu mutasyonlardan yoksun olan çok daha geniş hasta grubuna genişletme yolunu araştırıyor. Araştırmacılar, deneysel yeni bir bileşiği mevcut ilaçlarla eşleştirerek kanser hücrelerini sağlıklı dokuyu korurken öldürücü bir çıkmaza sürüklemeye yönelik bir strateji gösteriyorlar.
Mevcut yumurtalık kanseri tedavisindeki bir engel
Yumurtalık kanseri sıklıkla geç evrede tespit edilir ve kadınları etkileyen en ölümcül kanserlerden biri olmaya devam eder. Olaparib gibi PARP inhibitörleri gerçekten çarpıcı etki gösterebilir, ancak özellikle BRCA1 ve BRCA2 genleriyle bağlantılı bir DNA onarım yolunda kusuru olan hastalarda etkilidir. Bununla birlikte, çoğu tümör hâlâ sağlam bir onarım mekanizmasına sahiptir ve bu ilaçların neden olduğu DNA hasarını düzeltebilir; bu sayede kanser hücreleri hayatta kalır. Bu onarım ekibinin kilit parçaları arasında, homolog rekombinasyon adı verilen bir süreçle kırık DNA dizilerini onarmaya yardımcı olan BRCA2 ve Rad51 proteinleri bulunur. Kanser hücrelerinde bu onarım yolunu seçici olarak zayıflatmanın yollarını bulmak, PARP inhibitörlerini çok daha fazla hasta için faydalı hâle getirebilir.
İyi bilinen bir büyüme anahtarının rolü
Araştırma ekibi, birçok tümör hücresinin yüzeyinde bulunan ve büyümelerini tetikleyen epidermal büyüme faktörü reseptörü (EGFR) adlı, kanserle ilişkili tanıdık bir moleküle odaklandı. EGFR’nin yalnızca büyüme sinyalleri göndermekten fazlasını yaptığı bulundu: normal BRCA genlerine sahip over kanseri hücrelerinde yüksek EGFR düzeyleri kötü hasta sağkalımı ve PARP inhibitörlerine direnç ile ilişkiliydi. Hücre kültürlerinde ve fare modellerinde EGFR azaltıldığında veya kapatıldığında tümörler olaparibe çok daha duyarlı hale geldi. Araştırmacılar, EGFR’nin DNA hasarından sonra BRCA2 ve Rad51’in hücre çekirdeğine taşınmasına yardımcı olduğunu gösterdiler; böylece bu proteinler kırıkları onarıp tedavinin etkisini azaltabiliyor. EGFR’nin enzimatik aktivitesini basitçe engellemek yeterli değildi; bu onarım yolunu anlamlı biçimde bozmak için EGFR protein miktarının azaltılması gerekiyordu.
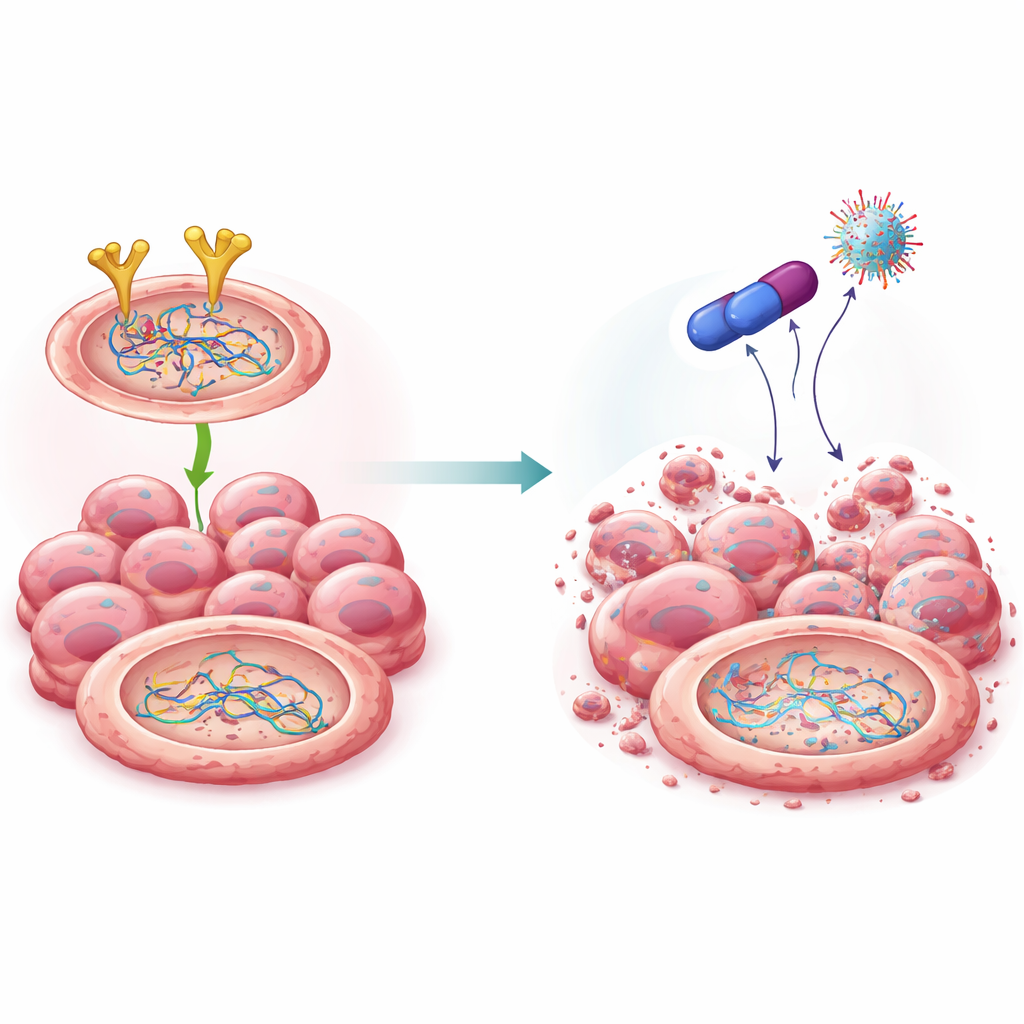
Onarım ekibini etkisizleştiren yeni bir bileşik
Biguanidler olarak bilinen bir ilaç ailesiyle yapılan önceki çalışmaya dayanarak, bilim insanları birkaç kimyasal akraba sentezledi ve öne çıkan bir molekül olan 4C’yi tanımladılar. Bu bileşik over kanseri hücreleri için güçlü bir toksisite gösterirken normal hücreler üzerinde nispeten daha nazikti. Bilgisayar modellemeleri ve laboratuvar testleri, 4C’nin doğrudan EGFR’ye bağlandığını ve onu hücrenin proteinleri parçalayma mekanizmasında yok edilmek üzere işaretlediğini gösterdi. Bazı mevcut EGFR ilaçlarının aksine, 4C yalnızca aktivitesini susturmak yerine EGFR’nin toplam miktarını azalttı. EGFR düzeyleri düştükçe BRCA2 ve Rad51’in stabilitesi de azaldı: bunlar yok edilmek üzere işaretlendi, parçalandı ve artık etkili DNA onarımını destekleyemedi. Önemli olarak, bu budama altta yatan genleri değiştirmeden protein düzeyinde gerçekleşti.
Hücre içindeki bir kurtarma yolunu bloke etmek
Çalışma, DNA hasarını tümör hayatta kalmasına bağlayan daha ayrıntılı bir olay zincirini ortaya koydu. PARP inhibitörleri DNA’ya zarar verdikten sonra, ATM adlı başka bir sensör proteini çekirdekten hücre gövdesine bir mesaj gönderiyor. Buna karşılık, EGFR BRCA2 ve Rad51 ile iş birliği yapıyor ve onların hasardan sonra çekirdeğe taşınmasına yardımcı oluyor; orada hasarı onarıyorlar. Araştırmacılar, c-Cbl adlı üçüncü bir proteinin normalde BRCA2 ve Rad51 için bir tür yok etme etiketi görevi gördüğünü keşfettiler. EGFR, bu onarım proteinlerine erişimde c-Cbl ile rekabet ederek onların yıkım için işaretlenmelerine karşı koruma sağlıyor. 4C EGFR düzeylerini düşürdüğünde, c-Cbl BRCA2 ve Rad51’e daha kolay bağlanabiliyor; bu da onların işaretlenmesine, parçalanmasına ve kaybına yol açıyor. Çekirdekte daha az onarım proteini olduğunda DNA yaraları birikir ve kanser hücreleri PARP inhibitörlerine karşı çok daha hassas hâle gelir.
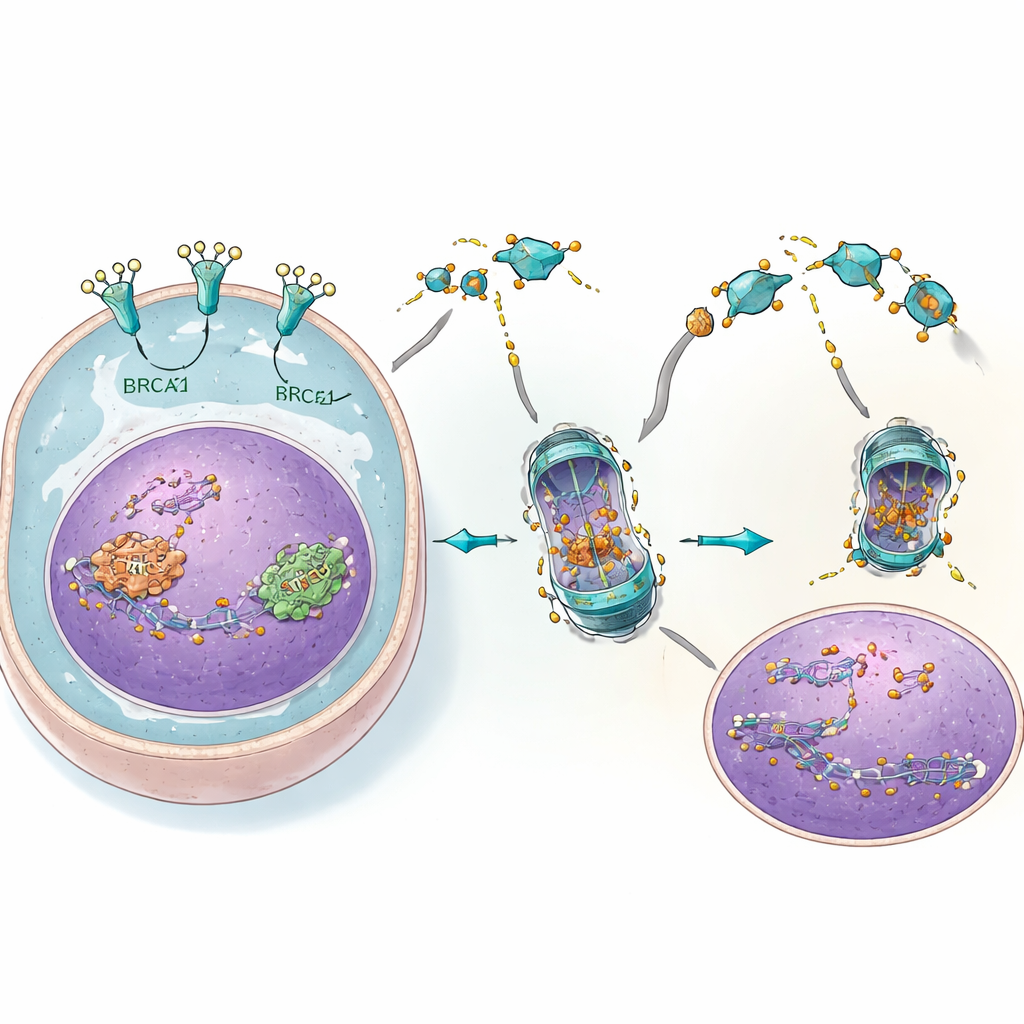
Hücrelerden hayvanlara: güçlü bir eşleştirme
Hem kültürdeki hücrelerde hem de fare modellerinde, 4C’nin PARP inhibitörleriyle birleştirilmesi güçlü bir çift darbe üretti. Tek başına her iki ilaca da direnç gösteren normal BRCA genli tümörler, her iki ilaç birlikte uygulandığında dramatik şekilde küçüldü veya büyümeyi durdurdu. DNA hasarı belirteçleri keskin biçimde arttı; bu, onarımın aşırı yüklendiği fikriyle tutarlı. Aynı zamanda, karaciğer ve böbrekler gibi normal hücreler ve önemli organlar zarar görmüş olduğuna dair çok az iz gösterdi; muhtemelen bunun nedeni onların çok daha düşük EGFR düzeylerine sahip olması ve bu belirli onarım kestirme yoluna daha az güvenmeleriydi. Kombinasyonun yararları, yumurtalık kanseri hücrelerinin vücutta yayılmasının azalmasını da kapsıyordu.
Bu hastalar için ne anlama gelebilir
Bu çalışma, bir kanser hücresinin gücünü zayıflığa çevirmenin bir yolunu öneriyor. Araştırmacılar 4C adlı yeni bileşikle EGFR’yi hedefleyerek BRCA2 ve Rad51’in sağladığı korumayı ortadan kaldırıyor; böylece onarımları normal olan tümörler, PARP inhibitörlerine karşı BRCA mutasyonu taşıyan kanserler gibi davranıyor. Bu zorunlu savunmasızlık, "sentetik letalite" olarak bilinir, mevcut ilaçların kapsamını daha fazla yumurtalık kanseri hastasına genişletebilir ve yan etkileri yönetilebilir tutabilir. 4C hâlâ deneysel aşamada olup daha gelişmiş modellerde ve klinik çalışmalarda kapsamlı testlere ihtiyaç duyacaktır; ancak çalışma, tümör hücrelerindeki belirli onarım yardımcılarını dağıtmanın tedavi sonuçlarını nasıl iyileştirebileceğine dair açık bir yol haritası sunuyor.
Atıf: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Anahtar kelimeler: yumurtalık kanseri, PARP inhibitörleri, EGFR, DNA onarımı, hedefe yönelik tedavi