Clear Sky Science · tr
YAP1’in O-GlcNAcileştirilmesi, HIF1α transkripsiyon faktörüne bağlanarak otofaji ve mitofajiyi aktive etmek yoluyla akciğer naklinde iskemik-reperfüzyon hasarını artırır
Akciğer nakli hastaları için bunun önemi nedir
Akciğer nakli, ileri akciğer hastalığı olanlara ikinci bir yaşam şansı verebilir; ancak yeni nakledilen akciğer sıklıkla kan akımı kesilip sonra yeniden sağlandığında bir hasar dalgasına maruz kalır. Bu sözde iskemik–reperfüzyon hasarı, hastaları hassas akciğerlerle, yoğun bakımda uzun kalışlarla ve daha kötü uzun vadeli sonuçlarla karşı karşıya bırakabilir. Bu makalenin temelini oluşturan çalışma, bu erken hasarı tetikleyen akciğer hücreleri içinde gizli bir moleküler zincir reaksiyonunu ortaya koyuyor ve bir gün akciğer nakillerini daha güvenli ve başarılı hale getirebilecek yeni ilaç hedeflerine işaret ediyor.
Kaybolan oksijenle tetiklenen zincir reaksiyon
Nakil sırasında verici akciğer geçici olarak kan ve oksijenden yoksun bırakılır, sonra alıcının dolaşımına bağlandığında aniden yeniden oksijenle buluşur. Araştırmacılar bu dur-kalk oksijen tedarikini laboratuvarda akciğer ve damar iç yüzünü döşeyen hücrelerde ve sıçan akciğer nakli modelinde modellediler. Bu stresin, hücrelerin içindeki büyüme ve hayatta kalma kontrol sistemi olan Hippo–YAP yolunu güçlü biçimde etkinleştirdiğini gördüler. Etkinleştiğinde YAP1 proteini çekirdeğe girer ve birçok geni açıp kapatmak için diğer faktörlerle iş birliği yapar. Bu çalışmada, hipoksiyi takiben reoksijenasyon YAP1 ve onun partner genlerini çok daha aktif hale getirdi ve bu artış hücre ölümü ile nakledilen akciğeri iltihaplandırıp zayıflatabilecek inflamatuar moleküllerin salınımı ile sıkı ilişkiliydi.
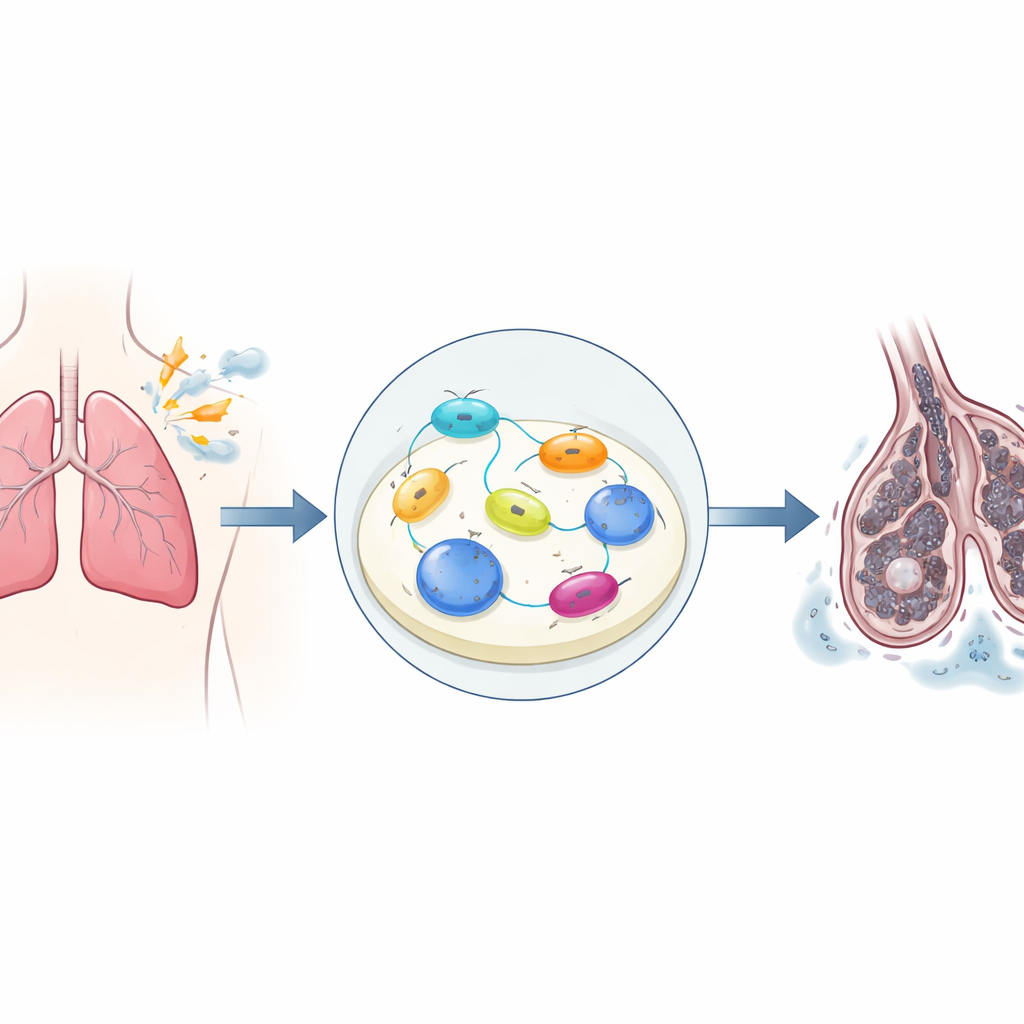
Aşırıya kaçan kendi-kendini temizleme
Hücreler, aşınmış bileşenleri parçalamak ve geri dönüştürmek için otofaji adı verilen içsel bir “kendi-kendini temizleme” sistemine ve hasarlı mitokondrileri seçici olarak uzaklaştıran daha odaklı bir sürece, mitofajiye güvenirler. Orta düzeyde bu süreçler hücrelerin strese uyum sağlamasına yardımcı olur. Ancak ekip, oksijen kesilip yeniden sağlandıktan sonra hem otofaji hem de mitofajinin akciğer hücrelerinde ve nakledilen akciğerlerde keskin şekilde arttığını buldu. Mikroskopta daha fazla geri dönüşüm vezikülü ve mitokondrilerin yutulup sindirildiğine dair işaretler görüldü. Aynı zamanda hayvanlarda akciğer dokusunda şişme ve yapısal hasar ile programlı hücre ölümünde artış görüldü. Bu, nakil ortamında kendi-kendini temizleme mekanizmasının aşırı hızlanıp korumadan ziyade hasara katkıda bulunmaya başladığını düşündürdü.
Proteinin davranışını değiştiren bir şeker etiketi
Bilim insanları daha sonra YAP1’in bu koşullar altında neden bu kadar zararlı hale geldiğini sordular. Birçok proteine eklenebilen ve bunların davranışını değiştirebilen O-GlcNAc adlı küçük şeker bazlı etikete odaklandılar. Bu etiketi ekleyen enzim OGT’dir. Oksijen yoksunluğu ve yeniden sağlanmasının hücrelerde hem genel O-GlcNAc etiketlenmesini hem de daha spesifik olarak YAP1’in etiketlenmesini artırdığını keşfettiler. YAP1 bu şeker etiketini taşıdığında, normalde düşük oksijene uyum sağlamak için koruyucu genleri açan diğer önemli oksijen algılayıcı protein HIF1α’ya daha sıkı bağlandı. Biyokimyasal testlerle, etiketli YAP1’in HIF1α’yı otofaji ve mitofajiyi yöneten genleri kontrol eden DNA bölgelerine çektiğini, bunların aktivitesini artırdığını ve hücrenin geri dönüşüm ile stres yanıtlarını daha da güçlendirdiğini gösterdiler.
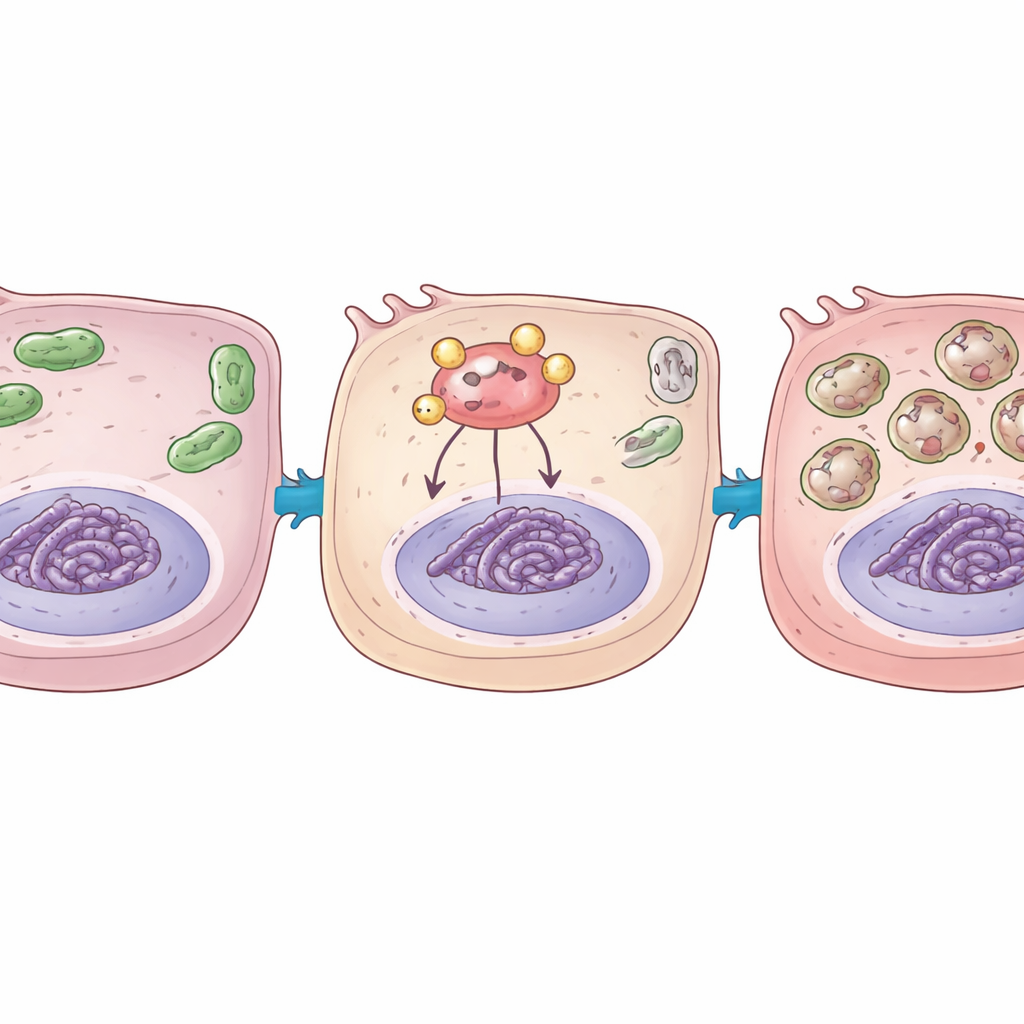
Zararlı döngüyü kapatmak
Bu yolun dizginlenip dizginlenemeyeceğini test etmek için araştırmacılar genetik araçlar kullanarak ya YAP1’i ya da şeker etiketini ekleyen enzim OGT’yi azaltmayı denediler. Hücre modellerinde YAP1’in azaltılması stres yolunun etkinleşmesini zayıflatmış, aşırı otofaji ve mitofajiyi kesmiş ve oksijen yeniden sağlandıktan sonra hücre ölümünü azaltmıştı. Nakledilmiş sıçan akciğerlerinde YAP1 veya OGT’nin baskılanması doku şişmesini azalttı, kendi-yeme ve mitokondri parçalanması belirteçlerini düşürdü ve programlı hücre ölümü geçiren hücre sayısını azalttı. Önemli olarak, OGT’nin engellenmesi YAP1’in şeker etiketlenmesini ve HIF1α’yı otofaji ile ilgili genlere çekme yeteneğini de azalttı; bu da ekibin ortaya çıkardığı zararlı döngüyü doğrudan zayıflattı.
Gelecek nakiller için bunun anlamı
Bir araya getirildiğinde, çalışma YAP1 proteini üzerindeki küçük bir kimyasal etiketin normal bir stres yanıtı ağını nakilden sonra akciğer hasarına yol açan bir sürücüye dönüştürebileceğini gösteriyor. YAP1’in oksijen sensörü HIF1α’ya yapışmasına yardım ederek ve hücresel kendi-yemesini sağlıklı düzeylerin ötesine çıkararak bu etiket yeni akciğerde şişme, yapısal hasar ve hücre kaybını teşvik ediyor. Bulgular, YAP1 aktivitesini azaltmayı, OGT tarafından yapılan şeker etiketlenmesini engellemeyi veya otofaji ile mitofajiyi dikkatli şekilde düzenlemeyi amaçlayan ilaçların, nakledilen akciğerleri erken hasardan korumak için yeni yollar sunabileceğini; böylece alıcıların hem sağkalımını hem de yaşam kalitesini iyileştirebileceğini öne sürüyor.
Atıf: Dai, S., Wan, X., Xia, L. et al. O-GlcNAcylation of YAP1 promotes lung transplant ischemia-reperfusion injury via binding to HIF1α transcription factor and activating autophagy and mitophagy. Cell Death Dis 17, 311 (2026). https://doi.org/10.1038/s41419-026-08548-w
Anahtar kelimeler: akciğer nakli, iskemi reperfüzyon hasarı, YAP1, otofaji, mitofaji