Clear Sky Science · tr
Uzun kodlamayan RNA ADEI/miR-93-3p/STAT3 ekseni, PD-1/PD-L1 kontrol noktasını düzenleyerek Epstein–Barr virüs pozitif diffüz büyük B hücreli lenfoma ilerlemesini ve bağışıklıktan kaçışı teşvik eder
Bağışıklık savunmalarımız için neden önemli
Yaygın Epstein–Barr virüsü (EBV) ile ilişkili bazı lenfomalar alışılmadık derecede zor tedavi edilir ve sıklıkla vücudun bağışıklık savunmasından kaçabilir. Bu çalışma, bu kanserlerin içinde gizli bir haberleşme sistemi ortaya koyuyor: tümörlerin büyümesine ve bağışıklıktan saklanmasına yardımcı olan uzun bir RNA molekülünü taşıyan küçük kesecikler olan ekzosomlar. Bu gizli iletişimin anlaşılması, bu inatçı kan kanserlerini teşhis etme ve tedavi etme konusunda yeni yollar açabilir.
Dengeyi bozan bir virüs
Diffüz büyük B hücreli lenfoma (DLBCL) en yaygın agresif lenfomadır. Tümör hücrelerinde EBV bulunduğunda, hastalar standart kemoterapi‑immünoterapiye genellikle daha kötü yanıt verir. Araştırmacılar önce laboratuvarda EBV pozitif ve EBV negatif lenfoma hücrelerini karşılaştırdı. EBV enfeksiyonunun lenfoma hücrelerinin daha hızlı bölünmesine, daha fazla kolon oluşturmasına ve farelerde daha büyük tümörler oluşturmasına neden olduğunu buldular. EBV pozitif hücreler ayrıca PD‑1 ile etkileşen ve saldırıyı kapatan bir yüzey molekülü olan PD‑L1’i daha fazla gösteriyordu. Ekip, lenfoma hücrelerini katil CD8 T hücreleriyle karıştırdığında, EBV pozitif tümörler bu T hücrelerinin sayısını ve etkinliğini azalttı; bu etki, PD‑1/PD‑L1 frenini engelleyen antikorlarla geri döndürülebildi.
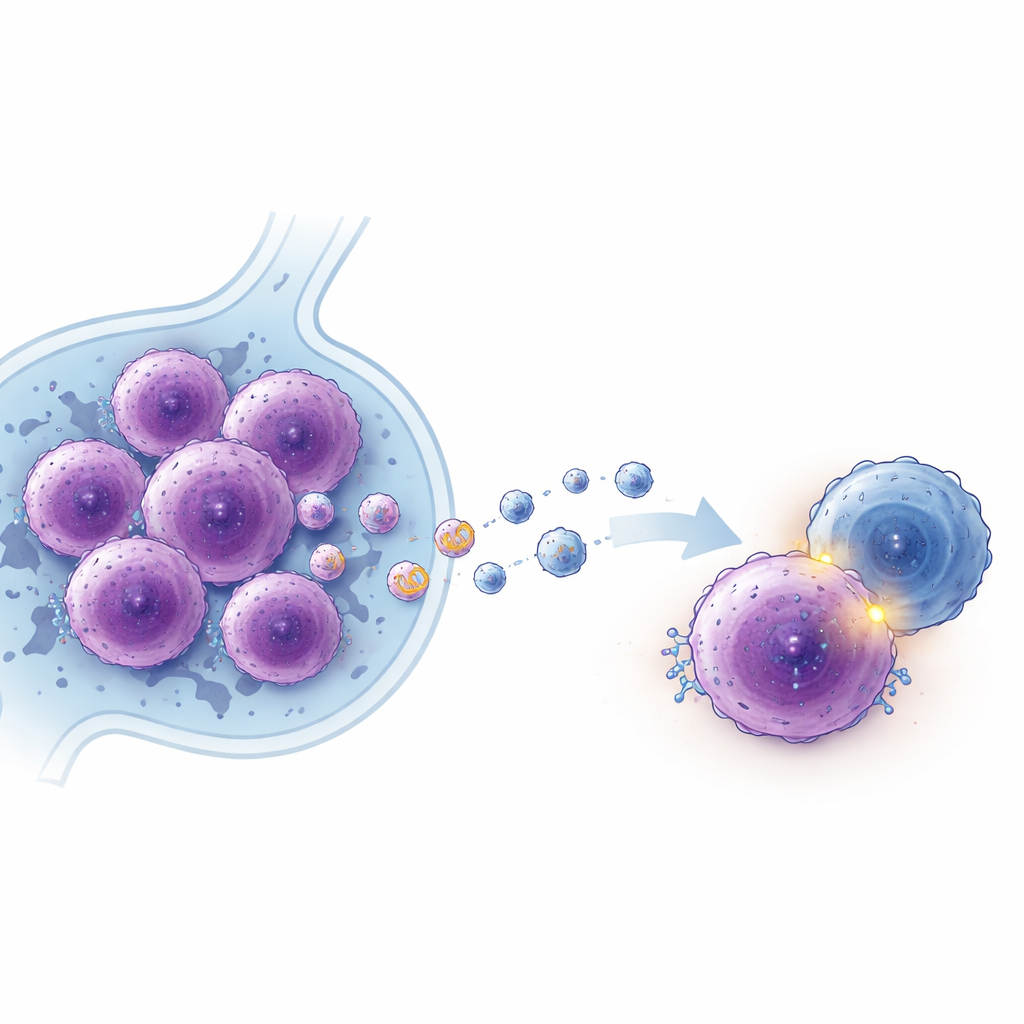
Tümörlerin büyümesine ve gizlenmesine yardımcı olan uzun bir RNA
EBV’nin tümör davranışını nasıl yeniden şekillendirdiğini anlamak için ekip, protein üretmeyen ancak birçok hücresel süreci düzenleyebilen uzun kodlamayan RNA’lara baktı. EBV pozitif ve EBV negatif DLBCL hücrelerinden salınan ekzosomların RNA içeriğini tarayarak, daha önce karakterize edilmemiş ve lncADEI adını verdikleri bir RNA’nın EBV pozitif hücrelerde ve onların ekzosomlarında güçlü biçimde arttığını keşfettiler. Lenfoma hücrelerini daha fazla lncADEI üretmeye zorladıklarında, hücreler daha hızlı çoğaldı, daha fazla koloni oluşturdu ve programlı hücre ölümüne (apoptoz) karşı direnç kazandı. lncADEI’yi azaltmak ise zıt etki gösterdi; hem kültürde hem de fare tümör modellerinde büyümeyi yavaşlattı ve hücre ölümünü artırdı.
lncADEI bağışıklıktan kaçışı nasıl yeniden kablolar
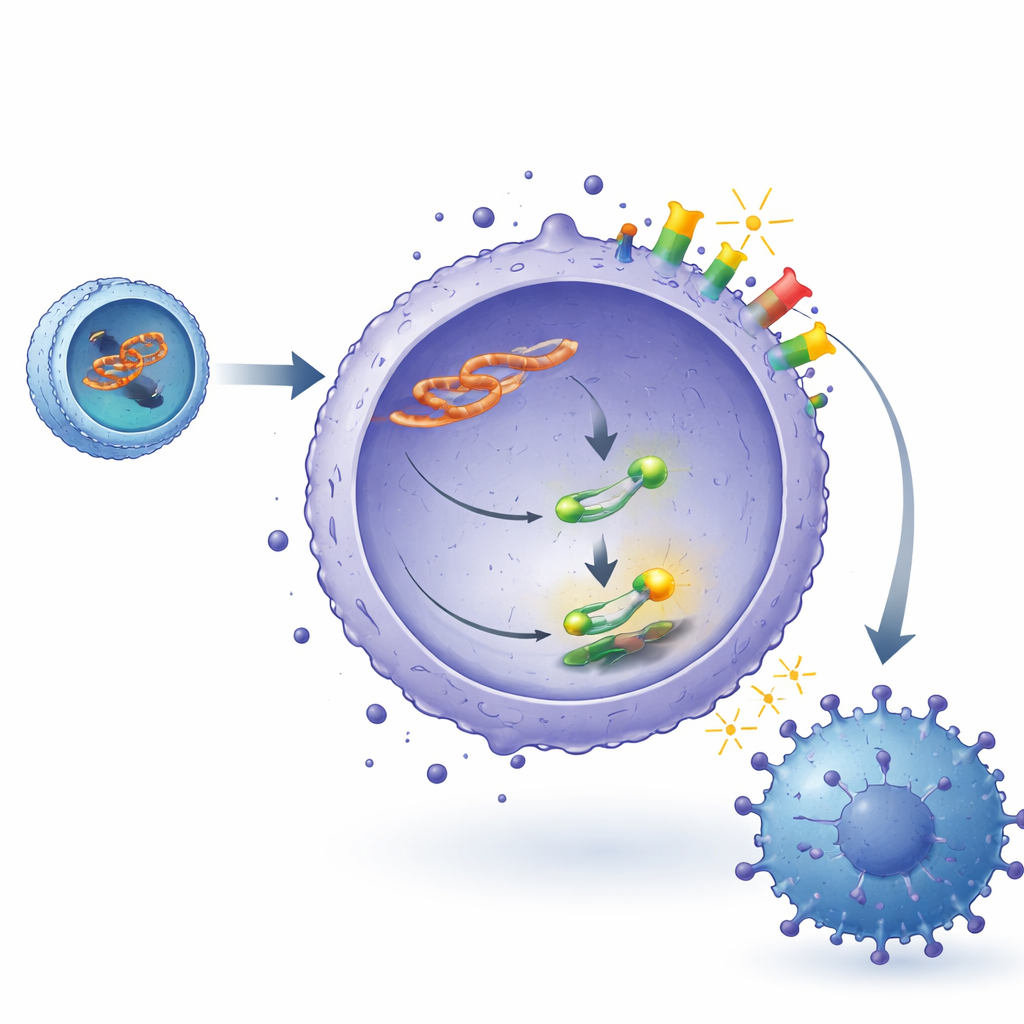
Araştırmacılar daha sonra lncADEI’nin PD‑1/PD‑L1 bağışıklık kontrol noktası ile nasıl bağlantı kurduğunu izlediler. Lenfoma hücrelerinin içinde lncADEI ağırlıklı olarak sitoplazmada bulunur ve burada miR‑93‑3p adlı küçük düzenleyici bir RNA için bir sünger gibi davranır. Normal koşullarda miR‑93‑3p, mesajına bağlanarak anahtar bir sinyal proteini olan STAT3’ün üretimini sınırlayarak STAT3’ü kontrol altında tutmaya yardımcı olur. lncADEI miR‑93‑3p’yi bağladığında, daha fazla STAT3 üretilir ve aktive olur. STAT3 ise doğrudan lenfoma hücrelerinde PD‑L1 geninin kontrol bölgesine bağlanır ve PD‑L1 üretimini artırır. Bu zincir—lncADEI’nin miR‑93‑3p’yi bloke etmesi, STAT3’ü serbest bırakması ve PD‑L1’i artırması—tümör hücrelerinde daha yüksek PD‑L1, CD8 T hücrelerine yönelik daha güçlü kapatma sinyalleri ve azalmış T hücre aktivitesi ile sonuçlanır.
Kötü talimatları yayan ekzosom “posta”sı
EBV pozitif lenfoma hücreleri lncADEI’yi kendilerine saklamaz. EBV negatif hücrelere göre çok daha fazla ekzosom salarlar ve bu ekzosomlar lncADEI ile doludur. EBV pozitif hücrelerin ekzosomlarına maruz kalan EBV negatif lenfoma hücreleri bunları alır, içlerindeki lncADEI seviyeleri yükselir ve daha agresif davranmaya—daha hızlı bölünmeye ve daha fazla koloni oluşturmaya—başlarlar. T hücrelerini içeren karışık kültürlerde, lncADEI ile zenginleştirilmiş ekzosomlar CD8 T hücrelerinin sayısını ve öldürme gücünü azalttı ve bu bağışıklık hücrelerinde PD‑1’i artırdı; bu da bağışık yanıtı daha da zayıflattı. Bu bulgu, EBV pozitif tümörlerin lncADEI‑ce zengin ekzosomlar aracılığıyla komşu tümör hücrelerini “eğitebildiğini” ve çevrelerini yeniden şekillendirebildiğini öne sürer.
Hasta kan örneklerinden ipuçları
Bu laboratuvar bulgularını gerçek hastalığa bağlamak için ekip, 47 DLBCL hastasının kan ekzosomlarında lncADEI’yi ölçtü. Tümörleri EBV pozitif olanların kan ekzosomlarındaki lncADEI düzeyleri, EBV negatif hastalara göre anlamlı biçimde daha yüksekti. Kandaki yüksek lncADEI ayrıca daha ileri hastalık evresi, daha agresif tümör alt tipi, daha yüksek standart risk skorları ve artmış doku hasarı belirteçleri ile ilişkilendirildi. Bu desenler, kandaki ekzosomal lncADEI’nin EBV kaynaklı lenfoma ve şiddetinin minimal invaziv bir göstergesi olarak kullanılabileceğini düşündürür.
Gelecekteki bakım için ne anlama geliyor
Günlük ifadeyle, bu çalışma EBV bağlantılı lenfomaların kullandığı üç adımlı bir numarayı ortaya koyuyor: uzun bir RNA (lncADEI) aşırı üretilir, gezici keseciklere paketlenir ve hem tümör içinde hem de komşu hücrelerde iyi bilinen bir bağışıklık freni olan PD‑L1’i yükseltmek için kullanılır. Sonuç daha hızlı tümör büyümesi ve zayıflatılmış bir T hücre saldırısıdır. Zincirdeki her adım—lncADEI’nin kendisi, miR‑93‑3p ve STAT3 ile etkileşimi ve lncADEI‑ce zengin ekzosomların salınımı—müdahale veya ölçüm için olası bir nokta sunduğundan, çalışma immünoterapiyi iyileştirme ve EBV ilişkilendirilmiş lenfomaları basit bir kan testiyle izleme yönünde yeni stratejilere işaret etmektedir.
Atıf: Zheng, W., Lai, G., Liao, Z. et al. Long noncoding RNA ADEI/miR-93-3p/STAT3 axis promotes Epstein–Barr virus-positive diffuse large B-cell lymphoma progression and immune evasion through regulating the PD-1/PD-L1 checkpoint. Cell Death Dis 17, 280 (2026). https://doi.org/10.1038/s41419-026-08532-4
Anahtar kelimeler: Epstein–Barr virüs lenfoma, bağışıklık kontrol noktası, uzun kodlamayan RNA, ekzosomlar, STAT3 sinyalleşmesi