Clear Sky Science · tr
Deubiquitinaz UCH-L1, PKM2’yi stabilize ederek üçlü negatif meme kanserinde glikolizi artırır ve paklitaksel direncini sağlar
Bu araştırma hastalar için neden önemli
Kemoterapi, ortak ilaç hedefleri olmayan ve agresif seyreden üçlü negatif meme kanseri için hâlâ başlıca seçeneklerden biridir. Yine de birçok tümör sonunda paklitaksel gibi güçlü ilaçlara karşı direnç kazanır; böylece kanser geri dönebilir ve yayılabilir. Bu çalışma, kanser hücrelerinin şeker yakma biçimini yeniden düzenleyerek paklitakselle başa çıkmalarına yardım eden gizli bir devreyi açığa çıkarıyor ve gelecekteki tedavilerin kemoterapinin etkisini daha uzun süre korumasına yardımcı olabilecek yeni bir zayıf noktayı işaret ediyor.
Tedavisi zor bir meme kanseri
Üçlü negatif meme kanseri, sahip olmadığı özelliklerle tanımlanır: östrojen, progesteron veya birçok modern ilacın hedeflediği HER2 reseptörlerini taşımaz. Sonuç olarak standart kemoterapi ilaçları tedavinin temelini oluşturur. Paklitaksel dünyada yaygın olarak kullanılan bu ilaçlardan biridir. Ancak hastaların önemli bir kısmı ya başlangıçtan itibaren iyi yanıt vermez ya da zamanla direnç geliştirir; bu da tümörün nüks etmesine ve daha kötü sağkalıma yol açar. Klinik ortamda bu desen uzun süredir görülse de, hangi tümörlerin paklitakselle dirençli olacağını tahmin edebilecek açık belirteçler ve bu direnci yönlendiren moleküler anahtarlar eksikti.
Meme tümörlerinde ortaya çıkan bir sinir proteini
Araştırmacılar, sinir hücreleri ve beyin hastalıklarındaki rolüyle daha çok bilinen UCH‑L1 adlı proteine odaklandı. Kamuya açık kanser veri tabanlarını tarayıp üçlü negatif meme kanseri hastalarından alınan tümör örneklerini inceleyerek, UCH‑L1 düzeylerinin bu tümörlerde normal meme dokusuna göre çok daha yüksek olduğunu buldular. Tümörlerinde daha fazla UCH‑L1 bulunan hastalar genellikle daha kısa sağkalım gösteriyor ve özellikle paklitaksel veya benzeri ilaçlardan daha az yarar sağlıyordu. Laboratuvarda yetiştirilen kanser hücre hatlarında UCH‑L1’i artırmak hücreleri paklitaksele karşı daha zor öldürülebilir hale getirirken, UCH‑L1’i azaltmak ters etkiyi gösterdi; bu bulgular hem kültür kaplarında hem de fare tümör modellerinde doğrulandı. 
Kanser hücrelerinin şeker açlığı ve ilaç direnci
Kanser hücreleri sıklıkla şeker yakmanın hızlı ama verimsiz bir yolunu, yani aerobik glikoliz veya Warburg etkisini tercih eder. Bu hızlı şeker kullanımı hızlı enerji ve büyüme için yapı taşları sağlar ve birçok tedaviye dirençle ilişkilendirilmiştir. Araştırma ekibi UCH‑L1 olan ve olmayan kanser hücrelerini karşılaştırdığında bu metabolik davranışta belirgin değişiklikler gördü. Daha az UCH‑L1’e sahip hücreler daha az glukoz tüketti, daha az laktat üretti ve daha az hücresel enerji sağlarken; ekstra UCH‑L1 taşıyan hücreler bunun tersini ve glikolize bağlı daha güçlü bir asitlenme sinyali gösterdi. Önemli olarak, 2‑DG adlı bir bileşikle glikolizi engellediklerinde UCH‑L1’in paklitakselle koruyucu etkisi büyük ölçüde ortadan kalktı. Bu, UCH‑L1’in kanser hücrelerinin kemoterapiye direnmesine büyük ölçüde şeker yakma makinesini hızlandırarak yardımcı olduğunu gösterdi.
Tümör yakıtını koruyan bir protein ortaklığı
Daha derine indiklerinde, araştırmacılar hücre içindeki UCH‑L1’in doğrudan etkileşimde olduğu ortakları aradılar ve glikoliz yolunda kritik bir kavşakta yer alan anahtar bir enzim olan PKM2’ye odaklandılar. Normalde PKM2 düzeyleri, proteinleri yıkım için işaretleyen ubiquitin adlı hücresel geri dönüşüm etiketiyle kontrol edilir. UCH‑L1, ubiquitini çıkarabilen bir “etiket sökücü” enzimdir. Çalışma, UCH‑L1’in PKM2’nin kuyruk bölgesine fiziksel olarak bağlandığını ve PKM2’yi hücrenin bertaraf sistemine gönderen belirli bir ubiquitin zinciri türünü özel olarak kopardığını gösterdi. UCH‑L1, PKM2 üzerindeki belirli bir noktada bu zincirleri keserek onun yıkımını engelliyor ve enzimin stabilitesini artırıyor. Daha fazla PKM2 ile glikoliz daha yoğun çalışıyor, tümörü besliyor ve paklitaksel maruziyetinin yarattığı strese karşı dayanmasını sağlıyordu. 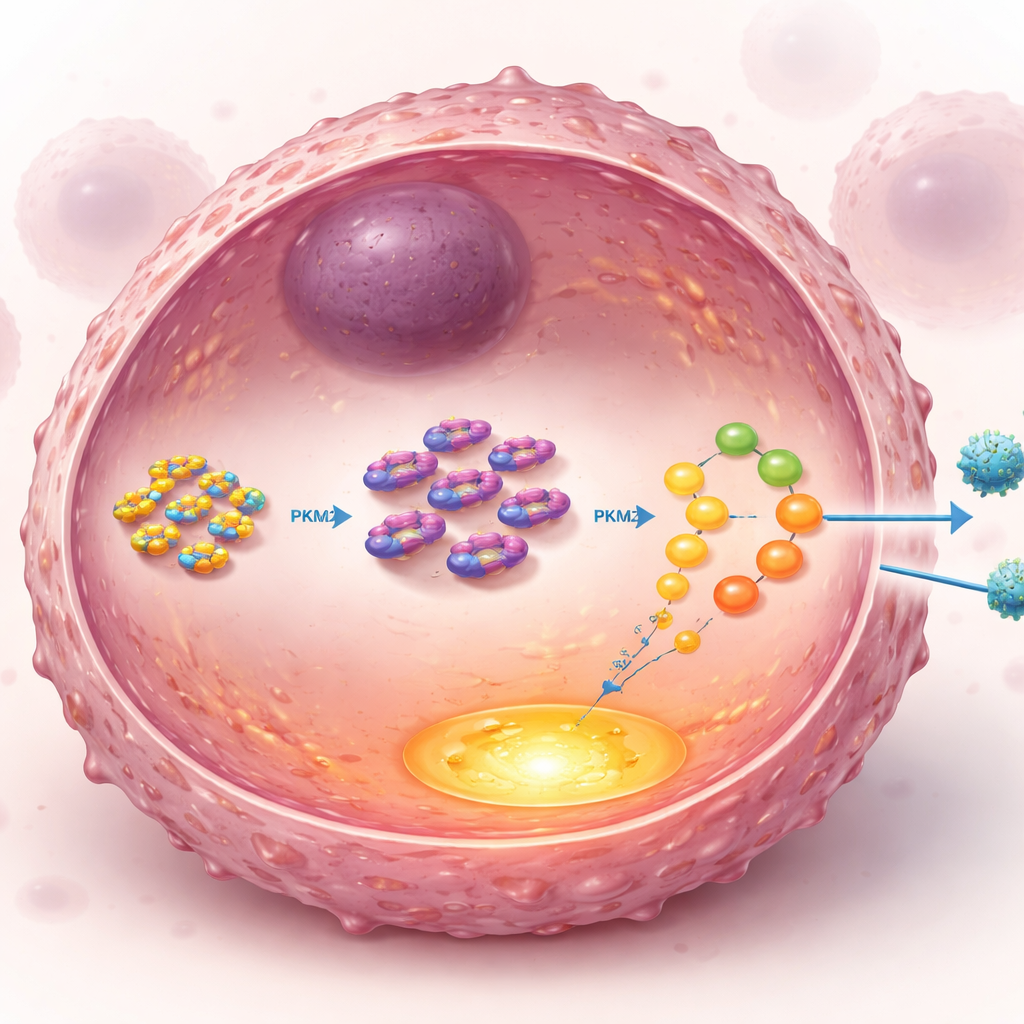
İnatçı tümörlerde direnci tersine çevirme
Araştırma ekibi daha sonra hasta kökenli veri setlerinden ve laboratuvar modellerinden alınan paklitaksel‑dirençli üçlü negatif meme kanseri hücrelerine yöneldi. Bu dirençli hücrelerde hem UCH‑L1 hem de PKM2 düzeyleri yükselmişti ve glikoliz artmıştı. UCH‑L1 veya PKM2’yi susturmak ya da kimyasal olarak glikolizi engellemek bu sertleşmiş hücreleri tekrar paklitaksele duyarlı hale getirdi, hücre ölümünü geri getirdi ve farelerde tümörleri küçülttü. UCH‑L1’den yoksun tümörlere PKM2’yi yeniden vermek bu faydanın büyük kısmını ortadan kaldırdı; bu da PKM2’nin bu direnç devresinin kilit aşağı akış oyuncusu olduğunu vurguladı. Hasta tümör örneklerinde UCH‑L1 ve PKM2 genellikle birlikte yüksek çıktı ve yüksek PKM2 kemoterapi sonrası daha kötü sonuçlarla da ilişkilendirildi.
Gelecek tedaviler için ne anlama geliyor
Uzman olmayanlar için sonuç şudur: bazı üçlü negatif meme kanserleri, UCH‑L1 ile PKM2 arasındaki ortaklık tarafından desteklenen bir şeker yakma motorunu devreye sokarak paklitakselden kurtuluyor. UCH‑L1, PKM2’nin parçalanmasını önleyen koruyucu bir mekaniker gibi davranarak kanser hücrelerinin daha fazla enerji üretmesine ve kemoterapinin yol açtığı hasara direnmesine izin veriyor. Tümörlerde UCH‑L1 veya PKM2 ölçümü, bir hastanın paklitaksele ne kadar iyi yanıt vereceğini öngörmeye yardımcı olabilir; UCH‑L1, PKM2 veya glikolizi engelleyen ilaçlar, bir gün standart kemoterapi ile birlikte kullanılarak direnci aşmak veya önlemek ve bu zorlu kansere sahip kişilerde sonuçları iyileştirmek için değerlendirilebilir.
Atıf: Chen, X., Zhou, X., Meng, Y. et al. Deubiquitinase UCH-L1 confers paclitaxel resistance via stabilizing PKM2 to promote glycolysis in triple-negative breast cancer. Cell Death Dis 17, 261 (2026). https://doi.org/10.1038/s41419-026-08521-7
Anahtar kelimeler: üçlü negatif meme kanseri, paklitaksel direnci, tümör metabolizması, glikoliz, PKM2