Clear Sky Science · tr
SETD2 tarafından histon 3 lizine 36 trimetilasyonu, bağırsak kök hücrelerinde epigenetik bir manzara oluşturarak lipid metabolizmasını yönlendirir ve hücre senesansını azaltır
Yaşlanırken Bağırsak Kök Hücrelerinin Neden Önemli Olduğu
Bağırsaklarımızın örtüsünün derinliklerinde, yiyecekleri sindirmemize ve besinleri emmemize yardımcı olan dokuyu sürekli yenileyen küçük kök hücreler aralıksız çalışır. Yaşlandıkça bu kök hücreler yorulur; bu da bağırsağın hastalıklara daha açık hale gelmesine ve iyileşmenin yavaşlamasına yol açar. Bu çalışma, DNA paketleme proteinleri üzerindeki ince kimyasal işaretlerin bağırsak kök hücrelerini genç tutmada nasıl rol oynadığı, bunların kaybının hücre içi yağ yakımını nasıl bozduğu ve özenle seçilmiş ilaçların bir gün bu düşüşü nasıl yavaşlatabileceğini araştırıyor.
Zorlu Bir Ortamda Yaşlanan Hücreler
Bağırsak iç yüzeyi vücudun en hızlı yenilenen dokularından biridir. Kript adı verilen küçük çukurların diplerine yerleşmiş kök hücreler, birkaç günde milyarlarca hücreyi yenilemek için bölünür. Bu sürekli çalışma, büyük ölçüde yağların parçalanmasından sağlanan düzenli bir enerji arzı gerektirir. Aynı zamanda bu kök hücreler, hangi genlerin aktif veya sessiz olacağını belirlemede rol oynayan histon proteinleri üzerindeki kimyasal işaretlerden oluşan bir “epigenetik” kodla kontrol edilir. Yazarlar, SETD2 adlı bir enzim tarafından oluşturulan H3K36 trimetilasyonu olarak bilinen bu işaretlerden birine odaklandı ve bu işaretteki değişikliklerin bağırsak kök hücrelerinin enerjisini neden kaybettiğini açıklayıp açıklamayacağını incelediler.
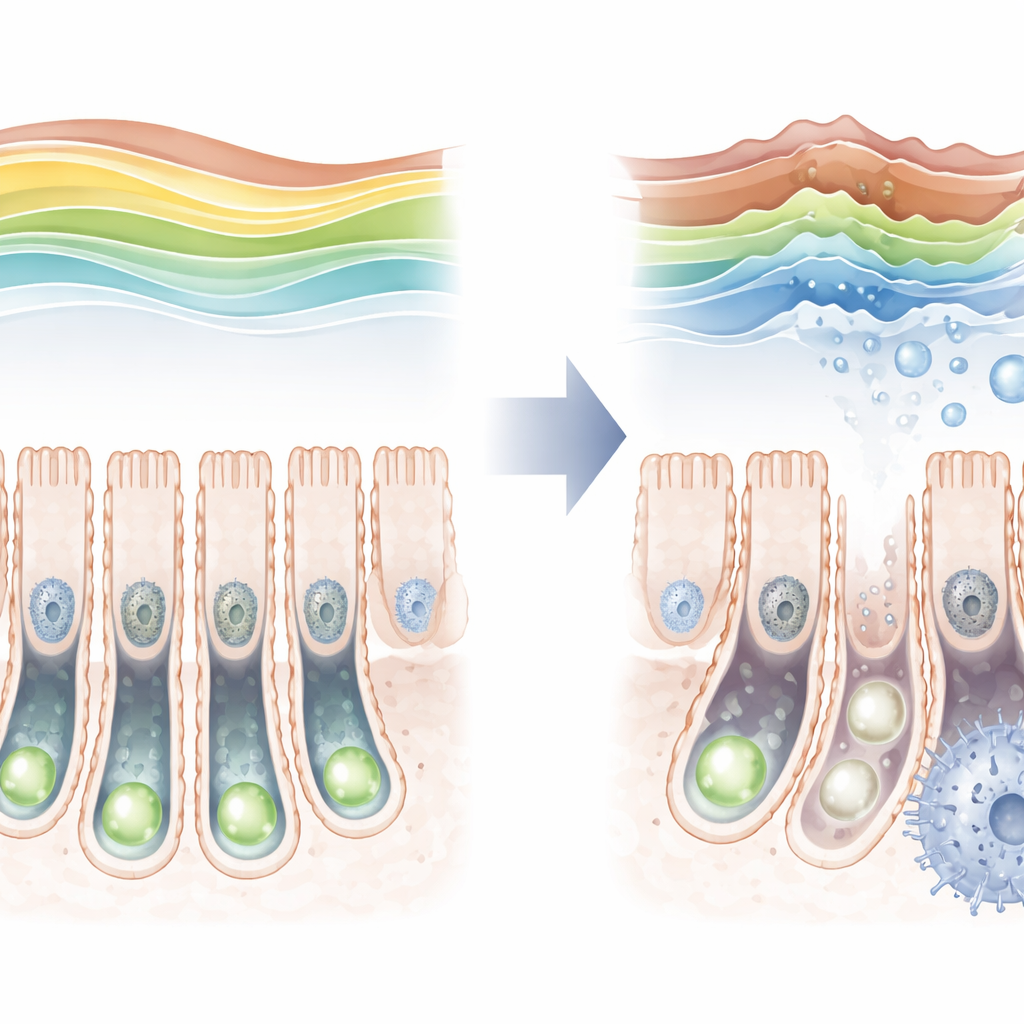
Yaşla Azalan Koruyucu Bir İşaret
Fare bağırsaklarını yaşam boyunca inceleyerek araştırmacılar, H3K36 trimetilasyonunun sabit olmadığını buldular. Doğum sonrası dönemde görece düşük, genç erişkinlikte zirveye çıkan ve ileri yaşta tekrar düşen bir profili vardı. Bu işaret yaşlı hayvanlarda azaldıkça, kök hücrelerde hücresel yaşlanma belirteçleri arttı; bu da ikisi arasında bir bağlantıya işaret ediyor. Bunu daha doğrudan test etmek için ekip, SETD2’nin yalnızca bağırsak kök hücrelerinde çıkarılabildiği fareler oluşturdu. Bu enzim silindiğinde koruyucu işaret neredeyse kayboldu, kök hücrelerin bölünme sıklığı düştü ve uzmanlaşmış bağırsak hücrelerinin tüm çeşitlerini üretmekte zorlandılar.
Epigenetik Değişikliklerin Yağ Yakımını Nasıl Raydan Çıkardığı
Tek bir histon işaretinin kaybı, kök hücrelerin içinde bir dizi değişikliği tetikledi. Gen aktivitesi ölçümleri, hücre döngüsü ve DNA kopyalanmasıyla ilişkili birçok genin aşağıya çekildiğini, stres ve yaşlanmayla ilişkili genlerin ise yukarıya çıktığını gösterdi. Çarpıcı biçimde, en güçlü sinyal bozulmuş lipid işleme yönündeydi: normalde yağ asidi oksidasyonunu—yağların enerji için kontrollü yakılmasını—destekleyen genler baskılanmış ve kriptlerin içinde yağ birikmeye başlamıştı. Metabolit profillemesi, uzun zincirli yağ asitlerinin biriktiğini doğruladı; bu, olağan yağ işleme yolaklarının aksadığının bir göstergesiydi. Aynı zamanda, çekirdekte DNA’nın fiziksel paketlenmesi değişti; birçok bölge daha açık veya daha sıkı kapanmış hale gelerek hücrenin kolayca kullanabileceği gen setini yeniden şekillendirdi.
Kromatin Yeniden Düzenleyiciler ve Senesansa Yürüyüş
Bu DNA paketleme değişikliklerinin nasıl ortaya çıktığını anlamak için yazarlar, genom boyunca hem açık kromatin bölgelerini hem de diğer bir dizi histon işaretini haritaladılar. H3K36 trimetilasyonu kaybolduğunda, metabolizma ve yaşlanmayla ilişkili genlerin yakınlarında özellikle olmak üzere geniş DNA bölgeleri “aktif” işaretler kazanıp daha erişilebilir hale geldi. Bu geçişte kilit rol oynayan unsur, çekirdek bir alt birimi SMARCA4 olan SWI/SNF kromatin yeniden düzenleme kompleksiydi. SETD2 eksikliği bulunan kök hücrelerde SMARCA4 düzeyleri arttı ve kompleks senesans programlarını tetikleyen bölgeleri açmaya yardımcı oluyor gibiydi. Araştırmacılar SMARCA4 aktivitesini genetik olarak azalttıklarında veya hedeflenmiş bir inhibitör kullandıklarında, kök hücreler bir tabakta sağlıklı mini-bağırsaklar oluşturma yeteneklerinin bir kısmını geri kazandı ve yaşlanma belirteçleri azaldı—bu da aşırı yeniden düzenlemenin bu hücreleri yorulmuş, senescent bir duruma ittiğini düşündürüyor.
Kök Hücreleri Kurtarmak İçin Enerji Yolaklarını Yeniden Uyandırmak
Bozulmuş yağ yakımı merkezi bir sorun olarak ortaya çıktığı için ekip, bu yolak güçlendirilirse kök hücre yaşlanmasına karşı koyup koyamayacağını test etti. Yağ asidi oksidasyonunun ana düzenleyicilerinden biri olan PPARα’yı aktive eden bir ilaç kullandılar. SETD2 eksik kök hücrelerden yetiştirilen organoidlerde bu tedavi büyümeyi artırdı, enerjik kök hücrelere özgü tomurcuklanma yapılarını geri getirdi ve yağ birikimini azalttı. Canlı farelerde aynı müdahale, kök hücre havuzunu kısmen yeniledi, senesans belirteçlerini düşürdü ve bağırsak kriptlerindeki lipid birikimini normale yaklaştırdı. Bu bulgular, yağ asidi oksidasyonunu epigenetik kontrol ile kök hücre sağlığı arasındaki kritik bir bağ olarak konumlandırıyor.
Sağlıklı Yaşlanma İçin Ne Anlama Geliyor
Bir araya getirildiğinde bu çalışma, SETD2 tarafından bırakılan belirli bir histon işaretinin bağırsak kök hücrelerinde dengeli bir epigenetik manzara korumaya yardımcı olduğunu gösteriyor. Bu işaret azaldığında, kromatin anormal biçimde yeniden düzenleniyor, yağ yakım yolları aksıyor, lipidler birikiyor ve hücreler senesansa doğru kayarak bağırsak onarım sistemini zayıflatıyor. Aşırı yeniden düzenleyici makinayı yatıştırmak veya hedefe yönelik ilaçlarla yağ metabolizmasını geri getirmek yoluyla, kök hücre fonksiyonunu ve bağırsak sağlığını ileri yaşlarda korumak mümkün olabilir. Bu bulgular farelerden elde edilse de, insan bağırsak hastalıklarında görülen desenleri yansıtıyor ve ince ayarlanmış metabolik tedavilerin bir gün kendi bağırsak kök hücrelerimizdeki yaşa bağlı gerilemeyi karşılayabileceği olasılığını gündeme getiriyor.
Atıf: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Anahtar kelimeler: bağırsak kök hücreleri, epigenetik, yağ asidi oksidasyonu, hücresel senesans, SETD2