Clear Sky Science · tr
ADSC’lerden salınan Lamp2a-bağlı bir RNA, TNBC’de ENO1–laktillasyon–glikoliz geri beslemesini ve hücre malign davranışını engelliyor
Hastalar için bunun önemi
Üçlü negatif meme kanseri, en agresif meme kanseri türlerinden biridir ve diğer alt tipleri daha tedavi edilebilir kılan hormon veya büyüme faktörü hedeflerinden yoksundur. Bu çalışma, bu tümörlerin düşük oksijenli ortamlarda hayatta kalmak için enerji kullanımını nasıl yeniden düzenlediğini açığa çıkarıyor ve o devreleri hedeflemenin yaratıcı bir yolunu tanımlıyor. Okuyucular için, kanser metabolizmasının anlaşılmasının geleneksel kemoterapiden belirgin şekilde farklı, çok hedefli yeni tedavilere nasıl yol açabileceğine dair bir pencere sunuyor.
Bu tümörler kendilerini nasıl besliyor
Birçok kanser, şekeri laktat yan ürüne çeviren hızlı ama verimsiz bir enerji üretim yolu olan glikolize yoğun biçimde dayanır. Hasta örnekleri, kamuya açık gen veri tabanları ve birden çok meme kanseri hücre hattını inceleyerek araştırmacılar, üçlü negatif tümörlerin diğer meme kanserlerine göre glikolize daha fazla bel bağladığını gösteriyor. Bu yolakta kilit bir enzim olan ENO1, bu tümörlerde özellikle yüksek düzeyde bulunuyor ve daha kötü sağkalımla ilişkilendiriliyor. Laboratuvarda yetiştirilen üçlü negatif hücrelerde ENO1 düzeyleri azaltıldığında hücreler glikolizden mitokondride daha normal enerji üretimine kaydı, daha yavaş büyüdü ve invade etme ya da koloni oluşturma yetenekleri azaldı.
Kanser hücreleri içinde tehlikeli bir geri besleme döngüsü
Daha derine indiğinde ekip, laktatın kendisinin ENO1’i güçlendirip kanser hücrelerini kısır bir döngüye kilitlediğini keşfetti. Laktat, proteinleri laktillama adı verilen kimyasal bir işlemle değişikliğe uğratabilir. Üçlü negatif hücrelerde fazladan laktat, ENO1’in laktillasyonunu artırdı; bu da enzimin aktivitesini ve kararlılığını yükselterek glikolizi daha da hızlandırdı ve daha fazla laktat üretildi. Katı tümörlere özgü olan düşük oksijen koşullarında bu döngü güçlendi, kanser hücrelerinin hücre ölümüne direnmesine ve çoğalmaya devam etmesine yardımcı oldu. Küçük moleküllü bir inhibitörle ENO1 aktivitesinin engellenmesi veya laktat üretiminin azaltılması bu döngüyü zayıflattı, glikolizi kısıtladı ve farelerde tümör büyümesini yavaşlattı.
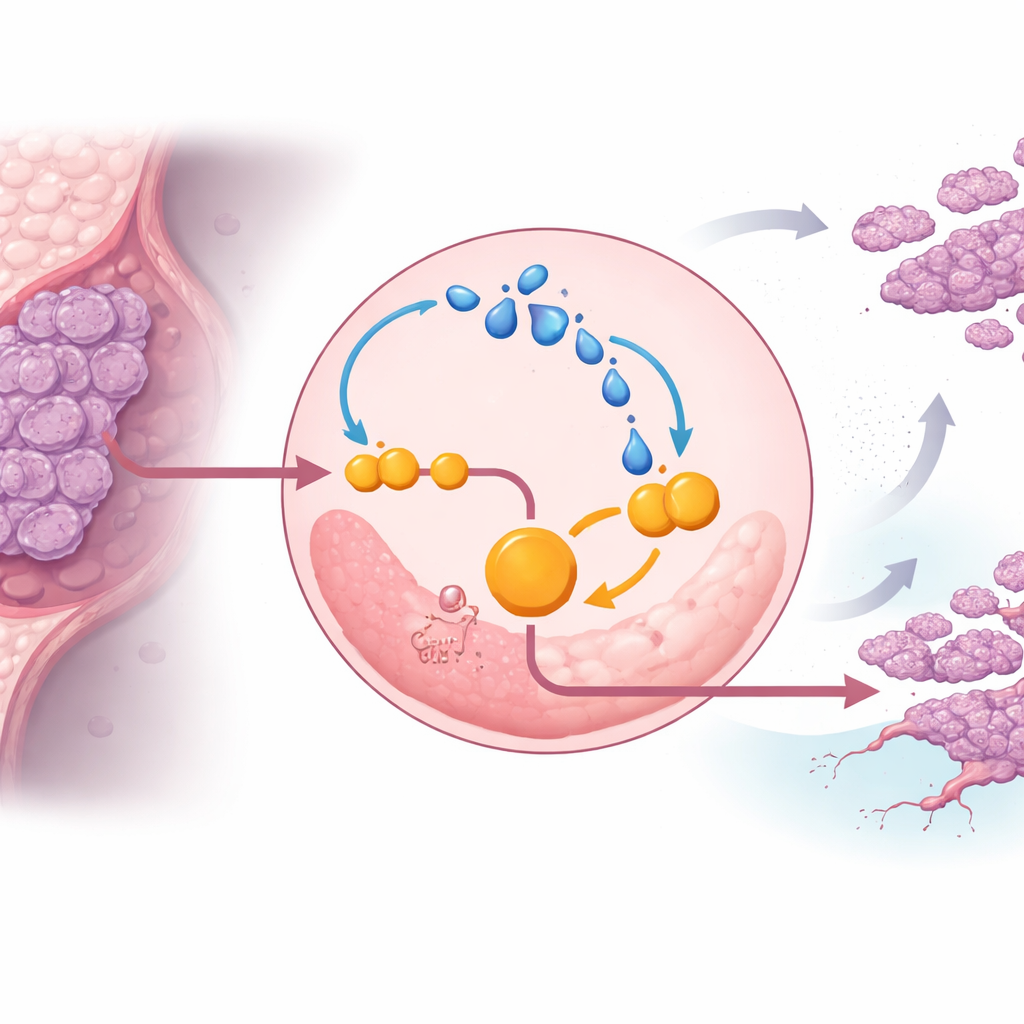
ENO1’i koruyan moleküler anahtar
Çalışma, bu döngüyü mümkün kılan ENO1 üzerindeki belirli bir kontrol noktasını tanımladı. EP300 olarak bilinen bir protein, ENO1’de birkaç lizin bölgesine laktat bazlı işaretler ekliyor ve K262 olarak adlandırılan bir bölge özellikle kritik çıktı. Bu bölge laktillanamayacak şekilde değiştirilince ENO1 hızla hücrenin geri dönüşüm merkezleri olan lizozomlara yönlendirildi ve parçalandı. Bu koruyucu işaret yoksa üçlü negatif hücreler glikolitik itici güçlerinin ve hayvan modellerinde tümör ve metastaz oluşturma yeteneklerinin büyük kısmını kaybetti. Bu, ENO1’in K262’deki laktillanmasını enzimi yok olmaktan koruyan ve kanserin değişmiş metabolizmasını sürdüren moleküler bir anahtar olarak öne çıkarıyor.
ENO1’i yok işaretlemenin yeni bir yolu
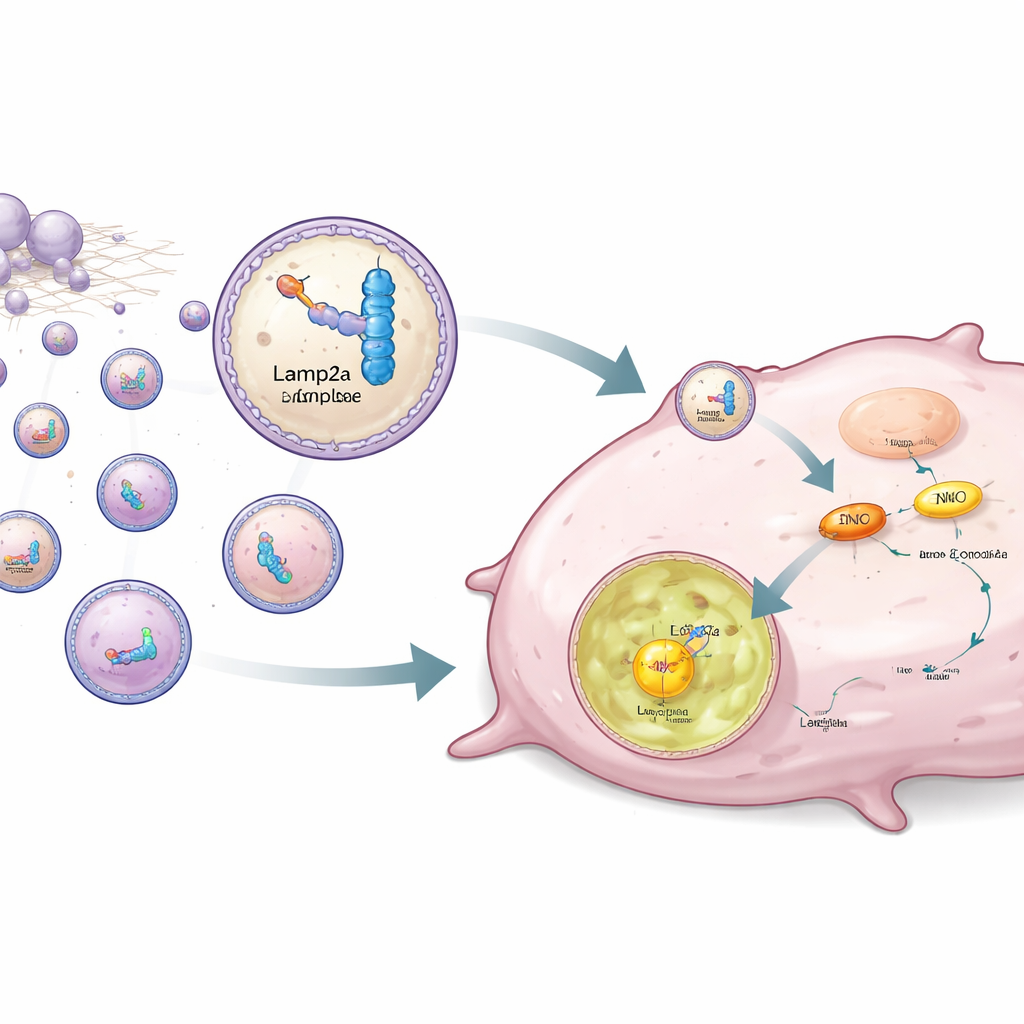
Yalnızca ENO1’i engellemek yerine yazarlar, onu seçici olarak kanser hücrelerinden uzaklaştırma stratejisi tasarladılar. ENO1 ayrıca belirli kısa RNA dizilerini tanıyan bir RNA-bağlayıcı protein olarak davranır. Ekip, ENO1’e güçlü bağlanan sentetik RNA parçaları tasarladı ve bunları hedeflenmiş protein degradasyonunda rol alan lizozomal membran proteini Lamp2a’ya bağladı. İnsan yağ kaynaklı kök hücreler genetik olarak bu RNA–Lamp2a çiftini üretmek ve bunları eksozom adı verilen küçük veziküllere paketlemek üzere değiştirildi. Bu mühendislik ürünü eksozomlar üçlü negatif hücrelere eklendiğinde, RNA kısmı ENO1’e tutunurken Lamp2a kısmı tüm kompleksi lizozomlara yönlendirerek ENO1’in, stabilite sağlayan laktillasyon işareti taşısa bile, parçalanmasını sağladı.
Hayvanlarda hedeflenmiş degradasyon yaklaşımını test etmek
Bu fikri pratik bir terapinin sınırına yaklaştırmak için araştırmacılar, değiştirilmiş kök hücreleri biyobozunur bir iskelet üzerine büyüttü ve bu yapıyı üçlü negatif tümörlerin yakınında farelerin derisi altına implant etti. Bu konumdan kök hücreler, ENO1’i hedefleyen kompleksleri taşıyan eksozomları sürekli olarak saldı. Bu farelerdeki tümörler, kontrol hayvanlarla karşılaştırıldığında belirgin derecede daha düşük ENO1 protein düzeyleri, azalmış glikoliz, daha az bölünen hücre ve daha fazla hücre ölümü belirtisi gösterdi. Tümörler daha yavaş büyüdü ve malign davranışları bariz şekilde zayıfladı; bu da ENO1’i lizozomlara yönlendirmenin tümörü tercih ettiği yakıt yolundan etkili şekilde mahrum bırakabileceğini gösterdi.
Gelecek tedaviler için olası çıkarımlar
Uzman olmayan bir okuyucu için çıkarılacak ana mesaj, bu çalışmanın üçlü negatif meme kanseri için hem bir zayıflık hem de potansiyel yeni bir tedavi açısı ortaya koymasıdır. Zayıflık, özellikle düşük oksijenli bölgelerde ENO1 ve laktat etrafında inşa edilmiş, kendi kendini güçlendiren enerji döngüsüne tümörün bağımlılığıdır. Tedavi açısı ise özel RNA ve kök hücre kaynaklı eksozomları kullanarak ENO1’i hücrenin imha mekanizmasına sürükleyen hedeflenmiş bir protein degradasyon sistemidir. Klinik kullanımdan hâlâ uzak olsa da bu yaklaşım, kanserin metabolik numaralarını derinlemesine anlamanın, kötü huylu hücreleri zehirlemek yerine etkisiz hale getirmeyi amaçlayan hassas tedaviler ilham verebileceğini gösteriyor.
Atıf: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Anahtar kelimeler: üçlü negatif meme kanseri, kanser metabolizması, laktat sinyallemesi, hedeflenmiş protein degradasyonu, ENO1 enzimi